
Термические методы
Термические методы анализа основаны на взаимодействии вещества с тепловой энергией. Наибольшее применение в аналитической химии находят термические эффекты, которые являются причиной или следствием химических реакций. В меньшей степени применяют методы, основанные на выделении или поглощении теплоты в результате физических процессов. Это процессы, связанные с переходом вещества из одной модификации в другую, с изменением агрегатного состояния и другими изменениями межмолекулярного взаимодействия, например, происходящими при растворении или разбавлении. В табл. 14.1 приведены наиболее распространенные методы термического анализа.
Таблица 14.1. Методы термического анализа
Название метода |
Регистрируемый |
Измерительный |
|
параметр |
прибор |
Термогравиметрия |
Изменение массы |
Термовесы |
Термический и диф- |
Выделяемая или по- |
Аппаратура ДТА, диферен- |
ференциальный тер- |
глощаемая теплота |
циальный сканирующий |
мический анализ |
|
калориметр |
Термометрическое |
Изменение |
Адиабатический калори- |
титрование |
температуры |
метр |
Энтапьпиметрия |
Выделяемая или по- |
Тоже |
|
глощаемая теплота |
|
Дилатометрия |
Изменение |
Дилатометры |
|
температуры |
|
Катарометрия |
То же |
Катарометры |
Термические методы успешно используются для анализа металлургических материалов, минералов, силикатов, а также полимеров, для фазового анализа почв, определения содержания влаги в пробах.
14.1. Термогравиметрня
Термогравиметрия (ТГ) заключается в измерении потери массы пробы при изменении температуры. Кривые зависимости Am от температу
р ы
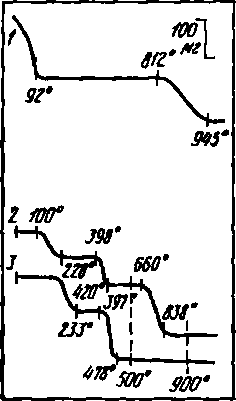
называются термогравиграммами (рис.
14.1). Часто изменение массы не очень ярко
выражено. Тогда целесообразно построить
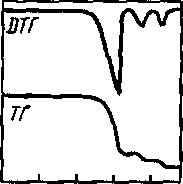
дифференциальную кривую (ДТГ) в координатах
Ат/АТ
=
/(Т)
(рис.
14.2). Термогравиграммы позволяют
проследить за ходом превращения
вещества в процессе нагревания. При
этом происходят разные химические
реакции: разложение, окисление и
восстановление, дегидратация,
замещение и т. п. Кривые можно использовать
для решения ряда задач.
ы
называются термогравиграммами (рис.
14.1). Часто изменение массы не очень ярко
выражено. Тогда целесообразно построить
дифференциальную кривую (ДТГ) в координатах
Ат/АТ
=
/(Т)
(рис.
14.2). Термогравиграммы позволяют
проследить за ходом превращения
вещества в процессе нагревания. При
этом происходят разные химические
реакции: разложение, окисление и
восстановление, дегидратация,
замещение и т. п. Кривые можно использовать
для решения ряда задач.
1. По потере массы можно судить о содержании определяемого компонента.
/ — хромата серебра; 2 — ок-салата кальция; 3 — оксалата магния
2. Можно установить интервал тем- ператур устойчивости разных форм веще- ства, в том числе гравиметрической фор- мы, что очень важно при определении веществ гравиметрически.
Например, потеря массы до 92 °С (рис. 14.1, кривая /) означает удаление промывной и адсорбированной воды. В интервале 812—945 °С протекает реакция
A gjCr04
->
02
+
Ag
+
AgCrOj
gjCr04
->
02
+
Ag
+
AgCrOj
Таким образом, при определении хрома в виде хромата серебра осадок следует прокаливать в интервале 100—800 °С.
3. Термогравиграммы дают информацию о составе соединений на разных стадиях разло- жения.
200
400 600 800 1'С
В качестве примера рассмотрим кривые
разложения оксалатов кальция и магния (см. рис. 14.1). Кривая 2 состоит из четырех площадок и трех резких скачков. Скачки соответствуют следующим процессам:
1) потеря воды (100—115° С) по уравнению
СаС204 • wH20 -* CaC204 Н20 + (и - 1)Н20
потеря молекулы воды моногидратом оксалата кальция (115—200 °С),
разложение оксалата до карбоната (400—420 °С)
СаС204 -» СаС03 + СО
4) разложение карбоната кальция (660—840 °С)
СаСО3-»Са0 + СО2
Разложение оксалата магния протекает в две стадии (кривая 3):
MgC204 • «Н20 -> MgC204 + лН20 (до 230 °С),
MgC204 MgO + СО + С02 (400—800 °С).
Если прокалить СаС204 и MgC204 при 500° С, а затем при 900 °С, можно рассчитать содержание Са и Mg в исходной смеси. При 500 °С осадок содержит СаСО, + MgO, при 900 °С — СаО + MgO.
Для непрерывной регистрации потери массы служат одночашечные аналитические весы с автоматическим регулированием температуры — термовесы.
Интервал потери массы зависит от ряда внешних факторов: скорости нагревания, массы осадка, скорости химической реакции при нагревании, наличия посторонних веществ. Например, на рис. 14.3 система имеет два устойчивых равновесных состояния: при температурах ниже Г, и выше Г,. Тогда если по мере нагревания до Тх выжидали время, необходимое для достижения равновесия, то изменение массы при изменении Г,
должно выглядеть так, как это изображено сплошной линией (резкая ступенька). При повышении скорости изменения Г протяженность участка до 7", будет возрастать с ростом
скорости, а при и-»аз ступенька 1 р~
вовсе исчезает. Все это следует учи- тывать при проведении анализа тер- 1
Рис- из- Термогравиметрические кри-
могравиметрическим методом. вые "Ри Р"3"0" СКОРОСТИ нагРев"»»v,<v,<v.
