
- •1 Основное кинетическое уравнение массопередачи. Коэффициент массопередачи и движущая сила процесса.
- •2 Движущая сила массообменного процесса при нелинейной равновесной зависимости. Число единиц переноса и его физический смысл.
- •3.Выражение для средней движущей силы и числа единиц переноса при линейной равновесной зависимости.
- •4.Модифицированные уравнения массопередачи. Число единиц переноса. Высота эквивалентная единице переноса.
- •6.Массобмен в системах без твердой фазы . Молекулярная и конвективная диффузия.
- •8.Молекулярная диффузия. Первый закон Фика. Коэффициент диффузии и его физический смысл.
- •9.Уравнение Щукарева. Коэффициент масоотдачи и его физический смысл, сопоставление с коэф. Массопередачи.
- •10.Выражение коэф массопередачи через коэф массоотдачи.
- •11.Равновесие в системах газ-жидкость. Закон Генри. Ур-е равновесной зависимости. Влияние давления и температуры на абсорбцию.
- •12.Равновесие в процессах пар-ж для идеальных смесей. Закон Рауля. Диаграммы t-X-y и X-y.
- •13. Принципиальная схема противоточной абсорбции и графическое изображение процесса.
- •14. Принципиальная схема абсорбции с рециркуляцией жидкости и графическое изображение процесса.
- •15. Схема ректификационной установки непрерывного действия. Материальный баланс ректификационной колонны. Флегмовое число.
- •16. Уравнения рабочих линий процесса ректификации для непрерывно действующей ректификационной колонны. Минимальное и оптимальное флегмовое число.
- •18. Влияние флегмового числа на размеры ректификационной колонны и расход тепла при ректификации. Оптимальное флегмовое число.
- •20. Схема периодически действующей ректификационной установки. Изображение процесса в у-х диаграмме при постоянном составе дистиллята.
- •22Построение кинетической кривой и определение числа тарелок.
- •23. Порядок расчета ректификационной тарельчатой колонны.
- •24.Гидравлический расчет тарельчатых абсорбционных(ректификационных)колонн.
- •21. Тепловой баланс процесса ректификации
- •27.Непрерывная противоточная экстракция .Материальный баланс.Графическое изображение процесса.
- •28.Ступенчатая противоточная экстракция .Принципиальная схема .Графическое изображение процесса.
- •29. Многократная экстракция с противотоком растворителя.
- •30. Массопередача в системах с твёрдой фазой.Массопроводность.Диф-ные ур-ния массопров-ти.
- •31. Процесс сушки. Технические способы проведения процесса. Виды связи влаги с материалом.
- •32. Основные способы сушки. Материальный баланс конвективной сушки.
- •33 Диаграмма состояния влажного воздуха (Диаграмма Рамзина)
- •34 Изображение в диаграмме н-х процессов изменения параметров влажного воздуха. Температура точки росы, охлаждение, нагревание, смешивание.
- •35 Уравнение рабочей линии сушки. Построение рабочей линии в н-х диаграмме.
- •36 Тепловой баланс воздушной сушки. Уравнение рабочей линии процесса сушки.
- •37.Параметры, влияющие на процесс сушки. Способы интенсификации сушка.
- •38.Сушка с многократным промежуточным подогревом воздуха. Схема и н-х диаграмма.
- •39.Сушка с частичным возвратом отработанного воздуха.Схема и н-х диаграмма.
- •40.Сушка с замкнутой циркуляцией высушиваемого газа. Схема и н-х диаграмма.
- •41. Процесс адсорбции. Динамическая и статическая активности адсорбентов. Условия, влияющие на
- •42. Физическая сущность процесса адсорбции. Адсорбенты. Условия, способствующие протеканию процесса адсорбции.
- •43. Ионообменные процессы – основные закономерности,
- •44. Кристаллизация. Основные способы проведения кристаллизация. Равновесие в процессах кристаллизации.
- •45. Мембранные процессы. Классификация мембранных процессов в зависимости от их механизма. Область применения.
- •46. Влияние различных параметров на селективность и проницаемость мембран
- •47. Материальный и тепловой баланс изогидрической кристаллизации
- •48. Материальный и тепловой баланс кристаллизации с удалением части растворителя.
1 Основное кинетическое уравнение массопередачи. Коэффициент массопередачи и движущая сила процесса.
Основной
закон массопередачи можно сформулировать,
исходя из общих кинетических закономерностей
химико-технологических
процессов.
jм=![]() =
=![]() =Kм*ΔС
– основной закон кинематики
=Kм*ΔС
– основной закон кинематики
Скоростью любого процесса МП будет называться количество вещества М, которое передается из одной фазы в другую через единицу поверхности контакта фаз F в единицу времени τ. [кг/м2 *ч]
М=Км*ΔС*F, где Км – коэффициент массопередачи (скорость процесса), С-концентрация
Км=![]() [кг/ед конц*м2]
[кг/ед конц*м2]
В аппаратуре, используемой для проведения массообменных процессов, равновесные концентрации распределяемого вещества никогда не достигаются. Действительные концентрации распределяемого вещества, или рабочие концентрации, всегда отличаются от равновесных. Разность между этими концентрациями, характеризующая степень отклонения от равновесия, и представляет собой движущую силу массообменных процессов.
2 Движущая сила массообменного процесса при нелинейной равновесной зависимости. Число единиц переноса и его физический смысл.
Как было указано ранее, движущая сила массообменных процессов определяется степенью отклонения от равновесия. Определяется разностью между рабочей и равновесной концентрациями или равновесной и рабочей, в зависимости от того, какие из них больше. При этом очевидно, что движущую силу можно выражать либо через концентрации распределяемого вещества в фазе G, т. е. через Δy, либо через концентрации его в фазе L, т. е. через Δx.
Ниже указаны возможные варианты выражения движущей силы массообменных процессов при различных направлениях перехода распределяемого вещества. Поскольку концентрации распределяемого вещества можно выражать любыми способами, важно подчеркнуть, что во всех случаях движущей силой процесса будет разность между рабочей и равновесной концентрациями, взятая с положительным знаком.
GL LG

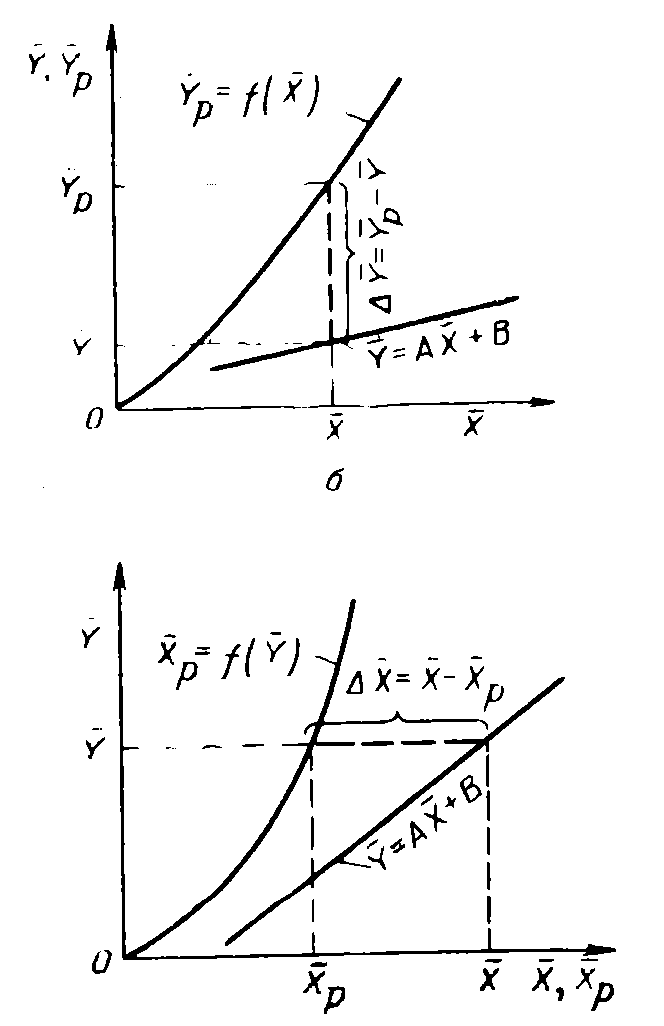
Из изложенного следует, что основное уранвение массопередачи можно записать:
dM=Ky*Δy*F=Kx*Δx*F, то есть Ky*Δy=Kx*Δx
Для одного и того же процесса, как правило Ky≠Kx и Δy≠Δx
Как видно из рисунков, движущая сила меняется с изменением рабочих концентрации, поэтому для всего процесса массообмена, протекающего в пределах концентраций от начальных до конечных, должна быть определена средняя движущая сила (Δyср и Δxср)
П ри
определении средней движущей силы могут
встретиться 2 случая:
ри
определении средней движущей силы могут
встретиться 2 случая:
- зависимость между равновесными концентрациями не линейна; для этого случая равновесная концентрация определяется общей функциональной зависимостью yp=f(x)
- зависимость между равновесными концентрациями линейна, т.е. yp=Ap*x(где Ар – постоянная величина)
Первый случай:
М=G*(yн-yк)=L*(xк-xн)=Ky*Δy*F=Kx*Δx*F
F=G*(yн-yк)/Ky*Δy, где (yн-yк)/Δy=my, аналогично для mx
F=L*(xк-xн)/Kx*Δx, где (xк-xн)/Δx=mx
mx и my – число единиц переноса, которое показывает на сколько единиц изменяется рабочая концентрация под действием единицы движущей силы
Δyср=yн-yк/![]()
Δxср=xк-xн/![]()
