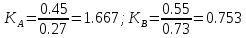Laboratornaya_Rabota_Fkhot_1
.docxМИНОБРНАУКИ РОССИИ
Санкт-Петербургский государственный
электротехнический университет
«ЛЭТИ» им. В.И. Ульянова (Ленина)
Кафедра микро и наноэлектроники
Отчёт по лабораторной работе №1
«Моделирование диаграмм состояния полупроводниковых систем с неограниченной растворимостью компонентов в жидкой и твердой фазах»
|
Студент гр. 4206 |
|
Петросян Л.Б. |
|
|
|
Базаня |
|
Преподаватель |
|
Александрова О.А. |
Санкт-Петербург
2016
Цель работы – изучение фазовых равновесий в бинарных полупроводниковых системах с непрерывным твердым раствором методом компьютерного моделирования; расчет параметров межатомного взаимодействия; выбор моделей растворов, адекватно описывающих экспериментальную Т-х проекцию диаграммы состояния
В лабораторной работе исследовался твердый раствор CdTe – ZnTe.
Исходные данные (температуры плавления, энтальпии плавления и координаты точек ликвидуса и солидуса) представлены на рисунке 1.
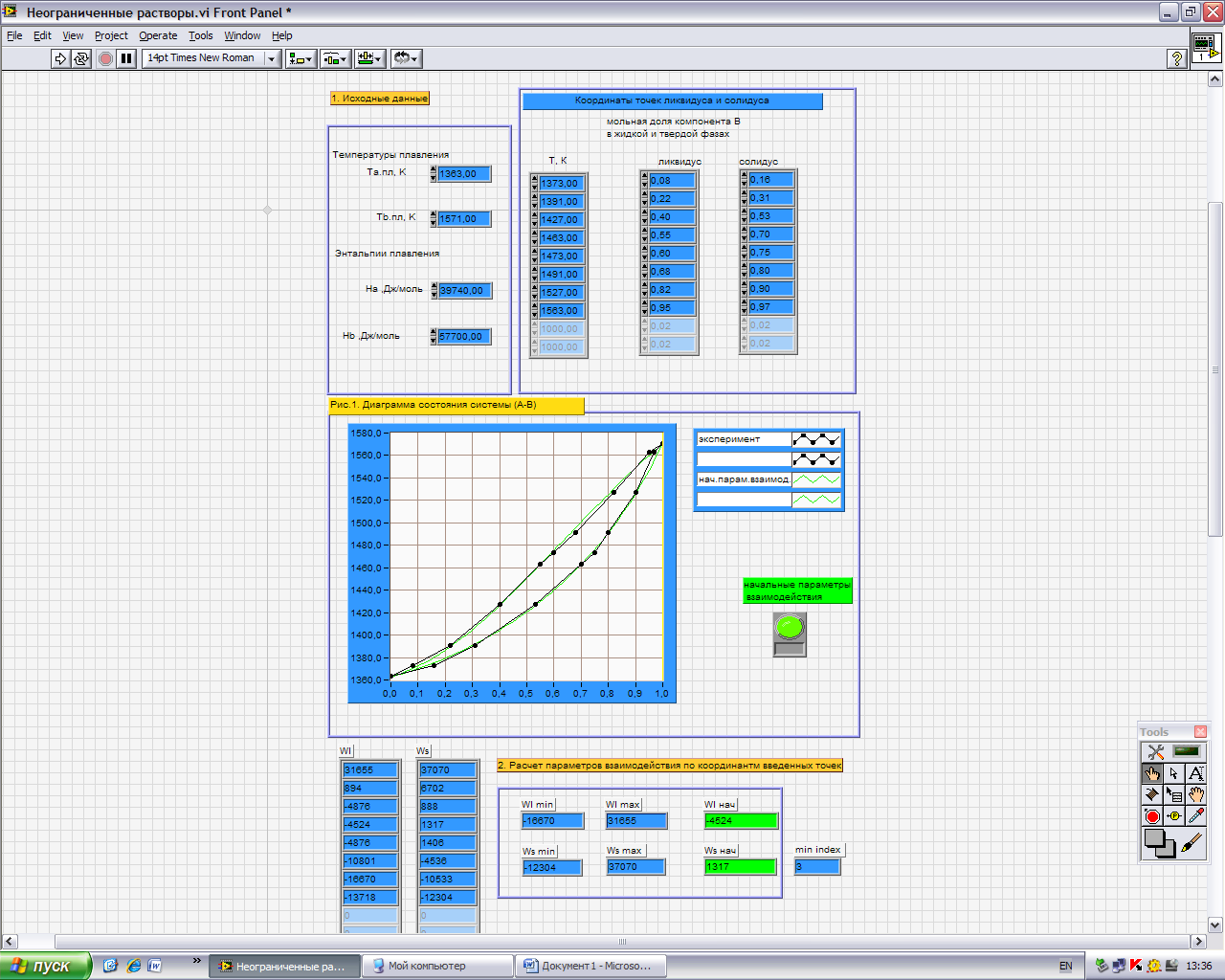
Рисунок 1 - Исходные данные
-
T-x проекция диаграммы состояния.
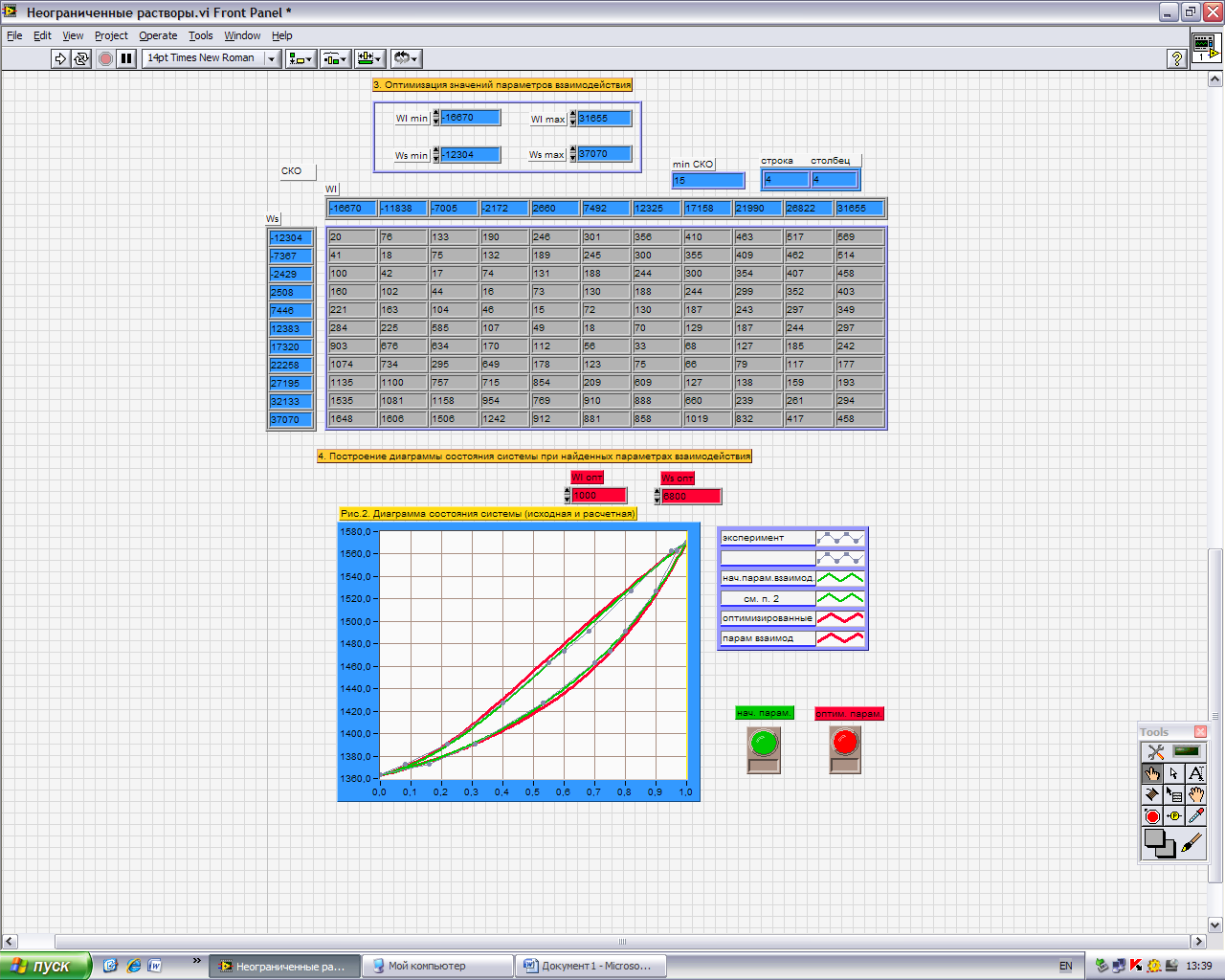
Рисунок 2 - Т-х диаграмма, полученная в ходе лабораторной работы. (Зеленая кривая - эксперимент; Красная кривая - оптимизированная)
Оптимальными
значениями параметров взаимодействия
(при которых СКО наименьшее) являются
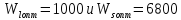 .
Отклонение экспериментальной кривой
и оптимизированной не превышает 1%.
.
Отклонение экспериментальной кривой
и оптимизированной не превышает 1%.
-
T-x проекция диаграммы состояния при обратном знаке параметров взаимодействия
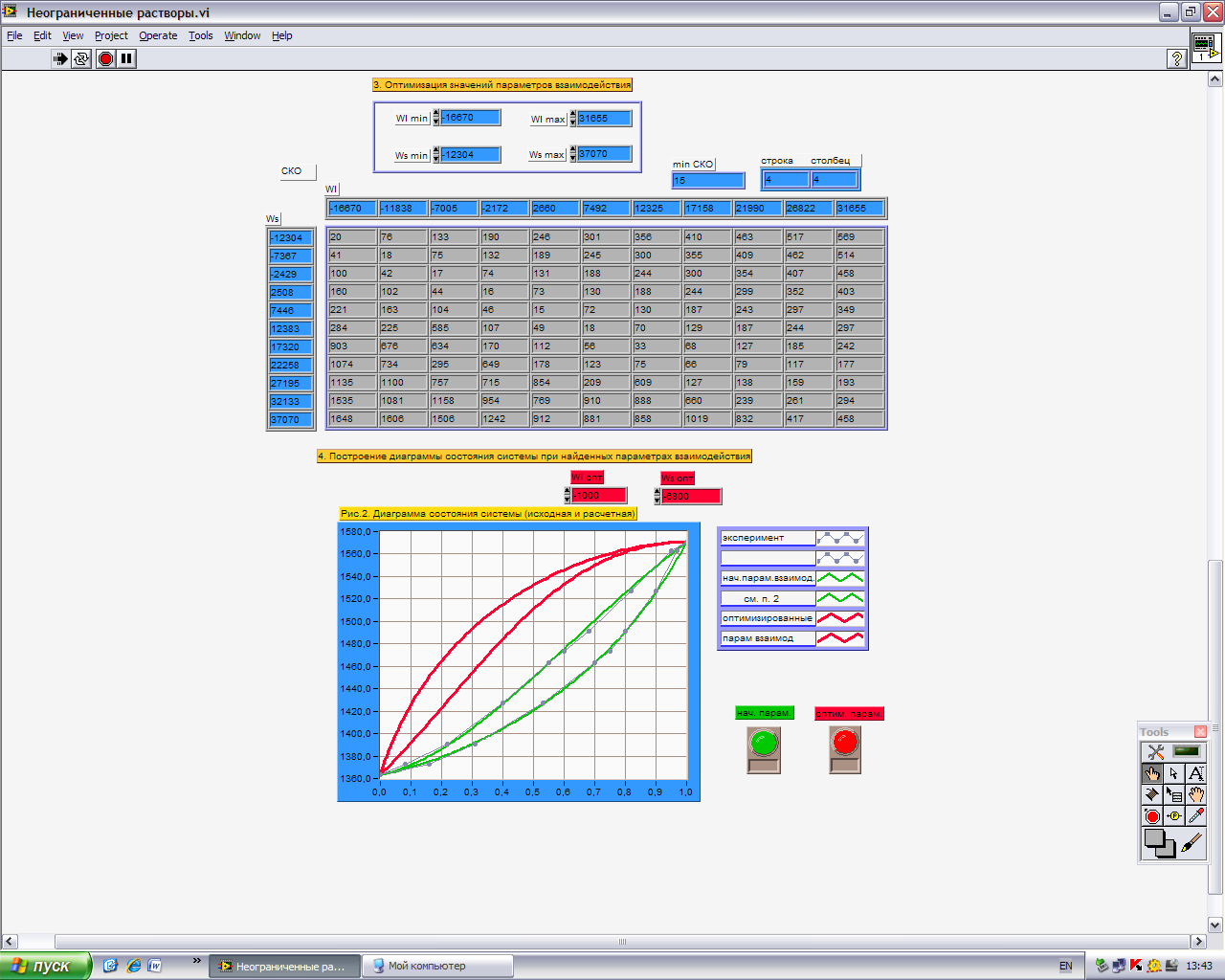
Рисунок 3 - Т-х диаграмма, при обратном знаке параметров взаимодействия (Зеленая кривая - эксперимент; Красная кривая - оптимизированная)
-
Термодинамические функции смешения
Построим концентрационные зависимости термодинамических функций смещения раствора, в соответствии с теорией Дж. Гильдебранда:
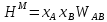
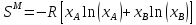
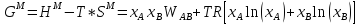
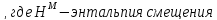
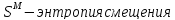
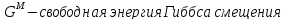
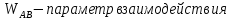
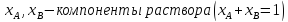
-
Жидкий раствор

Рисунок
4 –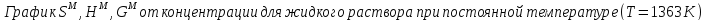

Рисунок 5 – Концентрационные зависимости энергии Гиббса для механической смеси (жидкий раствор)
-
Твердый раствор
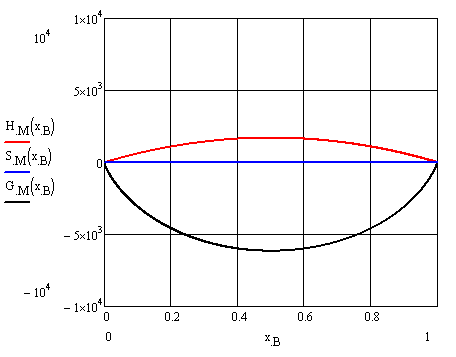
Рисунок
6 -
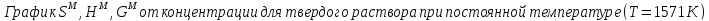
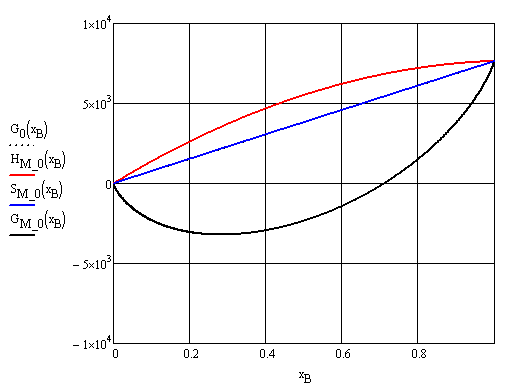
Рисунок 7 – Концентрационные зависимости энергии Гиббса для механической смеси (твердый раствор)
-
Активности компонентов и их коэффициенты активностей
Построим (а также сравним с классической теорией) концентрационные зависимости коэффициентов активностей и активностей компонентов в твердом и жидком растворах при Т=const, согласно теории активности Льюиса:
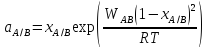
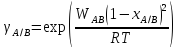
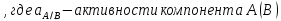
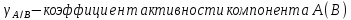
-
Жидкий раствор
|
а) |
б) |
|
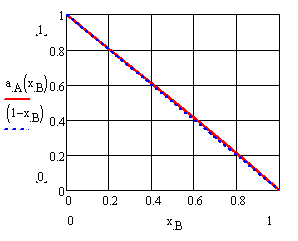
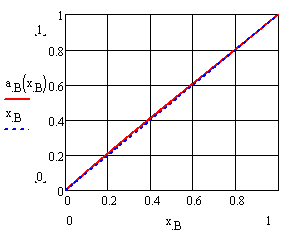
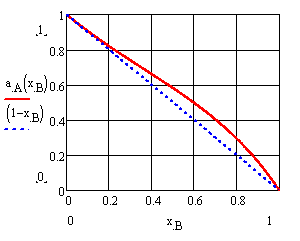
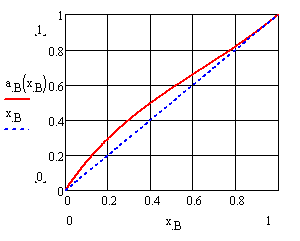
Рисунок 8 – Концентрационные зависимости активностей компонентов в жидком растворе a) А (CdTe), б) B (ZnTe) |
|
|
а) |
б) |
|
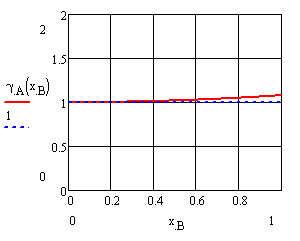
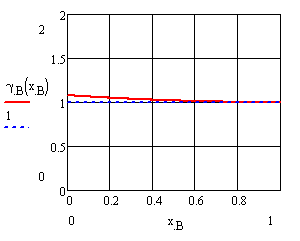
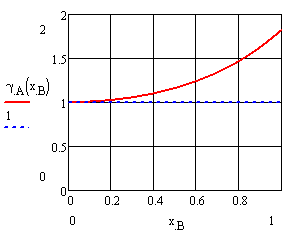
Рисунок 9 – Концентрационные зависимости коэффициентов активностей компонентов в жидком растворе a) А (CdTe), б) B (ZnTe) |
|
-
Твердый раствор
|
а) |
б) |
|
Рисунок 10 – Концентрационные зависимости активностей компонентов в твердом растворе a) А (CdTe), б) B (ZnTe) |
|
|
а) |
б) |
|
Рисунок 11 – Концентрационные зависимости коэффициентов активностей компонентов в твердом растворе a) А (CdTe), б) B (ZnTe) |
|
-
Температурная зависимость коэффициента активности компонентов A и B в твердом растворе.
Температурные
зависимости будем строить для разных
составов раствора
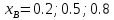
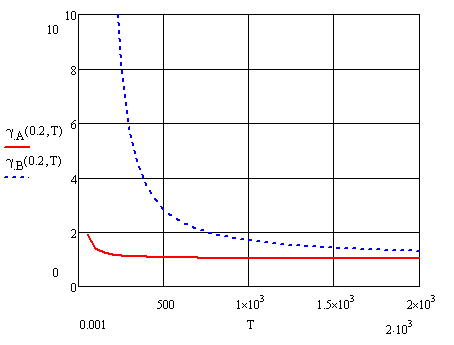
Рисунок
11 – Температурная зависимость коэффициента
активности компонентов А и В при
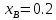
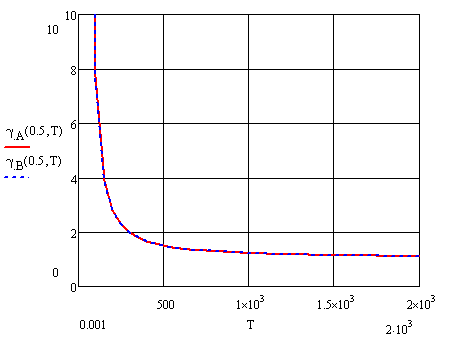
Рисунок
12 – Температурная зависимость коэффициента
активности компонентов А и В при
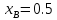
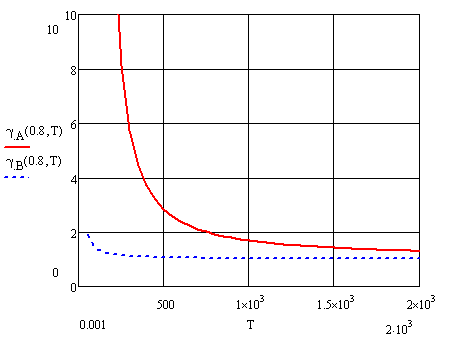
Рисунок
13 – Температурная зависимость коэффициента
активности компонентов А и В при
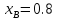
-
Равновесные коэффициенты распределения компонентов А и В
Коэффициенты распределения рассчитаем, используя Т-х диаграмму состояния. Коэффициент распределения находится по формуле
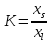
Рассчитывать будем
при температуре равной
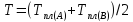 .
.
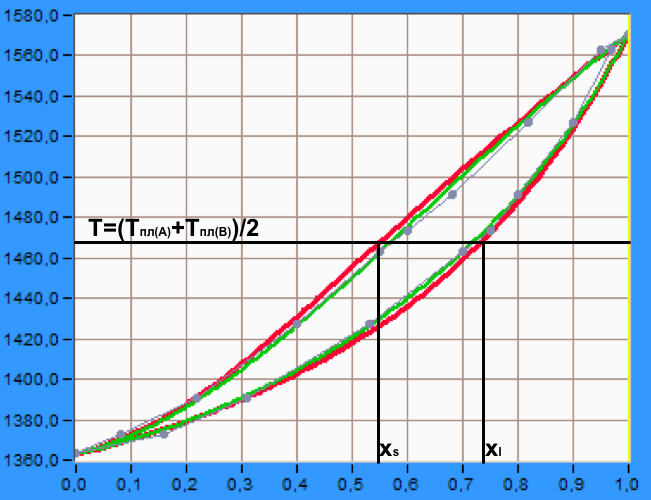
Рисунок 14 – Расчёт коэффициентов распределения
Для компонента B
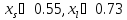 ;
для компонента A
;
для компонента A
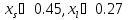 .
.
Следовательно, коэффициенты распределения равны: