
PosobieAnChem1
.pdfПо величине ионной силы в исходном растворе, равной 0,011,
находим Ag+ = OCN– = H+ = ± = 0,90.
Из условия задачи [Ag+] = 1,0 10 4 моль/л ( =1).
Равновесную концентрацию [OCN ] можно найти из системы двух уравнений (поскольку Ка = [Н+] [OCN ]/ [НOCN] = 3,3 10 4):
[OCN ]/ [НOCN] = 3,3 10 4 /1,0 10 2 = 3,3 10 2 и [OCN ] + [НOCN] = 1,0 10 3,
или предварительно вычислив Ка (HOCN) (пример 3.3).
Ка = К0а/ ±2 = 2,7 10 4/0,81 = 3,3 10 4.
Учитывая, что с(OCN ) = [OCN ] + [НOCN] = 1,0 10 3 моль/л и молярная доля OCN– = Ка /(Ка + [Н+]), с учетом уравнения (2.4) на-
ходим [OCN ]:
[OCN ] = OCN– сOCN– = 1,0 10 3 3,3 10 4 /(3,3 10 4 + 1,0 10 2) =
= 3,2 10 5 моль/л;
[Ag+] [OCN ] ±2 = 1,0 10 4 3,2 10 5 0,81 = 2,6 10 9 , что К0S.
Осадок не выпадет.
6.2. Вычисление растворимости малорастворимого электролита
Растворимостью малорастворимого электролита AmBn называют его общую концентрацию в насыщенном растворе, которая обозначается как S (моль/л). В случае преобладания в системе осадок – раствор равновесия 1 (стр. 75), т. е. ионной растворимости, S может быть выражена через общие концентрации ионов А и В.
Если в 1 л раствора перешло S моль электролита AmBn в реак-
ции 1), то, в отсутствие избытка какого-либо из ионов, уравнение реакции растворения можно представить следующими обозначе-
ниями концентраций ионов через величину растворимости S: |
|||
1) AmBn (тв.) |
mA |
+ nB, |
|
а: |
mS A A |
nS В В, |
|
с: |
mS |
|
nS, |
[ ]: |
mS A |
|
nS В. |
Соответственно а = с = [ |
], если для ионов = 1 и = 1. |
|
|||||||
Подставляя в выражение (6.1) |
эти обозначения, получаем для K0S |
||||||||
малорастворимого электролита AmBn уравнение в общем виде: |
|
||||||||
K0 |
= (mS )m |
m m (nS )n n |
n = mm nn·Sm+ n |
m |
m |
В |
n n |
(6.2) |
|
S |
A |
A |
В |
В |
A |
A |
В |
|
|
|
|
|
|
80 |
|
|
|
|
|

и выражение для растворимости электролита AmBn:
|
0 |
|
|
|
|
|
|
S = m n KS mm nn m n |
m n |
m n KS |
mm nn . |
(6.3) |
|||
|
A B |
A B |
|
|
|
|
|
При отсутствии побочных реакций ( A = В = 1) и при I = 0
( A = В = 1) выражение упрощается, и растворимость определяется только природой электролита и температурой (через величину K0S):
|
K 0 |
|
|
|
S = m n |
S |
n n . |
|
(6.4) |
mm |
|
|||
В присутствии избытка одноименного иона, например В с |
||||
концентрацией сВ: |
|
|
|
|
AmBn (тв.) mA |
+ |
nB, |
||
а: |
|
mS A A |
(nS+сВ) В В. |
|
Поскольку одноименный ион уменьшает растворимость, смещая равновесие влево, в расчетах часто пренебрегают величиной nS в
сумме (nS + сВ). Тогда для приближенного расчета растворимости в присутствии одноименного аниона справедливы выражения:
K |
= mm Sm с |
n, |
(6.5) |
|||
|
S |
|
|
|
В |
|
|
1 |
|
|
|
|
|
S |
|
|
KS |
|
(6.6) |
|
|
m |
|
||||
|
m |
|
сn . |
|
|
|
|
|
|
B |
|
|
|
Аналогично, в присутствии избытка катиона (здесь - ион Ат+) с введенной концентрацией сА для приближенного расчета растворимости справедливо выражение:
1 |
|
|
|
|
|
|
|
|
K S |
|
|
S = |
n |
n |
сAm . |
(6.7) |
|
Таким образом, согласно выражениям (6.3, 6.7 и 6.8), растворимость малорастворимого электролита зависит от его природы и температуры; от побочных реакций ионов; от ионной силы раствора, создаваемой посторонними электролитами (“солевой эффект”); от присутствия одноименных с осадком ионов.
В обратной задаче может быть вычислена константа растворимости малорастворимого электролита, если известна величина его растворимости.
Пример 6.7. Вычислить K0S(Ca3(PO4)2), если в 1 л растворяется 2,2 10–4 граммов фосфата кальция.
81

Р е ш е н и е . Найдем растворимость S (моль/л) соли в воде:
|
|
|
m |
|
2,2 10 |
4 |
|
S = с(Ca (PO ) ) = |
= |
|
= 7,1 10–7 моль/л. |
||||
|
|
||||||
|
|
||||||
|
|
|
|||||
3 |
4 |
2 |
MV |
|
312 1 |
|
|
|
|
|
|
|
|||
При такой низкой концентрации ионов в растворе величиной ионной силы можно пренебречь и считать = 1. Пренебрегая побочной реакцией гидролиза аниона, можно считать = 1. Равновесие в системе описывается уравнением:
|
|
Ca (PO ) |
2(тв.) |
3Ca2+ + |
2PO |
3–. |
|
|
|
3 |
4 |
|
|
4 |
|
|
а = с = […]: |
|
|
3S |
2S |
|
|
Вычисляем K0S в соответствии с выражениями (6.1) и (6.2): |
|||||||
K0 |
= K = K |
= [Ca2+]3·[PO 3-]2 |
= (3S)3·(2S)2 = 108S5 |
= 108 (7,1 10-7)5 = 1,9 10-29. |
|||
S |
S S |
4 |
|
|
|
|
|
Пример 6.8. Определить растворимость сульфата бария в
воде. Сколько граммов этой соли растворяется в 1 л воды, если
K0S (ВaSO4) = 1,1 10-10?
Р е ш е н и е . Поскольку в растворе отсутствуют посторонние электролиты, пренебрежем влиянием ионной силы. Побочных ре-
акций не происходит. Как в примере 6.6 при = 1 |
и = 1 по выра- |
|||||||||
жению (6.4) рассчитаем растворимость S: |
|
|
||||||||
|
|
ВaSO4(тв.) |
|
Вa2+ + SO42–. |
|
|||||
[ |
]: |
|
|
|
|
S |
S |
|
||
|
|
|
|
|
|
|
|
|
|
|
S = m n KS0 |
|
|
|
|
|
|
|
|
|
|
|
K |
0 |
1,1 1010 |
1,05 105 |
моль/л. |
|||||
|
mm nn |
|
|
S |
|
|
|
|
|
|
Тогда растворимость в г/л будет соответствовать массе соли m в 1 л
раствора: m = М(ВaSO4) S = 233 1,05 10–5 = 2,4 10–3 г.
Пример 6.9. Определить растворимость сульфида висмута в воде, если K0S(Вi2S3) = 1,0 10–97 (без учета гидролиза).
Р е ш е н и е . Равновесие в системе выражается уравнением:
Вi2S3(тв.) |
2Вi3+ + 3S2-. |
|
[…]: |
2S |
3S |
Вычисления проводим аналогично предыдущему примеру, используя выражение (6.4) (ионная сила мала):
|
m n KS0 |
|
|
|
|
|
|
|
|
|
mm nn = 2 3 |
KS0 |
|
5 1,0 10 97 |
|
–20 |
|
||
S = |
|
22 33 |
= |
|
|
108 = 1,56 10 |
моль/л. |
||
|
|
|
|
82 |
|
|
|
|
|

6.2.1. Влияние ионной силы раствора на растворимость
В присутствии посторонних ионов, создающих вокруг ионов осадка ионную атмосферу, но не вступающих с ними в химические реакции, I 0, и, согласно выражению (6.3), наблюдается увеличение растворимости осадка вследствие уменьшения знаменателя, называемое “солевым эффектом”. В этом случае, а также при достаточно большой концентрации собственных ионов, т. е. при высоком значении K0S ( 1 10-5), учитывают ионную силу раствора и растворимость вычисляют по формуле (при = 1):
|
K 0 |
|
|
|
|
|
|
|
|
S = m n |
S |
m |
n |
|
m |
|
n . |
(6.8) |
|
m |
|||||||||
|
|
n |
A |
B |
|
Пример 6.10. Определить растворимость PbCl2 в воде.
Р е ш е н и е . Так как K0S (PbCl2) = 1,6 10-5, что больше 1·10-5, при расчете растворимости следует учесть влияние ионной силы раствора. Равновесие в системе выражается уравнением:
PbCl2(тв.) Pb2+ + 2Cl–.
Из значения K0S проведем оценку растворимости по формуле (6.4):
|
m n KS0 |
|
|
|
|
|
|
|
|
|
S |
m |
n |
n |
3 1,6 10 5 |
4 |
1,6·10 |
–2 |
моль/л. |
||
m |
|
|
|
|||||||
|
|
|
|
|
|
|
|
|||
Ионную силу раствора вычисляем по формуле (2.1):
I = 0,5(1,6·10–2·22 + 2·1,6·10–2·12) = 0,048.
По табл. 1 приложения находим: Pb2+ = 0,47; Cl-= 0,86 и рас-
считываем растворимость хлорида свинца по формуле (6.8) с учетом ионной силы:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
= 3 1,6 10 5 |
|
|
|
S = m n KS0 |
1 22 |
Pb |
2 2 |
|
4 0,47 0,862 |
= 2,3 10–2 моль/л. |
|||
|
|
|
Cl |
|
|
|
|
|
|
Проведенные вычисления свидетельствуют о возрастании растворимости вследствие влияния ионной силы.
Пример 6.11. Сравните растворимость сульфата свинца в воде
срастворимостью в 0,10 М растворе нитрата калия.
Ре ш е н и е . K0S(PbSO4) = 1,6.10–8. Так как K0S 10–5, при расчете ионной силы можно учесть только вклад сильного индиффе-
рентного электролита KNO3. Вычисляем ионную силу раствора:
83

I = 0,5(0,1 12 + 0,1 12) = 0,1.
При этом Pb2+ = SO42–-= 0,43. Рассчитаем растворимость хлорида свинца в водном растворе нитрата калия по формуле (6.8):
S1 = S (в KNO3) = m n |
KS0 |
|
|
|
n = |
1,6 10 8 |
2,9 10 |
–4 |
моль/л. |
m |
n |
m |
2 |
|
|||||
|
m |
n |
Pb2 |
SO2 |
0,43 |
|
|
|
|
|
|
|
|
|
4 |
|
|
|
|
Растворимость PbSO4 без учета ионной силы (в воде без KNO3): S2 = S (в воде) = m n KS0 mm nn
KS0 mm nn 
 1,610 8 1,3 10–4 моль/л;
1,610 8 1,3 10–4 моль/л;
S1/S2 = 2,9 10–4/1,3 10–4 = 2,23.
Вследствие “солевого эффекта” растворимость повышается в 2,23 раза.
6.2.2. Влияние одноименного иона на растворимость осадка
Пример 6.12. Рассчитать (без учета и с учетом ионной силы раствора) растворимость CaCO3 в воде, в 1 литре которой растворе-
но 0,010 моль CaCl2.
Р е ш е н и е . K0S(CaCO3) = 3,8 10-9. CaCl2 – сильный электролит, образующий при диссоциации в растворе одноименный с осадком ион Ca2+, причем с(Ca2+) = с(CaCl2). Обозначим общие
концентрации ионов в насыщенном растворе CaCO3: |
|||
CaCO3(тв.) |
Ca2+ |
+ |
CO32–, |
[ ] = с: |
S + с(Ca2+) |
S(m = n = 1). |
|
Пренебрегая значением S в сумме (S + с(Ca2+)) и используя |
|||
формулы (6.2) и (6.7) при = 1, получаем выражения: |
|||
K0S = с(Ca2+) Са2+ S СO32– |
и S = [CО32–] = K0S/(с(Ca2+) Са2+ СO32–). |
||
Ионная сила раствора определяется, в основном, ионами |
|||
сильного электролита CaCl2 |
по формуле (2.1): |
|
|
I = 0,5(0,01 22 + 0,01 2 12) = 0,03; |
Са2+ = СO32– = 0,54. |
||
Тогда, с учетом ионной силы раствора,
S = [CО32–] = 3,8·10–9/0,01 0,542 = 1,3 10–6 моль/л.
Без учета ионной силы ( =1), но с учетом влияния одноименного иона растворимость составляет:
S = [CО32–] = 3,8·10–9/0,01= 3,8·10–7 моль/л.
Растворимость CaCO3 в воде при = 1 и = 1:
S = [Cа2+] = [CО32–] = 
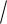 KS0 =
KS0 = 
 3,8 10-9 6,2 10 5 моль/л.
3,8 10-9 6,2 10 5 моль/л.
84

Проведенные расчеты свидетельствуют о существенном уменьшении растворимости в присутствии одноименного иона, причем это влияние более значительно, чем “солевой эффект”.
Пример 6.13. Рассчитать растворимость Fe(OH)3 в воде.
Р е ш е н и е . Особенностью решения данной задачи является необходимость учета ионов OH– из воды как одноименных ионов при вычислении растворимости гидроксидов, если произведение растворимости очень мало. K0S(Fe(OH)3) = 6,3·10–38. В этом случае принимаем концентрацию одноименного иона (аниона), [OH–] 1,0·10–7 моль/л. Растворимость вычисляем по выражению (6.6) с учетом стехиометрических коэффициентов реакции:
Fe(OH)3(тв.) |
Fe3+ |
+ 3OH–. |
[…] = с: |
S |
(3S+10–7) 10–7 |
(Учитывать ионную силу при низких концентрациях не требуется).
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
|
|
||
S = [Fe3+] |
1 |
m |
KS |
|
|
KS |
= K0 /[OH–]3 |
= 6,3 10–38/(10–7)3 = 6,3 10–17 моль/л. |
|
|
n |
3 |
|||||||
|
m сB |
|
|
сB |
S |
|
|||
|
|
|
|
|
|||||
Без учета “нейтральности” среды при низкой растворимости веществ растворимость Fe(OH)3 составила бы:
|
|
|
|
|
|
|
|
|
|
|
S = m n KS0 |
m |
m |
n |
n 1 3 6,3 10 38 |
3 = 2,2 10-10 |
моль/л, |
||||
|
|
|
|
|
|
1 3 |
|
|||
что в 3500000 раз выше.
6.2.3. Влияние конкурирующих реакций на растворимость
Ионы осадка могут вступать в реакции с компонентами раствора. Общая растворимость осадка в этих случаях складывается из всех форм, которые образует катион и анион. Наибольшее практи-
ческое значение имеет учет влияния комплексообразования катиона и протонирования аниона слабой кислоты, входящих в состав малорастворимого электролита.
Если рН при растворении создается и поддерживается буферным раствором, то предварительно следует вычислить [H+] соответственно конкретным условиям, а затем рассчитывать молярную долю свободных ионов и проводить расчет растворимости по выражению (6.3).
85
Однако для малорастворимых электролитов, способных растворяться в кислотах или основаниях определенной концентрации, расходующихся в ходе реакции растворения, расчет растворимости следует проводить по общей константе равновесия реакции растворения (примеры 6.16 – 6.17; см. также главы 2 и 5, примеры
5.15 – 5.17).
При растворении осадков в воде в ряде случаев следует рассматривать в качестве конкурирующих реакции гидролиза, которые для катиона могут сопровождаться образованием гидроксокомплексов, а для аниона слабой кислоты - протонированием. В этом случае в практических расчетах принимают следующее основное допущение: при низкой растворимости соли (низкой концентрации гидролизующихся частиц) среда раствора определяется диссоциацией воды и близка к нейтральной, т.е. [H+] ≈ [OH–] ≈ 10–7 моль/л
(пример 6.18).
Обычно при наличии конкурирующих реакций не учитывают влияние ионной силы (глава 2, раздел 2.2).
Пример 6.14. Рассчитать растворимость AgI в 1,0 М растворе аммиака.
Р е ш е н и е . В насыщенном растворе AgI в присутствии NH3, наряду с основной реакцией:
AgI(тв.) Ag++ I– |
(K0S |
|
= 8,3 10–17) |
|
|||||||||
протекают конкурирующие реакции (lg 1 = 3,32; lg 2 = 7,23): |
|
|
|
|
|
||||||||
Ag++NH3 [Ag(NH3)]+ |
, |
|
|
|
|
[Ag(NH3 ) ] |
|
; |
|||||
1 |
[Ag ][NH |
3 |
] |
||||||||||
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||
[Ag(NH3)]+ + NH3 [Ag(NH3)2]+, |
|
|
|
|
[Ag(NH3 )2 ] |
|
|
||||||
2 |
|
|
|
]2 . |
|||||||||
|
|
|
[Ag ][NH |
||||||||||
|
|
|
|
|
|
3 |
|
|
|
|
|
||
Растворимость AgI определяется общей концентрацией ионов серебра в
растворе:
S = c(Ag+) = [Ag+] + [Ag(NH3)+] + [Ag(NH3)2+].
По формуле (2.8) (см. пример 2.6) вычисляем молярную долю ионов Ag+:
Ag+ = |
1 |
= |
|
1 |
= 6,17·10–8. |
|
1 2,09 103 1 1,62 107 12 |
||||
1 1 NH3 2 NH3 2 |
|||||
Пренебрегая ионной силой, по формуле (6.3) ( I– = 1) вычисляем S (AgI):
86

|
|
|
|
|
|
|
|
|
8,3 |
|
17 |
|
|
|
|
|
0 |
|
|
0 |
|
|
|
10 |
|
-5 |
|
||
S = |
m n |
KS |
mm nn mA |
|
KS |
Ag |
|
|
3,7·10 |
моль/л. |
||||
6,17 |
10 8 |
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||
Проведенные расчеты показывают, что связывание катиона в растворе в комплекс приводит к повышению растворимости малорастворимого электролита.
Пример 6.15. Рассчитать растворимость CaCO3 при pH 5,0.
Р е ш е н и е . В данном примере pH задано в явном виде, причем подразумевается поддерживание рН буферным раствором.
В растворе CaCO3 (K0S = 3,8 10–9) наряду с основной реакцией |
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
CaCO3(тв.) Ca2+ + CO32– |
2– |
|
|||||||||||
протекают побочные реакции связывания ионов CO |
ионами водо- |
|||||||||||||||||||||
рода в HCO – |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
2– находим по |
||||
и H CO (разд. 2.2). Молярную долю CO |
||||||||||||||||||||||
|
|
3 |
|
|
|
2 |
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
3 |
|
выражению (2.5): |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
4,5 10 7 4,8 10 11 |
|
|
|
= 2,07 10-9. |
|||||||
2 |
(1 10 |
5 |
) |
2 |
1 |
10 |
5 |
4,5 10 |
7 |
4,5 10 |
7 |
4,8 10 |
11 |
|||||||||
|
CO3 |
|
|
|
|
|
|
|
|
|
||||||||||||
Растворимость вычисляем по формуле (6.3) при Ca2+ = 1: |
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3,8 10 |
9 |
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
K S |
|
|
|
|
|
|
|
|
|
|
1,35 моль/л. |
|
|
||||
|
|
S = |
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
2 |
|
|
|
2,07 10 9 |
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
CO3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
Протонирование аниона слабой кислоты повышает растворимость подобных малорастворимых электролитов.
Пример 6.16. Вычислите массу CaCO3, способного раствориться в 50 мл 2,0 М уксусной кислоты.
Р е ш е н и е . В данном примере pH в ходе растворения не задано в явном виде и не поддерживается постоянным из-за расхода
СН3СООН:
CaCO3(тв.) + 2СН3СООН Ca2+ + 2СН3СОО– + Н2CO3. [...]: 2 - 2S S 2S S
Общая константа равновесия реакции (см. раздел 2.3, пример 2.7(б)):
К = KS0Ka2 /Ka2Ka1 = 3,8 10–9 (1,74 10–5)2/4,5 10–7 4,8 10–11 = 5,33 10–2..
Подставляем в выражение константы реакции равновесные концентрации и находим растворимость S, решая квадратное уравнение:
K |
[Ca2 ][CH3COO ]2[H2CO3 ] |
|
|
4S 4 |
5,33 10 2 ; |
||
[CH |
COOH] 2 |
(2 2S)2 |
|||||
|
|
|
|||||
|
3 |
|
|
|
|
|
|
|
|
87 |
|
|
|
|
|

S2 + 0,231S - 0,231 = 0;
S = 0,231 |
|
|
|
|
|
|
0,053 0,924 |
|
0,757 |
0,38 |
моль/л; |
||
2 |
2 |
|||||
|
|
|
|
m(CaCO3) = S V M = 0,38 0,05 100 = 1,9 г.
Подобным образом рассчитывается растворимость малорастворимых гидроксидов в кислотах. Обратной задачей является нахождение концентрации кислоты в растворе для растворения определенного количества осадка (пример 6.17).
Пример 6.17. Какую концентрацию муравьиной кислоты следует создать в растворе, чтобы в 100 мл растворилось 0,2137 г
Fe(OH)3?
Р е ш е н и е . Растворение Fe(OH)3 |
в муравьиной кислоте при- |
||
водит к образованию ионов Fe3+ в растворе. По их концентрации |
|||
можно судить о растворимости Fe(OH)3 в указанных условиях: |
|||
|
с(Fe3+) = [Fe3+] = S(Fe(OH) ) = m/(V M(Fe(OH) ); |
||
|
|
3 |
3 |
|
S = 0,2137/(0,1 106,85) = 2,00 10–2 моль/л. |
||
Fe(OH)3(тв.) + 3НСООН Fe3+ |
+ 3НСОО– + 3Н2O, |
||
[...]: |
3х-3S |
S |
3S |
[...]: |
3х-3 0,02 |
0,02 |
3 0,02. |
Вычисляем общую константу равновесия для реакции растворения К (раздел 2.3), подставляем в неё выражения равновесных
концентраций |
и решаем |
полученное уравнение |
относительно |
|||||
с(НСООН), обозначая ее через 3х: |
|
|
|
|
||||
|
К = KS0 Ka3/KW3 = 6,3 10–38 (1,8 10–4)3/(10–14)3 = 3,67 10–7; |
|||||||
К = |
0,02 (0,06)3 |
3,67 10–7; |
|
(0,06)3 |
18,4 10–6; |
0,06 |
|
2,64 10–2; |
(3х 0,06)3 |
(3х 0,06)3 |
|
|
|||||
|
|
|
3х 0,06 |
|||||
|
7,92 10–2 |
х = 0,158 10–2 |
+ 6,00 10–2 = 6,16 10–2; х = 0,78; |
|||||
с(НСООН) = 3х = 2,34 моль/л.
Пример 6.18.* Вычислить растворимость сульфида ртути(1) в воде с учетом гидролиза.
Р е ш е н и е . Основная реакция при растворении:
Hg2S(тв.) Hg22+ + S2– (K0S (Hg2S) = 1·10-47).
В общем случае, в побочных реакциях гидролиза могут участвовать и катион, и анион. Однако сравнение констант гидролиза по первой ступени показывает, что гидролизом ионов Hg22+ можно
88

пренебречь и учитывать только протонирование аниона ионами водорода из воды:
Hg22+ + H2О Hg2(ОН)+ + Н+, Кгидр.1= КW· 1(Hg2(ОН)+) = 10-14 109= 10-5;
S2– + H2О HS– + ОН–, Кгидр.2= КW/Ка2(Н2S) = 10-14/2,5 10-13 = 4 10-2;
Кгидр.1 Кгидр.2
Допускаем, что pH ≈ 7 создается только диссоциацией воды, поскольку низкая концентрация подвергающихся гидролизу ионов S2–
мало повлияет на среду раствора. Найдем долю свободных ионов
S2– с учетом формулы (2.5) (для H2S Kа1 = 1·10–7 , Kа2 = 2,5·10–13).
S 2 |
|
|
|
|
|
|
|
|
1 10 7 |
2,5 10 13 |
|
|
|
|
= 1,3·10-6; |
||||||
(1 |
10 |
7 |
) |
2 |
1 |
10 |
7 |
1 |
10 |
7 |
1 10 |
7 |
2,5 10 |
13 |
|||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
KS0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
S = 2 1 |
|
|
|
|
|
|
3 1 10 47 |
|
|
|
|
1,2·10-14 |
моль/л. |
||||||||
|
|
22 1 |
S |
2 |
|
|
|
|
22 1 1,3 10 6 |
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Без учета гидролиза растворимость Hg2S была бы ниже:
S 3 1 10 47 22 1 1,4 10 16 моль/л.
1 10 47 22 1 1,4 10 16 моль/л.
Следовательно, в результате гидролиза ионов осадка повышается его растворимость.
6.2.4.Вклад молекулярной растворимости
вобщую растворимость
Если при растворении осадка общий процесс является суммой равновесий 2 и 3:
AmBn (тв) 2 AmBn (р-р) 3 mA + nB,
то общая растворимость малорастворимого электролита AmBn складывается из ионной и молекулярной растворимостей.
Молекулярная растворимость S0 – это составляющая растворимости, обусловленная наличием в растворе недиссоциированных (нейтральных) молекул. Константа K0 равновесия (2) может быть легко вычислена из произведения растворимости AmBn, табличных констант устойчивости комплексов и констант ионизации кислот (в соответствии с природой AmBn в растворе). В общем виде для равновесия (2):
K0 = [AmBn (р-р)] = S0. |
(6.9) |
Например, для малорастворимого комплексного соединения AB при ионной силе, близкой к нулю, справедливо:
89
