
Основы иммунологии
.pdf
роста ). Синтез этих цитокинов и продукта гена Foxр4+ – белка скурфина ассоциирован с супрессией иммунного ответа.
Т-цитотоксическими называют те Т-лимфоциты (18-22% в крови), которые несут антиген СD8 и рецептор к IgG (Fc ). Макромолекула CD8 служит рецептором для антигенов главного комплекса гистосовместимости I класса (МНС-I). После активации антигеном Т-супрессоры/цитотоксические клетки – Т-киллеры связываются с ним на поверхности клеток и, выделяя цитотоксин (белок перфорин), разрушают их. При этом Т-киллер остается жизнеспособным и может разрушать следующую клетку.
Т-клеточный рецептор
На поверхности Т-лимфоцитов имеется около 3х104 прочно связанных с мембранами Т-клеточных рецепторов (ТКР) к антигену, чем-то напоминающих антитела. Т-клеточный рецептор является гетеродимером и состоит из альфа- и бета- (молекулярная масса 40-50 кDа) и, реже, из / -цепей (1-5%-клеток в крови).
У Тх и Тц ТКР одинаковы по строению. Однако Т-хелперы взаимодействуют с антигеном, ассоциированным с HLA-молекулами II класса, а Т-цитотоксические распознают антиген в комплексе с HLA-молекулами I класса. Причем белковый антиген должен быть переварен антигенпредставляющими клетками и представлен в виде пептида длиной 8-11 аминокислот для Т-цитотоксических и 12-25 для Т-хелперов. Такое различие в связывании Тх и Тс пептидов обусловлено участием во взаимодействии молекул – CD4 у Тх и CD8 у Тц.
41
ГЛАВА 2. АНТИГЕНЫ. ДИНАМИКА ИММУННОГО ОТВЕТА
Антигены
Антигены (АГ) – это любые простые или сложные вещества, которые при попадании внутрь организма тем или иным путем, вызывают иммунную реакцию, и способны специфично взаимодействовать с продуктами этой реакции: антителами и иммунными Т-клетками.
Иммунизация – введение антигенов в организм с целью создания искусственного активного иммунитета или для получения препаратов антител.
Различают:
-ксеногенные (гетерологичные) антигены – межвидовые антигены, например – биомолекулы животных при их введении человеку, наиболее сильные антигены;
-аллогенные антигены или изоантигены, внутривидовые, отличающие людей (и животных) друг от друга;
-аутоантигены – собственные молекулы организма, на которые из-за нарушения аутотолерантности развивается иммунная реакция.
Основными свойствами антигенов являются иммуногенность и специфичность. Под иммуногенностью понимают способность антигена индуцировать в организме иммунную реакцию. Специфичность определяется взаимодействием антигена только с комплементарными ему антителами или рецепторами Т-лимфоцитов определенного клона.
Полноценными антигенами являются природные или синтетические биополимеры, чаще всего белки и полисахариды, а также комплексные соединения (гликопротеиды, липопротеиды, нуклеопротеиды).
Гаптены – низкомолекулярные вещества, которые в обычных условиях не вызывают иммунную реакцию. Однако при связывании с высокомолекулярными молекулами-«носителями» они приобретают
42
иммуногенность. К гаптенам относятся лекарственные препараты и большинство химических веществ. Они способны запускать иммунный ответ после связывания с белками организма, например с альбумином, а также с белками на поверхности клеток (эритроцитов, лейкоцитов).
Суперантигены – особая группа антигенов, которые в дозах значительно меньших, чем митогены, вызывают неспецифическую поликлональную активацию и пролиферацию большого числа Т- лимфоцитов (до 20%, обычные антигены – 0,01%). Эти антигены так же, как и обычные, распознаются Т-хелперами в ассоциации с антигенами гистосовместимости II класса или Т-супрессорами с молекулами I класса. Однако они высокотропны к -цепям некоторых типов Т-клеточных рецепторов и стимулируют все Т-клетки, несущие их, независимо от антигенной специфичности. При этом в большом количестве вырабатываются провоспалительные цитокины,
вызывающих воспаление и повреждение тканей. Суперантигенами являются бактериальные энтеротоксины, стафилококковые, холерные токсины и другие бактериальные антигены, некоторые вирусы (ротавирусы). После активации наступает апоптоз – гибель Т- лимфоцитов и возникает их дефицит.
В-клеточные суперантигены связываются с Fab-фрагментами различных иммуноглобулинов (VL и VH цепями), могут активировать В-лимфоциты. Белок А стафилококков наряду со взаимодействием с Fc-фрагментами IgG, связывается с 15-50% IgM, IgA, IgG и IgE через Fab фрагмент. Белок L пептострептококка связывается с VL порцией иммуноглобулинов.
Инфекционные антигены
Инфекционные антигены – это антигены бактерий, вирусов, грибов, простейших. Все они могут служить аллергенами, так как вызывают аллергические реакции.
В зависимости от локализации в бактериальной клетке различают К-, Н- и О-антигены (обозначают буквами латинского алфавита).
К-АГ (М.М. около 100кД) – это гетерогенная группа наиболее поверхностных, капсульных АГ бактерий. Характеризуют групповую и типовую принадлежность бактерий.
43
О-АГ – полисахарид, входит в состав клеточной стенки бактерий, являясь частью липополисахарида (ЛПС). Он особенно выражен у грамотрицательных бактерий. О-АГ определяет антигенную специфичность ЛПС и по нему различают много серовариантов бактерий одного вида.
В целом ЛПС является эндотоксином. Уже в небольших дозах вызывает лихорадку из-за активации макрофагов через CD14 и TLR-4 с выделением ИЛ-1, ИЛ-12, ФНО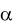 и других цитокинов, поликлональную тимуснезависимую активацию В-лимфоцитов и синтез антител, дегрануляцию гранулоцитов, агрегацию тромбоцитов. Он может связываться с любыми клетками организма, но особенно с макрофагами. В больших дозах угнетает фагоцитоз, вызывает токсикоз, нарушение функции сердечно-сосудистой системы, тромбозы, эндотоксический шок. ЛПС некоторых бактерий входит в состав иммуностимуляторов (продигиозан, пирогенал).
и других цитокинов, поликлональную тимуснезависимую активацию В-лимфоцитов и синтез антител, дегрануляцию гранулоцитов, агрегацию тромбоцитов. Он может связываться с любыми клетками организма, но особенно с макрофагами. В больших дозах угнетает фагоцитоз, вызывает токсикоз, нарушение функции сердечно-сосудистой системы, тромбозы, эндотоксический шок. ЛПС некоторых бактерий входит в состав иммуностимуляторов (продигиозан, пирогенал).
Пептидогликаны клеточной стенки бактерий, особенно полученные из них фракции мурамилпептидов обладают сильным адъювантным эффектом на клетки СИ, неспецифически усиливая ответ на различные антигены.
Н-АГ входит в состав бактериальных жгутиков, основа его – белок флагеллин, термолабилен.
Антигены вирусов. У большинства вирусов имеются суперкапсидные – поверхностные оболочечные, белковые и гликопротеидные АГ (например, гемагглютинин и нейраминидаза вируса гриппа), капсидные – оболочечные и нуклеопротеидные (сердцевинные) АГ. Определение вирусных антигенов в крови и других биологических жидкостях широко используется для диагностики вирусных инфекций. Наиболее иммуногенные, протективные пептиды вирусов используются для создания синтетических вакцин. По строению они вариабельны даже у одного вида вирусов.
К неинфекционным антигенам относятся АГ растений,
лекарственные препараты, химические, природные и синтетические вещества, антигены клеток животных и человека.
Аллогенные антигены. HLA-система
Молекулы-антигены, отличающие одного индивидуума от другого, называют аллоантигенами или изоантигенами. К
44

аллоантигенам относятся АГ эритроцитов, лейкоцитов, тромбоцитов и аллоантигенные варианты иммуноглобулинов Inv и Gm.
Антигены эритроцитов. По наличию А и В антигенов и соответствующих им естественных антител ( – альфа и 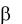 – бета) различают 4 группы крови у человека: 0(I) – нет антигенов, есть и антитела, А(II) – присутствует только А антиген и -антитела,
– бета) различают 4 группы крови у человека: 0(I) – нет антигенов, есть и антитела, А(II) – присутствует только А антиген и -антитела,
В(III) – есть В-АГ и -антитела, АВ(IV) – есть оба АГ, нет антител. Система Rhesus. У 85% людей на эритроцитах есть резус-АГ
(Rh+), обнаруженный впервые у обезьян вида макака-резус.
Аллогенные антигены лейкоцитов. HLA-система антигенраспознающих молекул.
В сыворотке крови больных, которым многократно переливали кровь доноров, а также у многорожавших женщин были обнаружены антитела агглютинирующие и лизирующие лейкоциты доноров. При переливании таким лицам цельной крови или лейкоцитарной массы у них могут быть аллергические трансфузионные реакции.
На лимфоцитах выявлена целая система молекул лейкоцитарных АГ – HLA (Human Leucocyte Antigens), которая контролируется генами главного комплекса гистосовместимости
(ГКГ или МНС – Major hystocompability complex). Комплекс включает около 4х106 пар нуклеотидов и состоит из множества тесно сцепленных генетических структурных единиц – локусов, представленных разными генами. Каждый из них может существовать в нескольких вариантах, называемых аллелями. Этот комплекс генов находится у человека в 6 хромосоме.
Продукты этих HLA-генов – HLA-молекулы (антигены) – это белки клеточных мембран. Их набор у каждого человека индивидуален и только у однояйцевых близнецов он одинаков.
Основные функции HLA-молекул (антигенов):
-участвуют в распознавании экзогенных антигенов;
-межклеточных взаимодействиях и развитии иммунного ответа;
-определяют предрасположенность к заболеваниям;
-являются маркерами «своего» – собственных неизмененных клеток;
45
- вызывают реакцию отторжения антиген-несовместимых трансплантатов тканей донора и только тогда они и являются антигенами.
Гены главного комплекса гистосовместимости или у человека – гены HLA системы и соответствующие им HLA-молекулы определяют силу и специфичность иммунного ответа. По существу обычное название – «HLA-антигены» неточно, так как эти молекулы служат антигенами, лишь поступая в другой организм (пересадка тканей, переливание лейкоцитов). Аутологичные HLA-молекулы неантигенны для самого организма и, более того, служат рецепторами для первичного распознавания процессированных антигенов, и в этом их важнейшая физиологическая роль.
Основное значение в иммунорегуляции имеют гены I и II классов гистосовместимости. Локусы генов I класса локализуются в периферическом плече 6 хромосомы, II класса – ближе к центромере.
HLA-АГ I класса имеются на всех ядросодержащих клетках: лимфоцитах, в меньшей степени – на клетках печени, легких, почек, очень редко на клетках мозга и скелетных мышц. Антигены I класса контролируются генными локусами: HLA-A, HLA-B, HLA-C и другими. Они взаимодействуют с антигенными пептидами вирусов, опухолевыми и другими АГ внутри цитоплазмы пораженных клеток. Далее комплекс HLA-АГ – антигенный пептид представляется на клеточной мембране СВ8+ Т-цитотоксическим лимфоцитам
(киллерам), которые разрушают измененные клетки.
HLA-AГ II класса (HLA-DR, HLA-DP, HLA-DQ и др.)
экспрессированы на В-лимфоцитах, ДК, макрофагах, активированных Т-лимфоцитах, а также появляются на эндотелиальных и эпителиальных клетках после стимуляции их -интерфероном. Они участвуют в распознавании чужеродных антигенов – пептидов размером до 30 остатков аминокислот. Их основная функция – процессинг (ферментативная переработка) и презентация экзоантигенов CD4+ хелперным клеткам для их последующей активации. Активация Т-хелперов обеспечивает развитие эффективного клеточного и гуморального иммунного ответа на представленный АГ.
46
Молекулы CD1, представляющие липидные антигены
CD1 антигены – это особая группа антигенпредставляющих молекул. Они находятся на поверхности всех АПК, а также на мембранах тимоцитов, Т лимфоцитов. Основная функция CD1
молекул – связывание и представление липидных антигенов. По структуре CD1 антигены сходны с НЛА антигенами 1 класса главного комплекса гистосовместимости. Однако в отличие от HLA 1 класса CD1 молекула имеет антигенсвязывающий участок, отличающийся выраженной гидрофобностью. Это обеспечивает ее прочное специфическое связывание с липидными антигенами.
Генетический локус, кодирующий CD1 антигены, находится в 1 хромосоме. Он включает не менее 5 различных генов (CD1a-e). Фенотипически семейство CD1 антигенов делится на 2 основные группы. Группа 1 включает CD1a, b, с варианты, в группу 2 входят CD1d молекулы. CD1 АГ 1 группы связывают многие микробные антигены липидной природы, например, АГ микобактерий. CD1d АГ 2 группы могут представлять как экзогенные (например, АГ простейших), так и аутоантигены.
Молекулы CD1 представляют антигены различным субпопуляциям Т-лимфоцитов, включая их особую популяцию – NKT-клетки, несущие одновременно маркеры как Т-лимфоцитов, так и NK-клеток (естественных киллеров). Эти лимфоциты также проявляют выраженную цитотоксическую активность.
Динамика иммунного ответа
В условиях реального иммунного ответа при попадании сложного комплексного антигена (например, бактериальной клетки или вируса) в организм иммунные реакции развертываются по
неспецифическим и специфическим механизмам.
Неспецифические механизмы иммунного ответа
Первоначально на антиген реагируют неспецифические гуморальные и клеточные факторы иммунной защиты. Более чем в
47
90% случаев этого бывает достаточно, чтобы предупредить развитие заболевания.
Главную роль в этих процессах играют мононуклеарная система фагоцитов, система гранулоцитов, ЕК-клетки, система комплемента, белки острой фазы воспаления (например, С-реактивный белок), естественные антитела.
После внедрения микробной клетки в макроорганизм одновременно развиваются несколько процессов.
Происходит активация комплемента по альтернативному пути через С3-компонент. В результате образуется мембраноатакующий комплекс С5b-С9, который лизирует микробную клетку. Образуется много антигенных фрагментов. В результате активации комплемента также образуются другие биологически активные компоненты комплемента С3b, а также С3а и С5а – анафилотоксины.
Эти компоненты усиливают иммунный ответ разными путями. С3b связывается с поверхностью микробной клетки. Далее этот
комплекс связывается с мембраной макрофага через рецептор для комплемента CD35. Тем самым он выступает в роли опсонина, вызывая накопление макрофагов в очаге воспаления и стимулируя их адгезию к клетками-мишеням.
Анафилотоксины, особенно С5а, являются наиболее мощными хемоаттрактантами. Они привлекают нейтрофилы и макрофаги, вызывая их оседание в очаге воспаления.
Белки острой фазы воспаления (С-реактивный белок,
фибронектин и др) связываются с микробной клеткой, препятствуя процессам микробной инвазии. Кроме того, С-реактивный белок активирует комплемент через С1 компонент по лектиновому пути с последующим образованием МАК и лизисом микробной клетки.
Естественные антитела обычно обладают низкой аффинностью к АГ и полиреактивностью. Обычно они продуцируются особой субпопуляцией СD5+ В-лимфоцитов. Вследствие разности в зарядах такие АТ связываются с АГ микробной клетки и могут активировать комплемент по классическому пути. Кроме того, они связываются с СД16 на поверхности нейтрофилов и макрофагов и вызывают адгезию фагоцитов и клеток-мишеней, выступая в роли опсонинов
(иммунный фагоцитоз).
Также естественные АТ могут обладать собственной каталитической (абзимной) активностью, что приводит к гидролизу поступившего антигена.
48
Однако наибольшее значение в динамике иммунного ответа на первых этапах имеют неспецифические клеточные реакции.
Основную роль здесь играет фагоцитоз микробных клеток нейтрофилами и макрофагами. Под действием хемокинов (анафилотоксинов, ИЛ-8) они мигрируют и оседают в очаге воспаления. Сильным стимулятором хемотаксиса фагоцитов являются также компоненты клеточной стенки микроба Далее происходит адгезия фагоцитов на клетках-мишенях. Она обеспечивается взаимодействием лектиновых рецепторов макрофага с полисахаридами клеточной стенки микроба, в результате процессов опсонизации микробов антителами и компонентами комплемента, а также через систему Toll-like рецепторов. Последнее взаимодействие играет особую роль, так как в зависимости от своей природы, АГ активирует определенный вид TLR. Это перенаправляет иммунный ответ либо по клеточному, либо по гуморальному пути.
Фагоциты поглощают АГ, далее активируется дыхательный
взрыв и происходит переваривание микробных клеток. |
|
||
Одновременно |
макрофаги |
выделяют |
комплекс |
провоспалительных цитокинов (ИЛ-1, ФНО, гамма-интерферон), которые активируют преимущественно Тх1 с развитием воспаления.
Этот процесс может существенно усиливаться вследствие связывания ЛПС бактерий с CD14 рецептором макрофага и TLR-4. При этом массивный выброс провоспалительных цитокинов вызывает лихорадку и может приводить к эндотоксическому шоку.
Важным компонентом неспецифического ответа является действие ЕК-клеток. Установлено, что они могут атаковать большинство клеток-мишеней независимо от их происхождения. Однако в организме на мембранах ядросодержащих клеток имеются HLA АГ I класса. При взаимодействии с ними ЕК получают сигнал, который в норме подавляет их активацию. При изменении экспрессии HLA АГ I класса в результате поражения клетки вирусом или ее опухолевой трансформации происходит активация ЕК, выделение перфорина и лизис измененной клетки-мишени. Кроме того, ЕК активируются, взаимодействуя своими Fc-рецепторами с антителами, адсорбированными на мембранных АГ чужеродных клеток
(антителозависимая клеточная цитотоксичность).
49
Специфический иммунный ответ на антигены
Одновременно с действием неспецифических систем иммунитета активируются специфические факторы иммунной защиты – Т-клетки, несущие Т-клеточные рецепторы к антигену (ТКР) и
антителообразующие клетки (плазмоциты).
Специфический иммунный ответ на Т-зависимые и Т- независимые АГ протекает по-разному.
Т-независимые АГ обычно являются высокомолекулярными чужеродными структурами, имеющими выраженный заряд (например, полисахариды бактерий). Такие антигены способны связать перекрестно не менее двух молекул специфических поверхностных IgМ или IgD на поверхности В-лимфоцита. Это является необходимым условием последующей дифференцировки и пролиферации В-клеток, их бластной трансформации и превращения в плазмоциты.
Так как в этом процессе не участвуют Т-клетки-хелперы и отсутствует продукция ИЛ-4, то не происходит изотипического переключения синтеза АТ с класса IgМ на IgG или IgА. Даже при повторном попадании тимуснезависимого АГ к нему по-прежнему будут вырабатываться АТ класса IgМ.
Однако АТ класса IgМ высокоэффективно активируют комплемент по классическому пути, а также могут проявлять абзимную каталитическую активность.
Тем не менее, наиболее эффективным и многостадийным является иммунный ответ на Т-зависимые АГ.
Специфический иммунный ответ на Т-зависимые АГ
Т-зависимый иммунный ответ требует процессинга и представления (презентации) АГ.
При попадании антигенов в кожу или на слизистые оболочки они захватываются АПК. Наиболее активными АПК являются
дендритные клетки (ДК), в частности – клетки Лангерганса, а также макрофаги. Клетки Лангерганса из кожи и слизистых мигрируют в регионарные лимфоузлы и превращаются в интердигитирующие дендритные клетки. Тем самым они осуществляют направленный транспорт АГ к Т-лимфоцитам, основная часть которых локализована в лимфоузлах.
50
