
В.В. Назаревич Параметры и функции состояния рабочего тела. Приборы для измерения параметров состояния
.pdf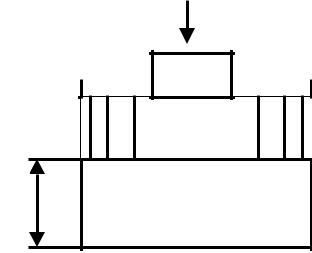
20
го объёма. Таким образом U , отражая состояние рабочего тела, является однозначной и непрерывной функцией параметров состояния тела
∆ U = U2 – U1 = f2(P2υ2T2) – f1(P1υ1T1).
На практике чаще пользуются формулой
∆U =Cy∆t ,
где Cy – удельная, средняя изохорная теплоёмкость рабочего тела.
Втермодинамике обычно находят лишь изменение внутренней энергии в заданном процессе, которое целиком определяется начальным и конечным состоянием рабочего тела и совершенно не зависит от его промежуточных состояний.
ВСИ изменение внутренней энергии ∆U измеряют в джоулях (Дж), а удельная внутренняя энергия ∆U , отнесённая к 1 кг рабочего тела, – в Дж/кг.
4.3. Энтальпия i – это тепловая функция состояния, введённая |
|||
для облегчения термодинамических расчетов измеряется, в Дж/кг. |
|||
Физический смысл энтальпии состоит в том, что i представляет |
|||
собой энергию расширенной системы – рабочего тела и окружающей |
|||
среды. Представить это можно следующим образом. Пусть в цилиндре |
|||
под поршнем находится рабочее тело – газ с параметрами U , |
P , T и V |
||
(рис.20). На поршень давит груз массой M . В равновесном энергетиче- |
|||
|
ском |
состоянии |
рабочее |
|
тело и груз будут нахо- |
||
М |
диться при равенстве энер- |
||
гий: |
потенциальной энер- |
||
|
гии груза Mgh и внутрен- |
||
|
|
ней энергии газа U . Общая |
|||
h |
|
энергия |
всей |
рассматри- |
|
P,V,T |
ваемой |
системы (рабочее |
|||
|
тело, груз, поршень и ци- |
||||
|
|
линдр) будет равна сумме: |
|||
|
|
Ecuc =U + Mgh . |
|||
|
Рис. 20 .Расширенная термодинамическая |
Выразив |
Mgh |
через |
|
|
система: |
параметры состояния газа, |
|||
|
рабочий газ – влажная среда |
как Mgh = PV , и учитывая, |
|||
что согласно определению общая энергия системы Ecuc это и есть эн- |
|||||
тальпия, можно записать i =U + PV . |
|
|
|
|
|

21
При любом бесконечно малом изменении состояния системы изменение энтальпии равно
di = dg +VdP ,
где dg – это количество тепла, полученное системой; VdP – работа
внешних сил над системой.
Из выражения видно, что в изобарном процессе при P = const и VdP =0 кол-во тепла, участвующего в процессе, равно разности эталь-
пий в конце и в начале процесса:
∆g p =i2 −i1. ∆i =C p∆t ,
где C p – удельная средняя изобарная теплоёмкость рабочего тела.
Последнее положение весьма удобно при проведении термодинамических анализов. На практике обычно требуется знать только изменение энтальпий в процессе, которое полностью определяется начальным и конечным состоянием рабочего тела и не зависит от промежуточных состояний.
4.4.Энтропия – это отношение теплоты, участвующей в процессе,
кабсолютной температуре рабочего тела.
Теплота q 1 кг любой термодинамической системы с температу-
рой рабочего тела T , с энергетической точкой зрения возможности получения полезной работы, состоит из двух частей: превратимой, которая при данной температуре окружающей среды способна перейти в
работу l, и непревратимой, равной q TT0 , которая остаётся в системе, q =l +q TT0 .
Непревратимая часть тепла системы q TT0 , равная произведению тепла на отношение абсолютных температур тел, участвующих в про-
цессе, содержит отношение, называемое энтропией: S = Tq .
Можно рассматривать энтропию как тепло, уходящее в окружающую среду в процессе преобразования тепла в работу. В адиабатной системе dS =0 .
Чем ниже температура T рабочего тела, тем больше энтропия и тем меньшая часть тепла системы может быть превращена в работу. Поскольку в реальных необратимых процессах в результате теплообме-
22
на температура рабочего тела падает, энтропия растёт, следовательно, энтропия системы является показателем необратимости процесса и снижения её работоспособности. В современной науке известны процессы, протекающие с уменьшением энтропии. Изменение энтропии в процессе можно определить через начальные и конечные параметры тела:
∆S = S − S = C ln |
T2 |
+ Rln |
V2 |
= C |
p |
ln |
T2 |
− Rln |
P2 |
, |
||||||
T |
V |
T |
P |
|||||||||||||
ν |
|
|
|
|
|
|
|
|
||||||||
и через теплоту процесса |
1 |
|
|
|
|
1 |
|
|
1 |
1 |
|
|||||
dq |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
dS = |
; S |
2 |
− S |
1 |
= ∫2 dq / T . |
|
|
|
||||||||
|
|
|
|
|||||||||||||
|
T |
|
|
|
1 |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
Кроме изложенного, энтропию можно рассматривать как среднюю, изохорную массовую теплоёмкость в интервале температур от абсолютного нуля до данной.
Поскольку рост энтропии указывает на наличие потерь полезной работы, следовательно, энтропийный метод анализа позволяет оценить достоинства, выявить недостатки тепловой машины по преобразованию тепла в работу и наметить пути совершенствования процессов преобразования.
4.5 Эксергия e – это максимальная работа, которую может совершить рабочее тело в данных условиях, пока его параметры не выровняются с параметрами окружающей среды. Это превратимая в работу часть общего тепла системы, участвующего в процессе:
e =lmax = q −T0( S1 −S0 ) =( i1 −i0 ) −T0( S1 −S0 ),
где i0 , S0 – энтальпия и энтропия рабочего тела в состоянии равновесия с окружающей средой; T0 – абсолютная температура окружающей среды; i1, S1 – энтропия и энтальпия рабочего тела на момент начала процесса; q – тепло системы.
Выражение T0( S1 −S0 ) характеризует потери полезной работы в
результате необратимости процесса. Это та часть из общего количества тепла, участвующего в процессе, которая в данных условиях не может превратиться в работу. Оставаясь в системе, это тепло при соответствующих условиях может быть преобразовано в работу. Иногда эти потери полезной работы называют анергией. Из определения эксергии видно, что если энтропия системы увеличивается, то её максимальная полезная работа уменьшается.
23
Эксергия как функция состояния весьма удобна для определения термодинамического совершенства любого теплового аппарата или его отдельных частей. Термодинамический анализ даёт более правильное представление об эффективности работы исследуемой тепловой машины.
5.ФУНКЦИИ ПРОЦЕССА
5.1.Характер протекания термодинамических процессов определяется функциями процесса, к которым относятся работа и теплота.
Функции процесса зависят не только от начального и конечного состояния вещества, но и от промежуточных значений параметров состояния в течение рассматриваемого процесса.
Теплота и работа представляют собой две единственно возможные передачи энергии от одного тела к другому.
5.2.Теплота – это конечный результат внутреннего или внешнего микропроцессов теплообменов. Теплота появляется лишь тогда, когда при наличии разности температур начинается процесс перехода внутренней энергии беспорядочного движения микрочастиц от одного тела
кдругому.
Количество теплоты, полученное (отданное) телом, можно определить калориметрическим путём или как произведение теплоёмкости C и массы вещества M на разность температур:
∆Q =CM∆T .
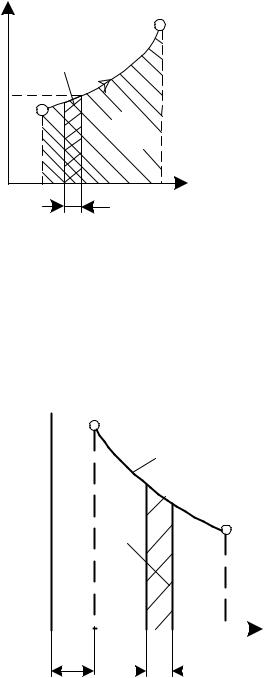
Понятие энтропии позволяет ввести чрезвычайно удобную для термодинамических расчётов T −S -диаграмму, на которой (как и на P −V -диаграмме)состояние термодинамический системы изображается точкой, а равновесный термодинамический процесс линией (рис.21).
Очевидно, что в T −S -диаграмме элементарная теплота процессы δq изображается элементарной площадкой с высотой T и основанием
dS , а площадь, ограниченная линией процесса, крайними ординатами и осью абсцисс, эквивалентна теплоте процесса.
|
24 |
|
T |
|
2 δq =TdS; |
δq |
|
|
|
S |
|
T 1 |
|
|
q |
q = ∫2 TdS. |
|
|
|
S1 |
S1 |
dS |
S2 |
|
|
|
Рис. 21. Графическое изображение |
||
теплоты в Т,S-координатах |
||
5.3. Работа – макропроцесс передачи энергии в форме направленного движения одного тела другому (рис.22).
P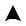 1
1
P = f(V)
l 2
V1 |
|
|
|
|
dV |
V |
|
|
|
|
|
|
|
|
|
Рис. 22. Графическое изображение работы в координатах P −V
В термодинамике передача энергии в форме работы может протекать двумя способами:
а) работой, связанной с изменением объёма рабочего тела. Эту работу называют работой расширения, работой газа или положительной работой:
l = ∫VV12PdV ;
25
б) работой, связанной с изменением внешней кинетической энергии без изменения объёма. В этом случае совершается работа внешних сил над рабочим телом. Этот вид работы называют работой над газом, отрицательной работой или располагаемой работой:
l = ∫PP12PdV .
Суммарное количество теплоты и работы определяет количество энергии, переданное в процессе энергообмена от одного тела к другому.
Работа характеризует упорядоченную форму обмена энергией с окружающей средой, при этом в системе всегда имеют место направленные макроскопические перемещения. Работа имеет размерность энергии и измеряется в джоулях (Дж). Величину L , отнесённую к массе рабочего тела, называют удельной работой, обозначают l и измеряют в Дж/кг.
Теплота и работа проявляются одновременно.
КОНТРОЛЬНЫЕ ВОПРОСЫ
1.Что изучает техническая термодинамика?
2.Что называется рабочим телом в технической термодинамике?
3.Какие термодинамические параметры относятся к основным?
4.Напишите размерность основных параметров.
5.Назовите и дайте определение функций состояния рабочего те-
ла.
6.Какими формами движения можно передавать энергию от одного тела к другому?
7.В чём состоит принципиальное отличие между теплотой и температурой?
8.Какие вы знаете температурные шкалы и какая между ними существует связь?
9.Какими приборами можно измерить давление и температуру?
10.Назовите разновидности давлений.
11.Что такое абсолютное давление и как оно определяется?
12.Какие вы знаете единицы измерения давлений, есть ли между ними связь?
26
СПИСОК РЕКОМЕНДУЕМОЙ ЛИТЕРАТУРЫ
1.Кириллин В.А. Техническая термодинамика / В.А. Кириллин,
В.В. Сычев. – М.: Наука, 1979. – 512 с.
2.Чистяков С.Ф. Теплотехнические измерения и приборы / С.Ф. Чистяков, Д.В. Радун. – М.: Высш. шк., 1972. – 264 с.
3.Нащокин В.В. Техническая термодинамика и теплопередача. –
М.: Высш. шк., 1980. – 469 с.
4.Андрющенко А.И. Основы технической термодинамики реальных процессов. – М.: Высш. шк., 1975. – 264 с.
27
Составители Владимир Владимирович Назаревич
Сергей Юрьевич Харченко
ПАРАМЕТРЫ И ФУНКЦИИ СОСТОЯНИЯ РАБОЧЕГО ТЕЛА. ПРИБОРЫ ДЛЯ ИЗМЕРЕНИЯ ПАРАМЕТРОВ СОСТОЯНИЯ
Методические указания к лабораторной работе по курсам: «Термодинамика» и «Теплоснабжение и тепловое хозяйство шахт» для студентов специальности 150200 «Автомобили и автомобильное хозяйство», специальности 170100 «Горные машины и оборудование»
Редактор Е.Л. Наркевич
ИД № 06536 от 16.01.02
Подписано в печать 25.12.2000. Формат 60×84/16. Бумага офсетная. Отпечатано на ризографе. Уч.-изд. л. 1,8. Тираж 75 экз. Заказ
ГУ Кузбасский государственный технический университет. 650026, Кемерово, ул. Весенняя, 28.
Типография ГУ Кузбасский государственный технический университет. 650099, Кемерово, ул. Д. Бедного, 4а.
