
4 курс / Общая токсикология (доп.) / Sernaya_kislota
.docxСерная кислота
Серная кислота H2SO4 имеет широкое применение в промышленности, в лабораториях, используется и бытовой обстановке (чаще всего в виде так называемого купоросного масла).
Чистая серная кислота — бесцветная, прозрачная маслянистая жидкость; неочищенная (купоросное масло) — буроватая жидкость, содержит 91—92% H2S04, в продаже—30—40%; серная кислота дымящаяся жидкость, в ней растворено 10—12%' серного ангидрида. При попадании на кожу серная кислота вызывает сильное жжение, проникая вглубь тканей, образует струп, сначала белого, а затем коричневого и даже черного цвета. По отпадении струпьев остаются глубокие язвы, заживающие с образованием стягивающих обезображивающих рубцов. Воздействие паров серной кислоты (что может наблюдаться, например, при травлении металлов) вызывает раздражение верхних дыхательных путей (насморк, кашель, затруднение дыхания), покраснение конъюнктивы, жжение в глазах.
При смертельных отравлениях доза концентрированной серной кислоты колеблется в пределах 3—10 г. Тяжесть клинической картины, течения и исхода отравления зависит от степени концентрации и количества принятой внутрь кислоты. Смертность превышает 50%.
Оксид серы раздражает дыхательные пути, вызывая спазм бронхов и увеличение сопротивления дыхательных путей. Острые отравления со смертельным исходом редки. Обычно считают, что смерть наступает от удушья вследствие рефлекторного спазма голосовой щели, внезапной остановки кровообращения в легких или шока. Смерть наступает как вскоре после отравления (через несколько часов) от отека легких, так и значительно позже (через 20 дней - 10 месяцев) - от заболевания органов дыхания. При воздействии SO2 в виде аэрозоля, образующегося при туманах и повышенной влажности воздуха, раздражающий эффект сильнее. При неблагоприятных метеорологических условиях может вызвать массовое отравление населения. Влажная поверхность слизистых поглощает SO2, затем последовательно образуются H2SO3 и H2SO4. Общее действие оксида серы заключается в нарушении углеводного и белкового обмена; угнетении окислительных процессов в головном мозге, печени, селезенке, мышцах; торможении окислительного дезаминироваиия аминокислот и окисления пировиноградной кислоты; снижении содержания витаминов B1 и С и т. д. Он также раздражает кроветворные органы, способствует образованию метгемоглобина и увеличивает токсичность образующихся соединений; увеличивает выделение с мочой копропорфирина и бисульфитсвязанных соединений; вызывает изменения в эндокринных органах, костной ткани; нарушает генеративную функцию. Имеются указания на эмбриотоксическое действие. Возможно, что существенную роль в указанных сдвигах играет ацидоз (поскольку SO2, циркулирующий в крови, растворяется в плазме и превращается в H2SO3).
Исследование на кислоты производятся, если предварительные испытания или материалы дела указывают на возможность отравления этими веществами. Объектами исследования являются содержимое желудка, рвотные массы, остатки пищи, частицы одежды и т.д., при исследовании на соли-печень.
На отравление серной кислотой может указывать внешний вид объектов исследования или трупа. Так, например, у лиц, принявших концентрированную серную кислоту, могут быть химические ожоги тканей губ, языка, пищевода, желудка в виде бурых полос и пятен, слизистые рта, глотки, пищевода при этом меняют цвет на серо-бурый, слизистая желудка – на серовато-красный, одежда, на которую попала серная кислота, может быть повреждена.
Для доказательства присутствия минеральных кислот в диализатах определяют кислотность этих жидкостей и наличие в них анионов соответствующих кислот.
Предварительно определение кислотности диализатов или содержимого желудка проводится с помощью кислотно-основных индикаторов, которые изменяют свою окраску в кислой среде (метиловый фиолетовый, метиловый оранжевый, конго красный и др.).
Для проверки кислотности вытяжек (диализатов) и для ориентировочного определения рН среды может также быть использована бумага, пропитанная универсальным индикатором.
После того как установлена ярко выраженная кислая реакция вытяжек из биологического материала или диализатов, проводят исследование этих жидкостей на наличие анионов серной, азотной, соляной и других кислот, при этом положительный результат предварительных испытаний диализата еще не является доказательством отравлений серной, соляной или другой кислотой, т.к. анионы указанных кислот могут присутствовать в организме как составная часть органов и тканей.
Предварительная реакция на сульфаты: к 1 мл диализата добавляют 0,1 мл 10% раствора HCl и 1 мл 5% раствора BaCl. При наличии сульфатов образуется белый осадок.
Для доказательства отравлений минеральными кислотами необходимо отогнать их из диализатов. При этом отгоняются только свободные кислоты. Учитывая то, что серная и азотная кислоты перегоняются при относительно высокой температуре, вначале эти кислоты переводят в более летучие соединения, которые в процессе перегонки легко переходят в дистилляты, например, серную кислоту переводят в сернистую, летучую в виде ангидрида.
Выделение серной кислоты из биологического материала
Подлежащие исследованию органы трупов измельчают, заливают водой до получения кашицеобразной массы, которую оставляют на 1—2 ч. Полученную вытяжку отфильтровывают, подвергают диализу 2-3 раза по 4-6 часов, слитые вместе диализаты выпаривают на водяной бане до 5-10 мл, а затем из диализата отгоняют серную кислоту.
При химико-токсикологическом исследовании серной кислоты на одежде или на других объектах эту кислоту можно извлечь этиловым спиртом, в котором растворяется эта кислота и не растворяются ее соли. С этой целью исследуемый материал измельчают и прибавляют к нему этиловый спирт. Через некоторое время жидкость отфильтровывают от твердых частиц исследуемого материала. Фильтрат на водяной бане выпаривают досуха. К сухому остатку прибавляют 10 мл воды, кипятят несколько минут, а затем охлаждают жидкость до комнатной температуры. Из полученной жидкости отгоняют серную кислоту и исследуют ее в дистилляте.
Отгонка серной кислоты
К диализатам прибавляют медные опилки и нагревают. При этом образуется ангидрид сернистой кислоты SO2, который отгоняют и собирают в приемник, содержащий раствор иода в йодиде калия. При взаимодействии ангидрида сернистой кислоты с водой и иодом образуется серная кислота:
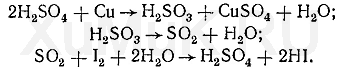
Способ отгонки серной кислоты состоит в следующем: в колбу аппарата для отгонки жидкостей, состоящего из колбы, холодильника с алонжем и приемника, вносят диализат и медные опилки. Конец аллонжа опускают в приемник, содержащий раствор иода. Колбу устанавливают на масляную или песочную баню и нагревают. Если во время перегонки происходит быстрое обесцвечивание иода, то его раствор небольшими порциями дополнительно вносят в приемник. После окончания отгонки серной кислоты в приемник прибавляют 2—3 мл разбавленной соляной кислоты и нагревают жидкость до полного исчезновения иода, не вступившего в реакцию с ангидридом сернистой кислоты. Освобожденный от иода дистиллят используют для обнаружения в нем серной кислоты.
Обнаружение серной кислоты в дистилляте
Реакция с хлоридом бария. К 3—5 каплям дистиллята прибавляют 1—2 капли 5 %-го раствора хлорида бария. Появление белого осадка сульфата бария указывает на наличие серной кислоты в дистилляте. Образовавшийся осадок не растворяется в азотной и соляной кислотах, а также в щелочах.
Реакция с ацетатом свинца. К нескольким каплям дистиллята прибавляют 2—3 капли 3 %-го раствора ацетата свинца. При наличии серной кислоты выпадает белый осадок сульфата свинца, который не растворяется в азотной кислоте, но растворяется в едких щелочах и в растворе ацетата аммония при нагревании:
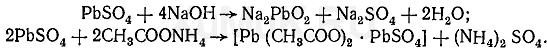
Реакция с родизонатом натрия основана на том, что родизонат натрия с солями бария образует родизонат бария, имеющий красную окраску. От прибавления серной кислоты или сульфатов к родизонату бария он разлагается. При этом образуется осадок сульфата бария и исчезает красная окраска родизоната:
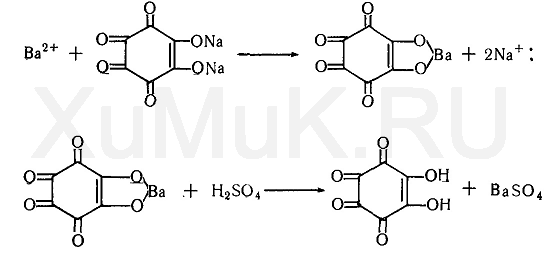
Выполнение реакции. На фильтровальную бумагу наносят каплю 1 %-го раствора хлорида бария и каплю свежеприготовленного 0,2 %-го раствора родизоната натрия. При этом на бумаге пятно приобретает красную окраску. На это пятно наносят 1—2 капли дистиллята. В присутствии серной кислоты окраска пятна исчезает. Эта реакция является специфичной на сульфаты и серную кислоту.
Количественное определение. Аликвоту извлечения титруют 0,1 М раствором гидроксида натрия в присутствии метилового оранжевого, затем в определенной части извлечения определяют количество сульфатов весовым способом, полученные результаты сопоставляют.
Результаты определения имеют относительное значение.
