4 курс / Сертификат медсестры / СОП_«Порядок_работы_с_незарегистрированными,_недоброкачественными
.docx
ООО «Аптека»/ИП Иванов И.И. |
|
Номер |
|
Лист |
|||
Название: Порядок работы с незарегистрированными, недоброкачественными, фальсифицированными, контрафактными товарами аптечного ассортимента |
|||
ДЕЙСТВУЕТ С: «___»__________20___г. |
ЗАМЕНЯЕТ: Вводится впервые |
ПРИЧИНА ПЕРЕСМОТРА: |
ДАТА СЛЕДУЮЩЕГО ПЕРЕСМОТРА: |
СОСТАВИЛ: |
УТВЕРДИЛ: Руководитель ____________________ «____»_______________20_______г. |
||
Цель: стандартизация работы с незарегистрированными, недоброкачественными, фальсифицированными, контрафактными товарами аптечного ассортимента
Область применения:
Где: на рабочих местах всех сотрудников аптеки
Когда: постоянно
Ответственность:
1. Сотрудник, ответственный за работу с фальсифицированными, недоброкачественными, контрафактными товарами аптечного ассортимента, товарами с истекшим сроком годности, товарами, обращение которых приостановлено.
2. Сотрудник, ответственный за систему качества (уполномоченный по качеству).
Основная часть СОП
1. Подготовительные операции: перечислить все карантинные зоны аптеки, указать в случаях и какой товар туда перемещается, как каждая из зон маркируется. Например, зоны карантинного хранения временно выведенных из обращения лекарственных средств расположены в шкафу № 5 в материальной комнате №1 и в холодильнике №2 (для термолабильных). Лекарственные препараты в этих зонах должны храниться в белых пластиковых контейнерах с маркировкой «Карантинная зона».
2. Если при приемочном контроле было выявлено несоответствие качества поступивших товаров условиям договора, данным сопроводительных документов, приемочная комиссия аптечной организации составляет Акт об установленном расхождении по количеству и качеству при приемке товарно-материальных ценностей. На основании акта в соответствии со статьей 483 ГК предъявляется претензия (направляется уведомление) поставщику.
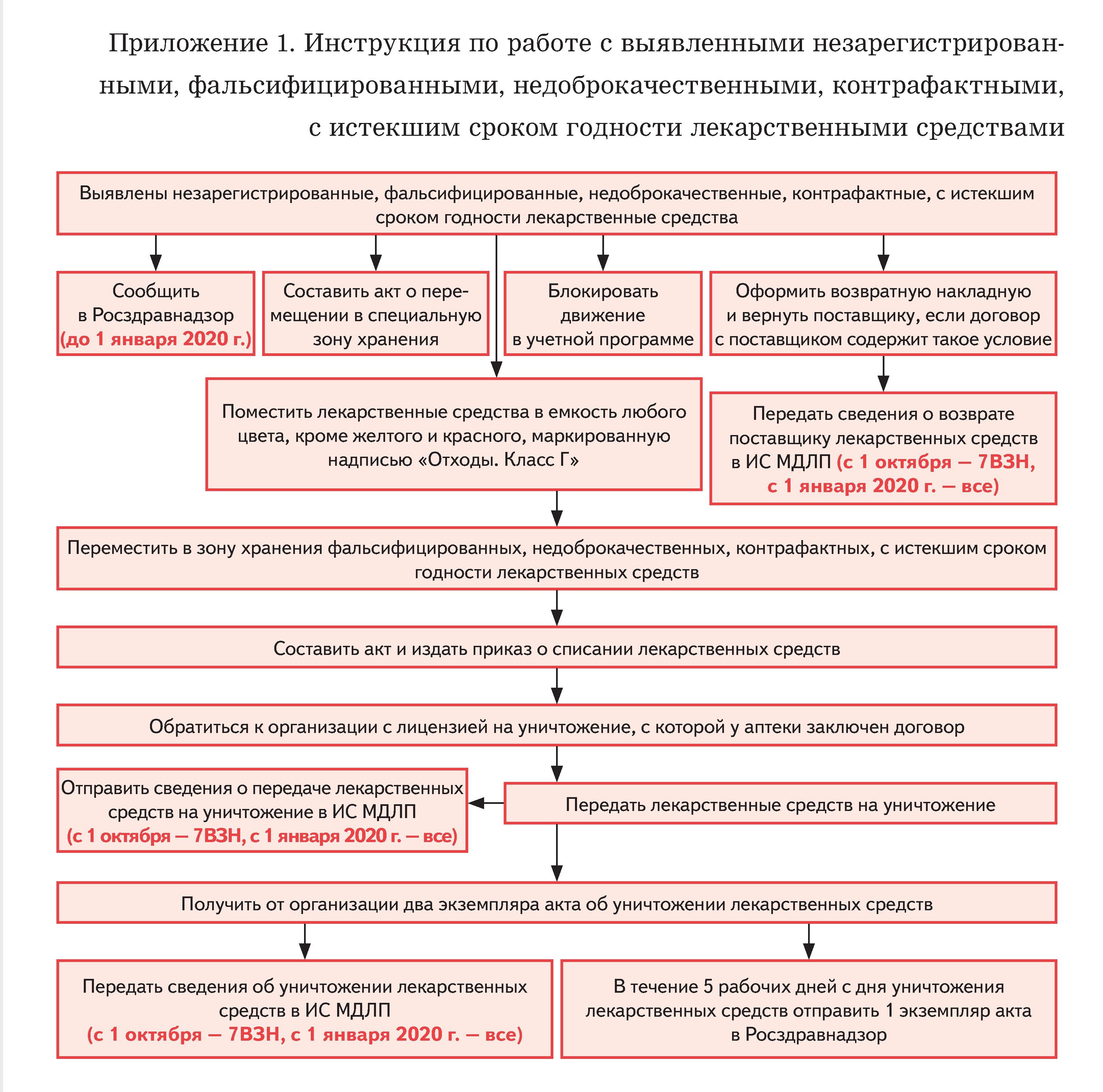
2. Порядок работы с незарегистрированными, недоброкачественными, фальсифицированными, контрафактными лекарственными средствами определяет инструкция для сотрудников (Приложение 1 к СОП).
3. Порядок работы с выявленными лекарственными средствами, обращение которых приостановлено, определяет инструкция для сотрудников (Приложение 2 к СОП).
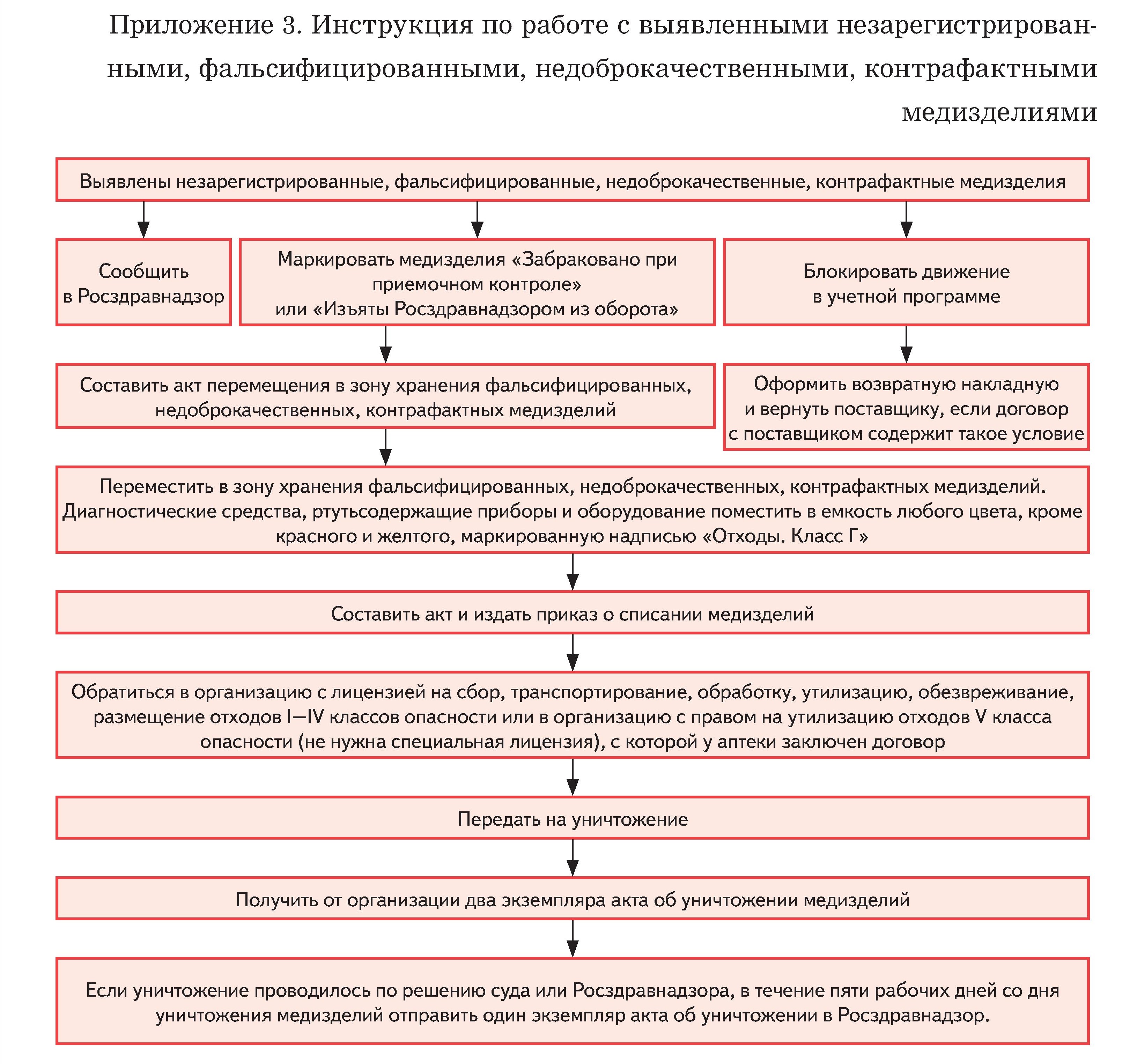
4. Порядок работы с незарегистрированными, недоброкачественными, фальсифицированными, контрафактными медицинскими изделиями определяет инструкция для сотрудников (Приложение 3 к СОП).
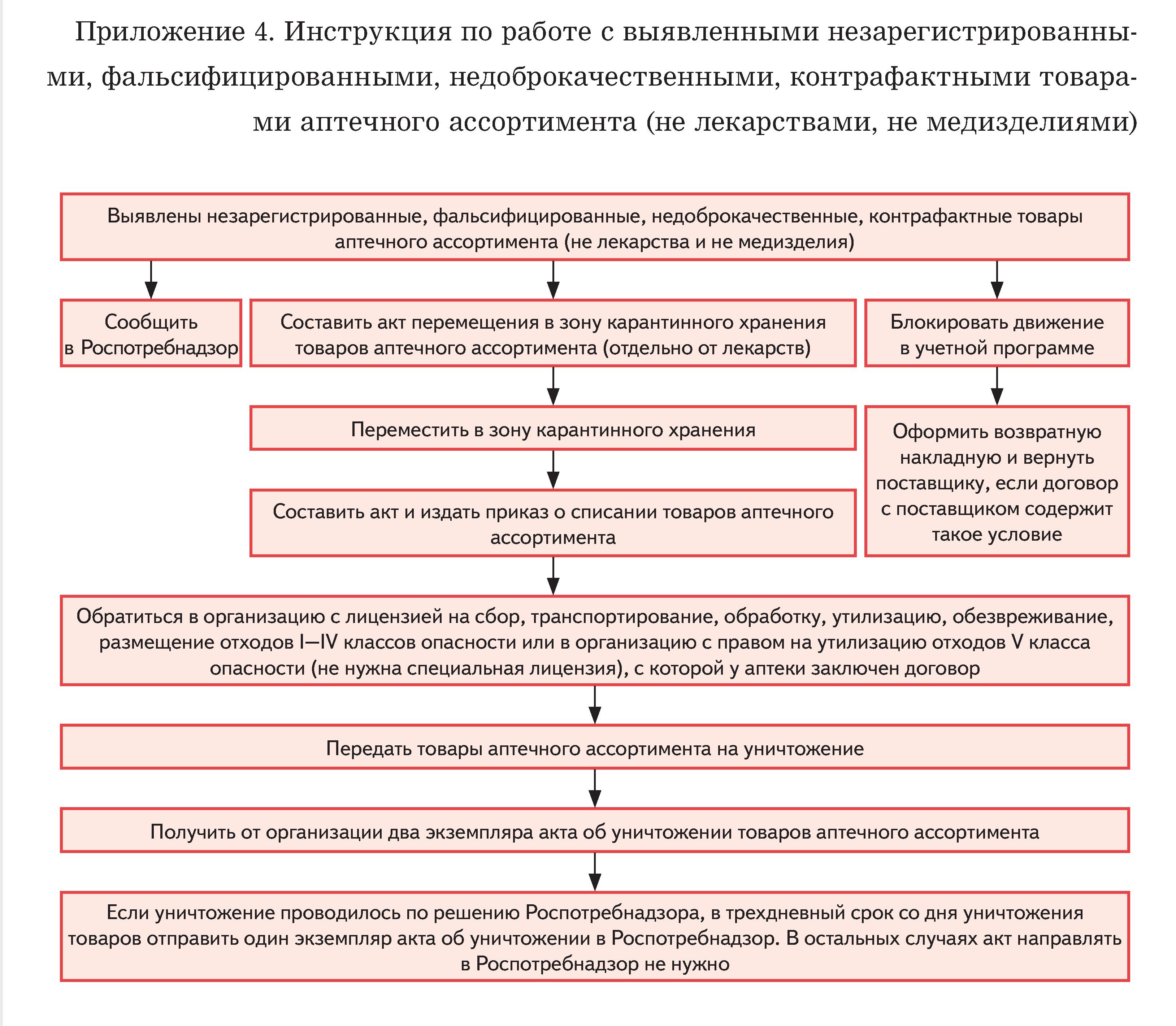
5. Порядок работы с другими незарегистрированными, недоброкачественными, фальсифицированными, контрафактными товарами аптечного ассортимента определяет инструкция для сотрудников (Приложение 4 к СОП).
6. Приложения к СОП: Инструкции для сотрудников 1–4, образец приказа
о списании и передаче на уничтожение товарно-материальных ценностей, образец акта о перемещении лекарственных препаратов в зону карантинного хранения/зону хранения фальсифицированных, недоброкачественных, контрафактных ЛП, лекарственных препаратов с истекшим сроком годности, приказ об организации работы с недоброкачественной продукцией в аптечной организации.
7. Нормативно-правовые документы, регулирующие уничтожение товаров аптечного ассортимента:
7.1. Федеральный закон от 21.11.2011 № 323-ФЗ «Об основах охраны здоровья граждан в Российской Федерации»
7.2. Федеральный закон от 12.04.2010 № 61-ФЗ «Об обращении лекарственных средств»
7.3. Приказ Минздрава от 31.08.2016 № 647н «Об утверждении Правил надлежащей аптечной практики ЛП для медицинского применения»
7.4. Приказ Минздрава от 31.08.2016 № 646н «Об утверждении Правил надлежащей практики хранения и перевозки лекарственных препаратов для медицинского применения»
7.5. Общая фармакопейная статья ОФС.1.1.0010.18 «Хранение лекарственных средств»
7.6. Постановление Главного государственного санитарного врача от 09.12.2010 № 163 «Об утверждении СанПиН 2.1.7.2790-10 "Санитарно-эпидемиологические требования к обращению с медицинскими отходами"».
7.7. Федеральный закон от 27.12.2002 № 184-ФЗ «О техническом регулировании»
7.8. Приказ Росздравнадзора от 27.04.2017 № 4043 «Об утверждении Перечня правовых актов и их отдельных частей (положений), содержащих обязательные требования, соблюдение которых оценивается при проведении мероприятий по контролю в рамках отдельного вида государственного контроля (надзора)»
7.9. Приказ Росздравнадзора от 09.11.2017 № 9438 «Об утверждении форм проверочных листов (списков контрольных вопросов), используемых Федеральной службой по надзору в сфере здравоохранения и ее территориальными органами при проведении плановых проверок при осуществлении федерального государственного надзора в сфере обращения лекарственных средств»
7.10. Постановление Правительства от 03.09.2010 № 674 «Об утверждении правил уничтожения фальсифицированных, недоброкачественных и контрафактных лекарственных средств»
7.11. Постановления Правительства от 29.09.1997 № 1263 «Об утверждении Положения о проведении экспертизы некачественных и опасных продовольственного сырья и пищевых продуктов, их использовании или уничтожении»
7.12. Технический регламент Таможенного союза ТР ТС 021/2011 «О безопасности пищевой продукции», утв. решением Комиссии Таможенного союза от 09.12.2011 № 880
7.13. Постановление Правительства от 12.12.2015 г. № 1360 «Об отдельных вопросах противодействия обороту фальсифицированных, недоброкачественных и контрафактных медицинских изделий»
7.14. Постановление Правительства от 14.12.2018 №1556 « Об утверждении Положения о системе мониторинга движения лекарственных препаратов для медицинского применения»
Ответственные исполнители ознакомлены и обязуются исполнять:
№ п/п |
Ф. И. О. |
Подпись |
Дата |
|
|
|
|
|
|
|
|
|
|
|
|