
5 курс / Пульмонология и фтизиатрия / Пневмонии_клиника,_диагностика,_лечение_и_профилактика_8
.pdf
Идиопатический легочныйфиброз
ном превышает 3000 евро при условии, что лечение должно проводиться пожизненно. Необходимо напомнить, что в странах ЕС ИЛФ относится к категории заболеваний, затраты на лечение которых компенсирует государство.
Однако следует отметить, что объем доказательств, полученных в ходе проведения рандомизированных исследований по изучению безопасности и эффективности нинтеданиба и пирфенидона при ИЛФ, не позволил авторам документа отнести рекомендацию использования препаратов к категории сильных (strong recommendation for use) — она отнесена к разряду условных (conditional recommendation for use).
Наряду с иматинибом, амбризентаном, варфарином отрицательную рекомендацию получила и комбинация преднизон + азатиоприн + N-ацетилцистеин). При этом если в руководстве 2011 года комбинация ГКС, ЦС и N-ацетилцистеина получила слабонегативную рекомендацию (weak-no), то в документе 2015 года она категорически не рекомендована к применению (strong recommendation against use). Предпосылкой для принятия такого решения явились предварительные результаты рандомизированного клинического исследования, которые были расценены как сигнал к увеличению показателя смертности и частоты госпитализаций в группе больных, получавших преднизон, азатиоприн и N-ацетилцистеин, в сравнении с группой плацебо [5]. В связи с этим исследование было досрочно остановлено.
На вопрос, как поступать с пациентами, которые принимают эту комбинацию препаратов и при этом субъективно оценивают ее эффективность и переносимость положительно, авторы документа отвечают следующим образом.
В таких случаях врачу необходимо провести с пациентом обсуждение потенциальных рисков приема ГКС и ЦС и принимать решение в каждом отдельном случае индивидуально в зависимости от ценностей и преференций больного.
С точки зрения авторов, эта рекомендация относится в первую очередь к украинским пульмонологам, лишенным возможности принимать альтернативные решения до той поры, когда рекомендованные руководством препараты станут доступными в Украине.
19

Очеркиклиническойпульмонологии
ЛИТЕРАТУРА
1.Fernandez-Perez, E. R. Incidence, prevalence, and clinical course of idiopathic pulmonary fibrosis [Text] / E. R. Fernandez-Perez, C. E. Daniels,
D.R. Schroeder et al. // Chest. — 2010. — Vol. 137. — P. 129–137.
2.American Thoracic Society, European Respiratory Society. Idiopathic pulmonary fibrosis: diagnosis and treatment. International consensus statement [Text] // Am. J. Respir. Crit. Care Med. — 2000. — Vol. 161. —
P.646–664.
3.An O cial ATS/ERS/JRS/ALAT Statement: Idiopathic Pulmonary Fibrosis: Evidence-based Guidelines for Diagnosis and Management [Text] // Am.
J.Respir. Crit. Care Med. — 2011. — Vol. 183. — P. 788–824.
4. An O cial ATS/ERS/JRS/ALAT Clinical Practice Guideline: Treatment of Idiopathic Pulmonary Fibrosis. An Update of the 2011 Clinical Practice Guideline [Text] // Am. J. Respir. Crit. Care Med. — 2015. — Vol. 192. —
P.e3–e19.
5.Raghu, G. Idiopathic Pulmonary Fibrosis Clinical Research Network. Prednisone, azathioprine, and N-acetylcysteine for pulmonary fibrosis [Text] /
G.Raghu, K. J. Anstrom, T. E. King et al. // N. Engl. J. Med. — 2012. — Vol. 366. —
P.1968–1977.
20

2. САРКОИДОЗ ОРГАНОВ ДЫХАНИЯ
Саркоидоз с поражением паренхимы легких в большинстве стран мира занимает первое место в структуре интерстициальных заболеваний легких (ИЗЛ). В Бельгии саркоидоз составляет 27 % всех случаев ИЗЛ [1], в Греции — 34,1 % [2], в Италии
— 33,7 % [3], во Франции саркоидоз и идиопатический легочный фиброз вместе — более 50 % [4]. С 70-х годов прошлого столетия наблюдается неуклонный рост заболеваемости саркоидозом и смертности больных [5, 6, 7].
Основные принципы диагностики и лечения саркоидоза представлены в Положении Американского торакального общества (ATS), Европейского респираторного общества (ERS) и Всемирной ассоциации саркоидоза и других гранулематозных поражений (WASOG) «Statement on Sarcoidosis» (1999) [8]. Согласно Положению, диагноз саркоидоза требовал обязательной верификации методами трансбронхиальной или хирургической биопсии легкого или внутригрудных лимфатических узлов, а в случае экстрапульмональных поражений — биопсии кожи и периферических лимфатических узлов. Вместе с тем за 15 лет, прошедшие от момента издания Положения, существенно возросли возможности компьютерной томографии органов дыхания, которая по результату морфологической диагностики патологических изменений в легких в настоящее время успешно конкурирует с патогистологическими методами.
Все это потребовало пересмотра диагностических подходов в ведении больных саркоидозом и явилось одной из предпосылок создания Унифицированного клинического протокола первичной, вторичной (специализированной) и третичной (высокоспециализированной) медицинской помощи «Саркоидоз» (приказ МЗ Украины № 634 от 08.09.2014) [9].
21

Очеркиклиническойпульмонологии
ОПРЕДЕЛЕНИЕ, ЭПИДЕМИОЛОГИЯ, КЛАССИФИКАЦИЯ
Саркоидоз — полисистемное заболевание неизвестной природы, характеризующееся образованием в пораженных органах неказеифицирующихся эпителиоидноклеточных гранулем.
Код МКБ 10: D86.0–2.
Обычно саркоидоз поражает людей молодого и среднего возраста и часто проявляется двусторонней лимфаденопатией корней легких, диссеминацией паренхимы легких, поражением глаз и кожи. Также могут быть вовлечены печень, селезенка, другие группы лимфатических узлов, слюнные железы, сердце, нервная система, мышцы, кости и другие органы. Бронхолегочная система поражается при саркоидозе в 90–95 % случаев.
Заболеваемость саркоидозом в разных странах мира варьирует от 0,125 до 24,0 новых случаев на 100 000 населения в год, распространенность — от 1 до 64 на 100 000 населения [10].
Достоверное влияние на заболеваемость саркоидозом оказывает климатический фактор — в странах Африки, Азии и Центральной Америки показатели заболеваемости саркоидозом самые низкие, а в странах с умеренным и холодным климатом — самые высокие [11]. Заболеваемость, превышающая 10 случаев на 100 000 населения в год, наблюдается в североевропейских странах — Дании (10,1), Финляндии (11,4), Норвегии (15,0) и Швеции (24,0) [12–14].
Получено статистическое подтверждение прямой зависимости заболеваемости саркоидозом в разных странах от их географической широты [15].
Описаны случаи семейного саркоидоза, частота которого составляет 1,7 % в Великобритании, 9,6 % в Ирландии, 3,6 % в Финляндии, 3,0 % в Татарстане [10].
Максимальный уровень заболеваемости саркоидозом наблюдается в возрасте от 35 до 55 лет, лица в возрасте до 25 и старше 75 лет болеют редко [16]. У мужчин пик заболеваемости отмечается в возрасте 30–35 лет, у женщин регистрируется два возрастных пика — 35–40 лет и приблизительно 55 лет [17, 18].
22

Саркоидозоргановдыхания
Практически во всех эпидемиологических исследованиях отмечено, что среди больных саркоидозом преобладают женщины (примерно 65 %).
В Украине заболеваемость саркоидозом органов дыхания составляет в среднем от 1,1 до 2,6 на 100 000 взрослого населения, а распространенность — от 4,6 до 7,9 на 100 000, что соответствует уровню южноевропейских стран. Ежегодно в Украине регистрируется приблизительно 700 новых случаев саркоидоза, а общее количество больных активным саркоидозом составляет около 2500 [19].
Длительное время для обозначения саркоидоза применялся эпонимический термин «болезнь Бенье-Бека-Шауманна», однако в 1948 г. на конференции в Вашингтоне был принят термин «саркоидоз», который в настоящее время используется в международной классификации болезней.
Положением ATS, ERS и WASOG Statement on Sarcoidosis (1999) [8] была принята классификация саркоидоза органов дыхания, основанная на данных рентгенографии органов грудной полости (таблица 2.1).
Таблица 2.1 Классификация саркоидоза органов дыхания по данным рентге-
нографии органов грудной полости (ATS/ERS/WASOG, 1999)
Стадии |
Характер изменений |
0Изменения на рентгенограммах отсутствуют.
IДвусторонняя прикорневая лимфаденопатия (ДПЛ).
II |
ДПЛ, изменения в легочной паренхиме. |
III |
Изменения в легочной паренхиме без ДПЛ. |
IV |
Распространенный фиброз легких. |
В 0 стадию отнесены пациенты, у которых отсутствуют изменения на рентгенограммах органов грудной полости, однако имеются экстраторакальные проявления саркоидоза. Тем не менее, у значительной части этих больных могут быть выявлены гранулемы в биопсийном материале легочной ткани [11]. По обобщенным статистическим данным, число пациентов с 0 стадией составляет 5–10 % от общего числа больных саркоидозом, пациентов с I стадией — 40–50 %, II стадией — 15–30 %, III стадией — 10–15 %, IV стадией — 5–10 % [8].
23

Очеркиклиническойпульмонологии
Необходимо отметить, что широкое внедрение в практику компьютерной томографии существенно изменило указанное распределение больных по стадиям — поскольку возможности компьютерной томографии в диагностике поражений паренхимы легких значительно выше по сравнению с рентгенографией, доля больных саркоидозом II–III стадии заметно возросла. По нашим данным, основанным на анализе медицинской документации 1776 больных, II стадия заболевания регистрировалась даже несколько чаще, чем I стадия (43,6 % и 41,6 % соответственно).
На рисунках 2.1–2.4 представлены характерные изменения, выявленные при рентгенографии (РГ) и компьютерной томографии высокого разрешения (КТВР) органов грудной полости у больных с разными стадиями саркоидоза органов дыхания.
Рис. 2.1. Саркоидоз органов дыхания I стадии (РГ и КТВР) — двусторонняя прикорневая лимфаденопатия.
Рис. 2.2. Саркоидоз органов дыхания II стадии
(РГ и КТВР) — двусторонняя прикорневая лимфаденопатия в сочетании с поражением паренхимы.
24
Саркоидозоргановдыхания
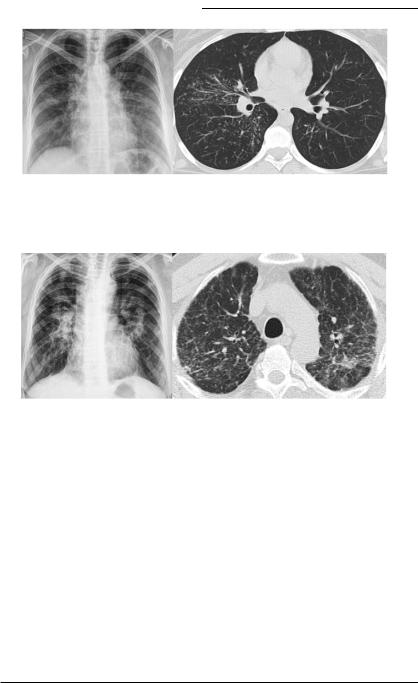
Рис. 2.3. Саркоидоз органов дыхания III стадии (РГ и КТВР) — поражение паренхимы без двусторонней прикорневой лимфаденопатии.
Рис. 2.4. Саркоидоз органов дыхания III стадии (РГ и КТВР) — распространенный фиброз легких.
ПАТОГЕНЕЗ И ПАТОМОРФОЛОГИЯ
Саркоидоз определяют как |
полиорганное заболева- |
ние неустановленной этиологии, |
которое характеризуется |
Т-лимфоцитарно-моноцитарной инфильтрацией в пораженных органах, формированием гранулем и нарушением нормальной микроархитектуры ткани. Саркоидные гранулемы представляют собой скопления активированных клеток моноцитарно-ма- крофагального ряда, а также развивающихся в условиях воспаления гигантских многоядерных клеток, эпителиоидных клеток и лимфоцитов [8].
25

Очеркиклиническойпульмонологии
Поскольку гранулемы при саркоидозе содержат большое количество лимфоцитов, их еще называют «иммунными», так как в них происходят иммунные реакции, направленные на элиминацию неустановленных пока антигенов [10]. В отличие от «неиммунных» гранулем, образующихся в ответ на воздействие неорганических агентов (кремний, бериллий и др.), образование «иммунных» гранулем сопровождается специфическим Т-клеточным ответом. Можно полагать, что в случае саркоидоза инициирующий агент обладает свойствами антигенности, находится в нижних отделах респираторного тракта, поглощается альвеолярными макрофагами и предоставляется в иммуногенной форме Т-лимфоцитам. Эти предположения подтверждаются результатами исследований, в которых введение фрагментов мембран альвеолярных макрофагов больных саркоидозом легких в кожу экспериментальных животных вызывало развитие кожных саркоидных реакций, а также способностью гранулем персистировать в пораженной ткани [10].
Для саркоидоза характерен перигранулемный тип фиброзирования. Поскольку процесс фиброзирования легочной ткани носит необратимый характер, с целью его возможного предотвращения проводится поиск маркеров интенсивности процесса фиброобразования при саркоидозе, который, к сожалению, еще не привел к положительным результатам.
Гистологически саркоидоз можно определить как заболевание, характеризующееся формированием во многих органах и тканях эпителиоидноклеточных гранулем без казеозного некроза [11]. Возможно развитие центрального фибриноидного некроза, однако он, как правило, точечный, плохо визуализирующийся. Некроз обычно предшествует либо резорбции грнулемы либо ее гиалинизации.
Эпителиоидноклеточная гранулема состоит из высокодифференцированных мононуклеарных (одноядерных) фагоцитов (эпителиоидных и гигантских клеток) и лимфоцитов. Гигантские клетки могут содержать цитоплазматические включения, такие как астероидные тельца и тельца Шаумана. Центральная часть гранулемы состоит преимущественно из CD4+ лимфоцитов, тогда как CD8+ лимфоциты представлены в периферической зоне [8, 10].
26

Саркоидозоргановдыхания
Процесс организации гранулем начинается с периферии, что придает им четко очерченный, «штампованный» вид (рис. 2.5).
В саркоидной гранулеме могут развиваться фиброзные изменения, которые обычно начинаются с периферии, распространяются к центру и завершаются полным фиброзом и/или гиалинизацией [8].
Саркоидные гранулемы локализуются в лимфатических узлах (особенно внутригрудных), паренхиме легких, в печени, селезенке. В легких приблизительно 75 % гранулем тесно прилегают или находятся в середине соединительнотканных структур около бронхиол, субплеврально или в перилобулярных пространствах. Вовлечение лимфатических сосудов наблюдается более чем у половины больных при открытой биопсии легких или аутопсии [8].
Саркоидные гранулемы заживают либо путем характерного концентрического фиброзирования, либо путем образования гомогенных гиалиновых тел. Факторы, которые оказывают влияние на развитие фиброза, пока недостаточно изучены. У 5–10 % больных саркоидозом легких развивается распространенный
Рис. 2.5. Эпителиоидноклеточная гранулема с циркулярным фиброзом по периферии. Гематоксилин-эозин, × 100 [Черняев А. Л., 2010].
27

Очеркиклиническойпульмонологии
интерстициальный фиброз (IV стадия саркоидоза), представляющий собой исход заболевания. На этой стадии теряются специфические морфологические черты саркоидоза [11].
Морфологический диагноз саркоидоза легких базируется на трех главных признаках: присутствие хорошо сформированной гранулемы с ободком из лимфоцитов и фибробластов по внешнему краю; перилимфатическое интерстициальное распределение гранулем (именно это делает трансбронхиальную биопсию чувствительным диагностическим методом) и исключение других причин образования гранулем [8].
ДИАГНОСТИКА Клинические проявления
Клиническая семиотика саркоидоза органов дыхания зависит от стадии заболевания. Саркоидоз I стадии протекает, как правило, бессимптомно и выявляется в результате профилактического рентгенологического обследования или при рентгенографии в связи с наличием экстрапульмональных проявлений [11, 20, 21]. У больных саркоидозом II и III стадии клинические проявления отсутствуют примерно у 20–30 % больных [20].
Начало заболевания может быть острым или малозаметным и постепенным. Для острого дебюта характерны респираторные симптомы (сухой кашель, боли в грудной клетке, реже
— одышка), повышение температуры тела, суставной синдром (артралгии, реже — артриты), узловатая эритема, увеличение периферических лимфатических узлов.
Симтомокомплекс, включающий двустороннюю лимфаденопатию, повышение температуры тела, узловатую эритему и суставной синдром, именуется синдромом Лефгрена в честь шведского клинициста Свена Лефгрена (Sven Löfgren, 1910–1978), который не только описал этот симптомокомплекс [22], но и внес большой вклад в учение о саркоидозе.
Узловатая эритема представляет собой гиперергическую реакцию. Эритематозные узелки, слегка приподнятые над кожей, могут возникать на любом участке тела, хотя наиболее частой локализацией узловатой являются голени, бедра, раз-
28
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/
