
- •Вопросы к зачёту по химии для студентов стоматологического факультета осенний семестр 2016-2017 уч.Год
- •Общая химия Вопросы №1 (способы выражения концентрации растворов, , скорость химической реакции, химическое равновесие, коллигативные свойства растворов, теория электролитов).
- •Вопросы №2 (водородный показатель, гидролиз солей, гетерогенные равновесия, комплексные соединения, поверхностные явления, адсорбция, дисперсные системы).
- •. Сравните растворимость этих солей.
- •Вопросы № 3 (биоорганическая химия).
Вопросы к зачёту по химии для студентов стоматологического факультета осенний семестр 2016-2017 уч.Год
В программу зачёта по предмету «Химия» входят следующие темы:
Способы выражения концентрации растворов
Химическая кинетика – скорость химической
реакции и химическое равновесие
Коллигативные свойства растворов
Теория электролитов
Водородный показатель
Гидролиз солей
Гетерогенные равновесия
Комплексные соединения
Поверхностные явления, адсорбция
Дисперсные системы
Поли- и гетерофункциональные соединения
Гетероциклические соединения
Углеводы
Аминокислоты.
Зачётный билет включает в себя два вопроса по общей химии и один вопрос по органической химии
Общая химия Вопросы №1 (способы выражения концентрации растворов, , скорость химической реакции, химическое равновесие, коллигативные свойства растворов, теория электролитов).
Смешали равные объёмы растворов соляной кислоты с концентрацией 0,1 моль/л. Чему равна молярная концентрация полученного раствора?
К 1л раствора соляной кислоты с концентрацией 0,1 моль/л добавили 4 л дистиллированной воды. Рассчитать молярную концентрацию полученного раствора.
К 1л раствора соляной кислоты с концентрацией 0,1 моль/л добавили 1 л раствора соляной кислоты с концентрацией 0,2 моль/л. Рассчитать молярную концентрацию полученного раствора.
Какой объём воды необходимо добавить к 200 г 4% раствора, чтобы получить 1% раствор?
Как изменяются в обратимом процессе скорости прямой и обратной реакций с течением времени?
Скорость реакции 2A + 2B → D рассчитывается по уравнению
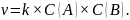 Чему
равен порядок этой реакции?
Чему
равен порядок этой реакции?
Скорость некоторой реакции не зависит от концентрации реагентов. Чему равен порядок этой реакции?
Во сколько раз необходимо повысить давление в системе:
 ,
чтобы скорость реакции возросла в 64
раза?
,
чтобы скорость реакции возросла в 64
раза?
Запишите выражение константы равновесия для системы:
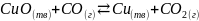
К системе
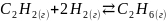 ,
находящейся в состоянии химического
равновесия, добавили водород. Изменилась
ли константа равновесия?
,
находящейся в состоянии химического
равновесия, добавили водород. Изменилась
ли константа равновесия?В систему внесли катализатор. Изменилась ли константа равновесия?
Какие воздействия можно произвести на систему
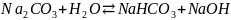 ,
находящуюся в состоянии химического
равновесия, для смещения равновесия
вправо?
,
находящуюся в состоянии химического
равновесия, для смещения равновесия
вправо?
Осмотическое давление внутри клетки составляет 7,1 атм. Что произойдет при помещении клетки в дистиллированную воду?
Сравните температуры кристаллизации водных растворов глюкозы с моляльностью 0,2 моль/кг и 0,4 моль/кг.
Сравните температуры кипения водных растворов сахарозы с моляльностью 0,2 моль/кг и 0,4 моль/кг.
Сравните значения осмотического давления бензола, этанола, дистиллированной и водопроводной воды.
Как изменится степень диссоциации уксусной кислоты при разбавлении раствора? А константа диссоциации?
Степень диссоциации электролита равна 90%. К какому классу электролитов относится это вещество – к слабым, сильным или средней силы?
Сравните ионную силу растворов хлорида кальция и сульфата железа (III) с равными молярными концентрациями.
рКа (HCN) = 9,31, рКа (HCOOH) = 3,77. Какой анион является более сильным основанием, CN – или HCOO-?
