
4 курс / Дерматовенерология / Виды филлеров
.pdfОбзор |
Review |
Пластическая хирургия и эстетическая медицина |
Plastic Surgery and Aesthetic Medicine |
2023, №1, с. 67-76 |
2023, no 1, pp. 67-76 |
https://doi.org/10.17116/plast.hirurgia202301167 |
https://doi.org/10.17116/plast.hirurgia202301167 |
Виды филлеров и их характеристика (часть 1)
© Е.В. ИКОННИКОВА1, 2, Н.Е. МАНТУРОВА2, 3, Л.С. КРУГЛОВА1, 2
1ФГБУ ДПО «Центральная государственная медицинская академия» Управления делами Президента Российской Федерации,
Москва, Россия;
2АО «Институт пластической хирургии и косметологии», Москва, Россия;
3ФГАОУ ВО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» Минздрава России,
Москва, Россия
РЕЗЮМЕ
Инъекционная контурная пластика является одной из наиболее востребованных процедур в косметологии, и ее популярность не-
уклонно возрастает. Широкий ассортимент филлеров, представленных на рынке, позволяет проводить успешную коррекцию эстетических недостатков и возрастных изменений с учетом индивидуальных особенностей пациента. Возникновение отсроченных вос-
палительных реакций является редко встречающимся нежелательным явлением и часто приводит к диагностическим затруднениям,
особенно при наличии косметологических процедур в анамнезе. Осложняет ситуацию применение несертифицированных филлеров, многие из которых являются перманентными, что напрямую влияет на тактику терапии и ее прогноз. Поэтому знания о свойствах, характеристиках, особенностях поведения в тканях различных видов филлеров необходимы каждому врачу-косметологу, дерматовенерологу, пластическому хирургу. В первой части обзора приводится классификация филлеров и дается подробное описание
перманентных микроимплантатов.
Ключевые слова: осложнения, перманентные филлеры, постоянные филлеры, синтетические филлеры, отсроченная воспалительная
реакция, гистология филлеров, гранулема.
ИНФОРМАЦИЯ ОБ АВТОРАХ:
Иконникова Е.В. — https://orcid.org/0000-0002-8813-9132 Мантурова Н.Е. — https://orcid.org/0000-0003-4281-1947 Круглова Л.С. — https://orcid.org/0000-0002-5044-5265
Автор, ответственный за переписку: Иконникова Е.В. — e-mail: evikonnikova@bk.ru
КАК ЦИТИРОВАТЬ:
Иконникова Е.В., Мантурова Н.Е., Круглова Л.С. Виды филлеров и их характеристика (часть 1). Пластическая хирургия и эстетическая медицина. 2023;1:67–76. https://doi.org/10.17116/plast.hirurgia202301167
Types of fillers and their characteristics (part 1)
© E.V. IKONNIKOVA1, 2, N.E. MANTUROVA2, 3, L.S. KRUGLOVA1, 2
1Central State Medical Academy of Administrative Directorate of the President of the Russian Federation, Moscow, Russia; 2Institute of Plastic Surgery and Cosmetology, Moscow, Russia;
3Pirogov Russian National Research Medical University, Moscow, Russia
ABSTRACT
Contouring injection is one of the most popular procedures in cosmetology, and its popularity is steadily increasing. Various available fillers allow successful correction of aesthetic defects and age-related changes considering individual characteristics of patients. Delayed inflammatory reactions are a rare undesirable phenomenon and often lead to diagnostic difficulties, especially after previous cosmetic procedures.
Non-certified fillers complicate the situation. Many of these fillers are permanent that directly affects therapeutic strategy and prognosis. Therefore, every cosmetologist, dermatologist and plastic surgeon should be aware of the properties, characteristics and behavior in tissues of various fillers. The first part of review is devoted to classification of fillers and description of permanent microimplants.
Keywords: complications, permanent fillers, synthetic fillers, delayed inflammatory reaction, histology of fillers, granuloma.
INFORMATION ABOUT THE AUTHORS:
Ikonnikova E.V. — https://orcid.org/0000-0002-8813-9132
Manturova N.E. — https://orcid.org/0000-0003-4281-1947
Kruglova L.S. — https://orcid.org/0000-0002-5044-5265
Corresponding author: Ikonnikova E.V. — e-mail: evikonnikova@bk.ru
TO CITE THIS ARTICLE:
Ikonnikova EV, Manturova NE, Kruglova LS. Types of fillers and their characteristics (part 1). Plastic Surgery and Aesthetic Medicine. 2023;1:67–76. (In Russ.). https://doi.org/10.17116/plast.hirurgia202301167
Plastic surgery and aesthetic medicine 2023, no 1 |
67 |

Обзор Review
Несмотря на длительную историю применения |
цины некоторых из этих изделий остановлено [10], |
различных инъекционных микроимплантатов |
эти филлеры до сих пор встречаются на сером рын- |
(филлеров), их общепризнанная классификация |
ке или применяются в ряде стран офф-лейбл [18, 19]. |
до сих пор отсутствует [1]. Филлеры можно клас- |
А к врачам по поводу лечения осложнений или про- |
сифицировать по-разному, например в зависимо- |
ведения дополнительных процедур обращаются па- |
сти от особенностей состава: аутологичные, био- |
циенты, которым в разное время были введены не- |
логические или синтетические. Абсолютным боль- |
резорбирующиеся материалы. |
шинством авторов, включая консенсусные группы, |
|
филлеры подразделяются в зависимости от продол- |
Характеристика различных видов |
жительности действия на временные (биоразлагае- |
|
мые), полупостоянные (с замедленной биодеграда- |
филлеров |
цией) и постоянные (перманентные, небиоразлагае- |
|
мые) [1—3] (табл. 1). |
Реакция тканей при имплантации филлеров |
R.J. Rohrich и соавт. предложили более деталь- |
в кожу и жировую клетчатку определяется во мно- |
ную классификацию, разделив филлеры в зависи- |
гом их физико-химическими свойствами. К про- |
мости от времени их обнаружения в тканях на вре- |
гнозируемым реакциям относятся эритема, отек, |
менные (менее 6 мес), длительные (от 6 мес до 2 лет), |
кровоизлияния в местах инъекций и болевые ощу- |
полупостоянные (от 2 до 5 лет) и постоянные (более |
щения. Эти явления характерны для раннего пост- |
5 лет) [4], однако эта классификация не получила |
процедурного периода, связаны, в том числе, с са- |
широкого распространения. |
мой процедурой инъекций и обычно разрешаются |
Таким образом, к временным сегодня относятся |
самопроизвольно в течение нескольких дней [20]. |
филлеры на основе гиалуроновой кислоты, которые, |
Все виды филлеров после введения вызывают вари- |
по заявлениям производителей, полностью резорби- |
абельное воспаление в комплексе реакций на ино- |
руются в течение 6—24 мес [1, 5]. |
родное тело [21, 22], что, при благоприятных усло- |
К полупостоянным относятся филлеры, состо- |
виях, приводит к перифокальному неоколлагено- |
ящие из поли-L-молочной кислоты (PLLA) [6], |
генезу. При введении инъекционного имплантата |
поли-L,D-молочной кислоты (PLDLA), гидрокси- |
в ткани происходит активизация тканевых фермен- |
апатита кальция (CaHA) (микросферы, суспенди- |
тов и образование свободных радикалов, расщепляю- |
рованные в геле на основе карбоксиметилцеллю- |
щих филлер на мелкие фрагменты, которые захваты- |
лозы) [7] и поликапролактона (PCL) (микросферы, |
ваются и удаляются циркулирующими макрофагами |
суспендированные в геле на основе карбоксиметил- |
с дальнейшим попаданием частиц в лимфу. Размер, |
целлюлозы) [8]. Период их резорбции находится |
форма и гидрофильность частиц напрямую влияют |
в пределах 12—36 мес. |
на эффективность фагоцитоза (табл. 2). |
К постоянным относятся филлеры, содержащие |
Частицы диаметром более 20 мкм фагоцитозу |
частицы полиметилметакрилата (PMMA) [9], фраг- |
не подвержены [24], при размере частиц менее |
менты гидроксиэтилметакрилата и этилметакри- |
20 мкм фагоцитоз становится возможен, но его ин- |
лата (HEMA/EMA) [10, 11], на основе полиакрил- |
тенсивность зависит от формы частиц (она важна |
амидного гидрогеля (PAAG) [12], полиалкилими- |
для распознавания фагоцитами и их эффективного |
да (PAIG) [13], силикона [14, 15] и имеющие другие, |
прикрепления) [25] и гидрофильности. Гидрофиль- |
более редко встречающиеся синтетические соста- |
ные частицы в меньшей степени подвержены фаго- |
вы и их комбинации [16]. Филлеры из этой группы |
цитозу, но они приобретают гидрофобные свойства |
вызывают в месте введения хроническую реакцию |
в случае их опсонизации [24]. |
на инородное тело со стимуляцией соединительной |
Реакция на инородное тело включает стадии вос- |
ткани и иммунной системы, что может обусловли- |
паления и заживления поврежденной ткани, однако |
вать возникновение тяжелых отсроченных нежела- |
в ряде случаев происходит образование гигантских |
тельных явлений [17]. Несмотря на то, что произ- |
клеток инородных тел (ГКИТ) [21, 26]. Возникнове- |
водство и применение в сфере эстетической меди- |
ние ГКИТ связано с большим размером частиц инъе- |
Таблица 1. Обзор основных видов филлеров в настоящее время и в ретроспективе [1]
Биоразлагаемость/долговечность |
Основное действующее вещество |
Длительность присутствия в тканях |
Временные |
Коллаген (в виде филлера уже не используется), |
6—24 мес |
|
гиалуроновая кислота |
|
Полупостоянные |
Полимолочная кислота, гидроксиапатит кальция |
12—36 мес |
(биостимулирующие) |
(CaHA), поликапролактон (PCL) |
|
Постоянные |
Силикон, полиалкилимидный гель (PAIG), |
Неопределенное время |
|
полиакриламидный гель (PAAG), HEMA/EMA |
|
|
(частицы гидроксиэтилметакрилата |
|
|
и этилметакрилата в гиалуроновой кислоте) и др. |
|
68 |
Пластическая хирургия и эстетическая медицина 2023, № 1 |

Обзор Review
Таблица 2. Структурные свойства филлеров и их иммунологическое действие при имплантации в кожу и мягкие ткани [23, 24]
Структурные свойства |
Иммунологический эффект / тканевая реакция |
|
Электрический заряд |
Положительно заряженные частицы |
Привлечение и/или активирование макрофагов |
Отрицательно заряженные частицы |
Отталкивание некоторых отрицательно заряженных бактерий |
|
Особенность поверхности микрочастиц |
Неровная поверхность |
Длительная воспалительная реакция |
Гладкая поверхность |
Формирование фиброзной капсулы вокруг материала |
|
Размер частицы |
Крупные частицы (>20 мкм) |
Не фагоцитируются |
Мелкие частицы (<20 мкм) |
Быстрый фагоцитоз на фоне выраженной местной воспалительной реакции |
|
Гидрофильность/гидрофобность |
Гидрофильные полимерные гели |
Высокая биосовместимость |
Гидрофобные полимерные гели |
Способствуют абсорбции фибронектина и, следовательно, клеточной адгезии, |
|
тем самым стимулируя провоспалительную реакцию |
цированного филлера, вследствие чего их фагоцитоз |
Акрилаты: полиметилметакрилат, |
макрофагами становится невозможен. Гигантские |
гидроксиэтилметакрилат |
клетки и связанная с ними повышенная активность |
и этилметакрилат |
фибробластов обычно исчезают к 6 мес с момента |
|
имплантации филлера [27]. Таким образом, удале- |
Полиметилметакрилат (PMMA) входит в состав |
ние из тканей биорезорбируемых филлеров проис- |
филлера, который состоит на 25% из гладких микро- |
ходит за счет ферментативной биодеградации и фа- |
сфер PMMA, взвешенных в растворе частично де- |
гоцитоза [17, 28]. |
натурированного бычьего коллагена (75%) [31, 32]. |
Несмотря на абсолютную популярность филле- |
В течение 1—3 мес после введения филлера коллаген |
ров на основе гиалуроновой кислоты, в случае воз- |
подвергается ферментативной биодеградации и вы- |
никновения осложнений, особенно отсроченных |
ведению. Сначала он замещается грануляционной |
воспалительных реакций (ОВР), возникает перво- |
тканью, а затем волокнистой соединительной тка- |
очередная необходимость достоверного определе- |
нью. Микросферы действуют как постоянный сти- |
ния вида введенного наполнителя, что напрямую |
мул для фибробластов, это в конечном счете приво- |
определяет тактику лечения и его прогноз. Разно- |
дит к тому, что с течением времени 80% объема в зоне |
образие физико-химических свойств филлеров об- |
имплантации составляет собственная соединительная |
условливает различия и особенности их поведения |
ткань пациента, замещающая коллаген введенного |
в тканях, в том числе специфические гистологиче- |
филлера. Таким образом поддерживается продолжи- |
ские [29] и ультразвуковые признаки. Это определяет |
тельный эффект эстетической коррекции [9, 32, 33]. |
необходимость глубокой информированности врача |
Встречаются и другие модификации данного типа |
об особенностях каждого вида филлеров. |
имплантатов, схожие по свойствам, поведению в тка- |
|
нях и возможным нежелательным явлениям, где в ка- |
Постоянные (синтетические) филлеры |
честве жидкой основы применяется гиалуроновая |
кислота. В некоторых филлерах акрилаты представ- |
|
|
лены гидрофильными частицами из гидроксиэтил- |
На сегодняшний день применение этой группы |
метакрилата (HEMA) и этилметакрилата (EMA) [11]. |
филлеров в большинстве стран крайне ограниченно, |
Первоначальные отчеты заявляли о хорошем уровне |
многие из них запрещены к применению или сня- |
переносимости данного типа филлеров, но вскоре |
ты с производства. Тем не менее, с учетом их пер- |
стало очевидно, что они вызывают поздние грануле- |
манентного присутствия в тканях, они продолжа- |
мы в большом проценте случаев [34—36]. Также счи- |
ют вызывать тяжелые нежелательные явления даже |
талось, что имплантаты данного типа не мигрируют, |
спустя годы после их инъецирования [30]. Многие |
однако в последующем был описан случай отдален- |
из них содержат химически сходные или даже иден- |
ного перемещения из зоны введения [33]. |
тичные агенты, которые могут различаться лишь |
К осложнениям введения микросфер PMMA от- |
формой и размерами частиц, но при этом характе- |
носят формирование уплотнений, узелков, видимой |
ризуются очень вариативными профилями неблаго- |
поверхностной сосудистой сети в течение 3—24 мес |
приятного воздействия [16]. Наиболее распростра- |
и более после инъекции [9, 27, 31, 37—39]. Иссле- |
ненными представителями данной группы являются |
дования in vitro показали, что микросферы PMMA |
филлеры на основе полиметилметакрилата, гидрок- |
могут вызывать первичную иммуноопосредован- |
сиэтилметакрилата/этилметакрилата, полиакрила- |
ную реакцию на инородное тело с активацией ма- |
мида, полиалкилимида, полидиметилсилоксана. |
крофагов и запуском Т-клеточного сигнального ка- |
Plastic surgery and aesthetic medicine 2023, no 1 |
69 |
Обзор Review
скада [40, 41]. А, так называемые, стабильные гранулемы, не проявляющиеся клинически в течение долгого времени, внезапно могут трансформироваться в прогрессирующую гранулематозную реакцию на PMMA с выраженной клинической манифестацией [41, 42]: сначала постепенно, в течение нескольких недель, и примерно в одно и то же время на всех участках введения филлера появляется легкое воспаление, затем происходит формирование узелков, они становятся видимыми, твердыми при пальпации, присоединяется эритема с застойно-цианотич- ным оттенком с выраженным усилением рисунка капиллярной сети на их поверхности [27].
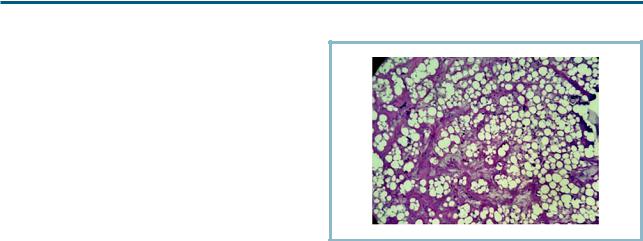
Гистопатология характеризуется наличием пу- |
Рис. 1. Гистологическая картина гранулематозной реакции в от- |
стых круглых вакуолей в местах присутствия частиц |
вет на введение PMMA: сферические частицы филлера в окруже- |
PMMA (растворенных спиртом в процессе подго- |
нии гигантских клеток инородных тел, лимфоцитарного инфиль- |
трата и соединительной ткани с признаками гиалинизации, ×4 [42]. |
|
товки образцов) [41, 42] (рис. 1). Ткань между ними |
|
представлена множеством многоядерных гигантских |
|
клеток и макрофагов, большим количеством фибро- |
|
бластов и коллагеновых волокон. Иногда наблюда- |
стицы начинают разлагаться после многих лет при- |
ются лимфоцитарные инфильтраты и эпителиоид- |
сутствия в тканях человека. Края акриловых частиц |
ные клетки [27]. В некоторых случаях отмечаются |
становятся неровными и «лохматыми», визуализи- |
участки некротизации. Помимо этого, может про- |
руясь в виде ободков, имеющих другую электронную |
исходить удлинение эпидермальных гребней в об- |
плотность, чем центральные части частиц. Высказы- |
ласти инородного материала, что приводит к обра- |
ваются предположения, что ОВР могут вызвать либо |
зованию свищей. Некоторые гранулемы со време- |
акриловые мономеры, высвобождаемые распадаю- |
нем становятся склеротическими [39]. Постепенно |
щимся полимером, либо неровные края частиц [49]. |
может развиться фистуляция, иногда наблюдается |
Однако, несмотря на возможные осложнения, дан- |
кератоакантомоподобный вид [43]. У некоторых па- |
ный вид препаратов до сих пор рекомендуется рядом |
циентов происходит изменение цвета кожи (обесцве- |
авторов для проведения эстетической коррекции раз- |
чивание) и формирование телеангиэктазий или воз- |
личных зон лица [50, 51]. |
никает отечный склероз дермы, окружающей введен- |
|
ный материал [44]. |
Полиакриламидный гель |
Размер и форма частиц в составе перманентных |
|
филлеров, по-видимому, играют определенную роль |
|
в возникновении воспалительных реакций. Было от- |
Полиакриламидный гель (PAAG) представляет со- |
мечено, что частицы с зазубренными краями, по- |
бой прозрачную гидрогелевую субстанцию, состоя- |
лигональной формы и меньших размеров (менее |
щую из 95% воды и 5% полиакриламидного полимера. |
20 мкм) чаще вызывают гиперактивный иммунный |
Использование PAAG в качестве инъекционного им- |
ответ, чем крупные, сферические частицы с гладкой |
плантата началось еще в 1983 г. [27]. Его широко при- |
поверхностью [45]. Интересно, что выраженность |
меняли в эстетической хирургии и косметологии [52] |
ранней тканевой реакции не является показателем |
для коррекции объема молочных желез, ягодиц и икр, |
скорости образования гранулемы. Гидрофильные |
а также при липодистрофии лица, врожденных поро- |
акрилатные гели после инъекции вызывают мини- |
ках развития и косметических недостатках. |
мальную реакцию на инородное тело, но впослед- |
Сообщается, что период полураспада PAAG в ор- |
ствии оказалось, что в более поздние сроки проис- |
ганизме человека может составлять более 20 лет [17]. |
ходит возникновение ОВР [46] с высокой частотой |
Несмотря на то, что гель исходно обладает высокой |
(1,2% случая на 1000 пациентов) [11]. По данным |
биосовместимостью [53] и удовлетворительной пе- |
еще более поздних исследований (2015 г.), частота |
реносимостью, в процессе его применения отмече- |
гранулем составила 1,7% (17 из 1008 пациентов) [47]. |
но развитие множества серьезных нежелательных |
В публикации 2018 г. приводятся данные о возник- |
явлений, таких как отек, абсцессы, обезображива- |
новении гранулем с частотой в пределах 0,02—2,5% |
ние лица, дислокация геля и респираторный ди- |
в зависимости от наименования филлера, содержа- |
стресс-синдром [54—58]. Основным риском являет- |
щего PMMA [48]. |
ся развитие позднего инфекционного процесса, ко- |
На электронных микрофотографиях иссеченных |
торый часто манифестирует через 8—12 мес после |
кожных гранулем не обнаруживаются признаки бак- |
инъекции или даже в более поздние сроки, что может |
териальных биопленок. Показано, что акриловые ча- |
стать причиной формирования абсцессов и некрозов. |
70 |
Пластическая хирургия и эстетическая медицина 2023, № 1 |
Обзор |
Review |
|
|
|
|
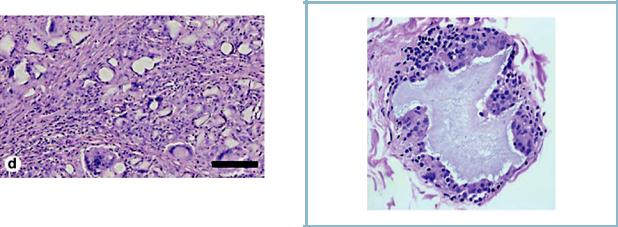
Рис. 2. Гранулематозная реакция на PAAG: гистиоциты и гигантские клетки инородных тел, лимфоцитарная инфильтрация, фибробласты.
Введенный гель визуализируется в виде аморфной базофильной субстанции, в том числе в составе гигантских клеток инородных тел (полоска внизу — 10 мкм) [61].
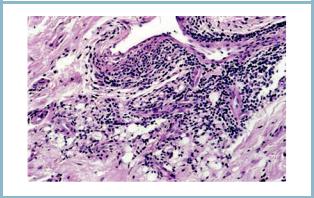
Рис. 3. Гистопатология иссеченной ткани. Гранулематозная реакция: слияние PAIG с окружающим его скоплением эпителиоидных клеток и гигантских клеток инородных тел, ×400 [65].
Предполагается, что фактором развития гранулематозного процесса является склонность к формированию биопленок вокруг PAAG [27, 59]. При этом культуральный анализ часто остается отрицательным, а бактерии идентифицируются только с помощью полимеразной цепной реакции (ПЦР). Типично выявление Propionibacterium acnes, Streptococcus oralis, Streptococcus mirabilis и Staphylococcus aureus, которые в обычных условиях не являются патогенными, а также атипичных микобактерий [60].
Поскольку PAAG обладает высокой исходной биосовместимостью и не вызывает врастания тканей или образования капсул, со временем может происходить его миграция (например, смещение от лица к шее, от груди к паху, от ягодиц к коленной впадине), особенно у пациентов с рыхлой соединительной тканью [27].
Гранулемы PAAG [61] (рис. 2), как правило, относятся к воспалительному или отечному типу. Процесс их формирования начинается, когда в месте локализации филлера отмечается присутствие базофильных мононуклеарных и гигантских клеток, а также происходит формирование тонкой капсулы. Далее следует серозная стадия с накоплением жидкости внутри капсулы и последующим нарастанием давления, боли и отека окружающих тканей. Периваскулярные и очаговые скопления лимфоидных клеток формируют своеобразный барьер вокруг гелевых частиц, что совместно с макрофагами, их фагоцитирующими, впоследствии может вызвать образование стерильного абсцесса и некроза [62].
Для гистологической картины гранулем PAAG характерны озера аморфного внеклеточного базофильного материала, не имеющего двойного лучепреломления, окрашивающегося альциановым синим [29] и похожего по внешнему виду на гиалуроновую кислоту. Гистологическая дифференциация между гиалуроновой кислотой и PAAG может вызы-
вать определенные трудности, поскольку оба филлера имеют вид аморфного базофильного материала. Тем не менее окрашивание альциановым синим слабо положительно с PAAG и сильно положительно с гиалуроновой кислотой, а гранулемы гиалуроновой кислоты обычно включают менее плотный воспалительный инфильтрат, чем гранулемы PAAG [63].
Полиалкилимидный гель
Филлеры на основе полиалкилимида (PAIG) содержат 96% воды и 4% полиалкилимида. Перманентный характер PAIG определяется химической стабильностью и устойчивостью к гидролизу. После инъекции вокруг филлера образуется тонкая волокнистая капсула, которая отделяет его от окружающих тканей, что, как предполагалось, предотвращает миграцию [64]. Тем не менее миграция данного материала является типичным осложнением, о котором сообщалось в многочисленных публикациях [65, 66]. Другими нежелательными явлениями являются отеки, узелки, инфекция, тяжелые воспалительные реакции и отсроченные абсцессы [66].
Гистологически PAIG представлен базофильным аморфным материалом, окруженным нейтрофилами. Окраска по Граму и культуральное исследование может выявить бактерии [67, 68]. При формировании гранулемы отмечается присутствие эпителиоидных клеток и ГКИТ [65] (рис. 3).
Силикон
Термин «силикон» был введен в начале 1900-х годов для описания большого семейства синтетических полимеров, содержащих кремний. Это универсаль-
Plastic surgery and aesthetic medicine 2023, no 1 |
71 |
Обзор |
Review |
ный материал, который часто применяется в биомедицинских целях. Его первое использование в эстетических целях датируется 1940-ми годами, когда он был введен для увеличения груди [69]. Медицинское силиконовое масло, «жидкий силикон 350 cS» (позже известный как Biopolimero-350) широко применялись для увеличения груди, а впоследствии и для коррекции лица.
Вязкость этих соединений определяется возможностью их полимеризации и сшивания молекул. Они могут существовать в форме твердых веществ (эластомеров), гелей и жидкостей. Научное название жидкого силикона — полидиметилсилоксановая жидкость. Вязкость силиконовых жидкостей измеряется в сантистоксах (cS), где 100 cS — это вязкость воды. Вязкость часто отражается непосредственно
вназваниях наполнителя, например «Адатосил-5000» и «Силикон-1000» [14]. Силикон для введения в ткани был одобрен FDA в 1964 г., но спустя несколько десятилетий запрещен во многих странах в связи с возникновением необратимых тяжелых осложнений [27, 70]. Нежелательные явления после введения силикона подразделяются на местные и системные. К местным относятся невоспалительные узелки (из-за неравномерного распределения введенного материала) и воспалительные узелки (силиконовые гранулемы) [71], сопровождающиеся эритемой и отеком разной степени выраженности. Введение больших объемов силикона может привести к целлюлиту, изъязвлению, абсцессу, некрозу [72]. Основные системные осложнения включают пневмонит, гепатит, острый респираторный дистресс-синдром, миграцию (при использовании силиконового масла пониженной вязкости), рожистоподобные реакции, слепоту, неврологические дисфункции, лимфаденопатию, смерть после непреднамеренного попадания наполнителя в глазные или менингеальные сосуды, ASIA-синдром [72, 73]. Также был зарегистрирован случай развития лимфомы после инъекции силикона [74].
Гранулемы склонны развиваться в разные сроки, иногда через десятилетия после инъекции. Среднее время между введением силикона и появлением симптомов гранулем составляет 5 лет (по данным обзора за 2021 г.) [75], а время между появлением симптомов и постановкой диагноза составляет
всреднем 5,8 мес. Некоторые авторы различают силиконому, состоящую почти исключительно из макрофагов, содержащих мелкие капли силиконового масла, и практически не содержащую воспалительные клетки, и силиконовую гранулему, состоящую из силиконсодержащих макрофагов, лимфоцитов и гигантских клеток [60] (рис. 4). Плотные лимфоцитарные инфильтраты имеют преимущественно периваскулярную локализацию. Макрофаги, нагруженные силиконовыми каплями (картина, напоминающая швейцарский сыр) [27], могут гистологически имитировать липобласты и липосаркому [76].
Рис. 4. Плотные лимфоцитарные инфильтраты вокруг сосудов и мелкие капли силикона (в области нижнего края рисунка), напоминающие мелкие жировые клетки [60].
Также силикон при введении в ткани стимулирует образование вокруг себя тонкостенной фиброзной капсулы, что у пациентов с рыхлой соединительной тканью может привести к дислокации материала вдоль фасциальных пространств при мышечных сокращениях или под действием силы тяжести. Помимо этого, частицы силикона с помощью макрофагов
идругих фагоцитирующих клеток могут, транспортируясь по лимфатическим и кровеносным сосудам, мигрировать далеко от места их введения [72, 77]. По данным обзора за 2021 г. [75], миграция силикона в отдаленные от места введения локации наблюдалась у пациентов в 21% случаев (у 3 из 14 пациентов), в том числе у одного пациента произошла опасная для жизни миграция в легкие.
Клинически силиконовые гранулемы могут появляться внезапно, имитируя аллергическую реакцию, сопровождаются сильным отеком и эритемой, а также множественными неподвижными твердыми узловыми элементами мягкоэластической консистенции. Этому процессу может сопутствовать регионарная лимфаденопатия (увеличение, болезненность лимфоузлов, определяемые при пальпации) [27]. В случаях отека, локализующегося в периоральной области, важно проводить дифференциальную диагностику силиконовой гранулемы и хейлита Мишера, который представляет собой гранулематозный процесс, приводящий к стойкому отеку и увеличению губ [78—80].
Однако силиконовые изделия не являются химически идентичными или эквивалентными друг другу. Их различные формы (например, эластомеры, жидкости, гели), имплантированные в разные анатомические зоны, могут иметь отличающийся друг от друга потенциал осложнений [14]. Существуют различные теории этиопатогенеза возникновения силиконовых гранулем. D.P. Friedmann
исоавт. считают, что биопленки играют ведущую роль в формировании силиконовых гранулем в связи с тем, что силиконовые частицы имеют поверх-
72 |
Пластическая хирургия и эстетическая медицина 2023, № 1 |
Обзор Review
ность, свойства которой позволяют микроорганизмам легко к ней прикрепляться. Для их идентификации они предложили использовать ПЦР-тесты [81]. В другом исследовании было продемонстрировано, что иммунный ответ на силиконовые материалы значительно усиливается дополнительными антигенами, которые входят в их состав в виде различных примесей [19].
Силиконовые гранулемы имеют много общего с кожным саркоидозом, и понимание роли иммунологического процесса при этом заболевании может способствовать лучшему пониманию их патогенеза [82]. Интересно отметить, что, как и при саркоидозе, осложнения после введения силикона могут возникнуть на фоне постоянной антигенной сти-
муляции, что инициирует каскад воспалительных |
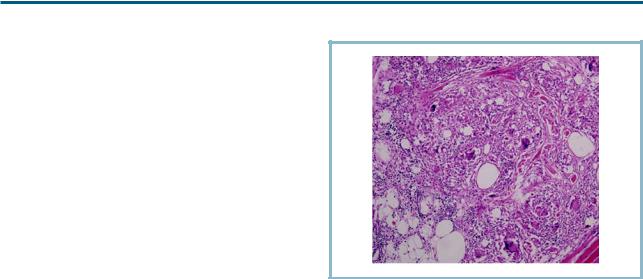
Рис. 5. Гистопатологическая картина парафиновой гранулемы: |
|
реакций. В этом процессе предполагается участие |
включения наполнителя в виде, напоминающем швейцарский |
|
Toll-подобных рецепторов [14]. Несмотря на воз- |
сыр (вакуоли разных размеров), окруженные гигантскими клет- |
|
можные осложнения при инъецировании силиконо- |
ками и макрофагами, ×100 [88]. |
|
вых наполнителей, их низкая стоимость и стойкость |
|
|
эстетической коррекции по-прежнему определяют |
Инъекция парафина приводит к образованию |
|
их применение в ряде стран, в том числе в нелегаль- |
склерозирующей липогранулемы (парафиномы), ха- |
|
ной косметологии. Например, неоднократно отмеча- |
рактеризующейся фиброзом и деформацией [87]. |
|
лись случаи проведения инъекций силикона под ви- |
Вазелин и минеральные масла вызывают схожую |
|
дом наполнителя на основе гиалуроновой кислоты, |
реакцию тканей [84—86]. Гистологически склеро- |
|
в связи с чем при возникновении осложнений вве- |
зирующая липогранулема (рис. 5) характеризуется |
|
денные в заблуждение пациенты сообщают невер- |
наличием множественных кистозных пространств |
|
ные сведения [72]. Врачам необходимо учитывать |
различного диаметра (вид, напоминающий швейцар- |
|
это обстоятельство и применять дополнительные ме- |
ский сыр), расположенных на фоне склерозирован- |
|
тоды диагностики. |
ных коллагеновых пучков с присутствием лимфоци- |
|
|
тов, макрофагов, эпителиоидных и гигантских кле- |
|
Минеральные масла, парафин, |
ток. Клинические и гистологические особенности |
|
этих гранулем аналогичны клиническим и гистоло- |
||
медицинский вазелин, |
гическим особенностям силиконовых гранулем [88]. |
|
жирорастворимые витамины |
Инъекции масляных растворов витамина Е да- |
|
ют аналогичную гистопатологическую картину, но, |
||
|
||
Вазелин, парафин, ланолин, рыбий жир, пче- |
поскольку в настоящее время они нелегально при- |
|
линый воск широко использовались для коррекции |
меняются прежде всего в области лица (чаще всего |
|
эстетических недостатков в конце XIX и начале XX |
для увеличения объема губ), патологические изме- |
|
века. Несмотря на то, что первоначальный резуль- |
нения имеют гораздо более острый характер и вос- |
|
тат казался удовлетворительным, отдаленные по- |
палительный компонент в этих случаях более очеви- |
|
следствия были катастрофическими: воспаление, |
ден [16, 88—93]. Сам маслянистый материал может |
|
отек, образование гранулем, изъязвление, абсцеди- |
быть потерян во время обработки и подготовки об- |
|
рование, присоединение инфекций, уплотнение ко- |
разца ткани для гистологического исследования [91]. |
|
жи, обезображивание лица и даже онкология [83]. |
Использование масел для эстетической коррекции |
|
Первые описания побочных эффектов были опу- |
сопровождается возникновением таких нежела- |
|
бликованы еще в 1906 г., они характеризовались воз- |
тельных явлений, как липогранулема, выраженное |
|
никновением уродующих подкожных узелков у двух |
уплотнение кожи, ее деформация, изъязвление и по- |
|
пациентов, которым ввели парафин для коррекции |
явление локальной гиперпигментации в месте инъ- |
|
мимических морщин. Побочные эффекты парафи- |
екции. Жирорастворимым витаминам необходимо |
|
на необратимы, поэтому он больше не используется |
масло в качестве основы, например стерильное ара- |
|
в эстетической медицине. Однако до сих пор неодно- |
хисовое или соевое. Предполагается, что осложнения |
|
кратно встречаются случаи возникновения воспали- |
являются результатом взаимодействия тканей имен- |
|
тельных гранулем после нелегального или самосто- |
но с маслянистым растворителем, а не с самим вита- |
|
ятельного введения вазелинового масла, парафина |
мином [89, 93]. Возникновение липогранулемы мо- |
|
или маслянистых растворов, содержащих витамин |
жет также определяться количеством введенного ма- |
|
Е, а также витамины D и А [83—86]. |
териала и его иммуногенностью [89]. |
Plastic surgery and aesthetic medicine 2023, no 1 |
73 |

Обзор Review
Таким образом, перманентные филлеры харак- |
ки каждого вида филлеров для повышения точности |
теризуются не только стойкостью и долговременно- |
диагностики, назначения адекватного лечения и пла- |
стью эстетического эффекта, но и характерными из- |
нирования последующей косметологической тера- |
менениями в тканях с высокой степенью вероятно- |
пии с учетом соответствующего анамнеза. |
сти развития отсроченных воспалительных реакций, |
|
носящих тяжелый, хронический характер. Имен- |
Авторы заявляют об отсутствии конфликта интересов. |
но поэтому врачам необходимо знать характеристи- |
The authors declare no conflicts of interest. |
ЛИТЕРАТУРА/REFERENCES
1.Bachour Y, Kadouch JA, Niessen FB. The aetiopathogenesis of late inflammatory reactions (lirs) after soft tissue filler use: A systematic review of the literature. Aesthetic Plast Surg. 2021;45(4):1748-1759. https://doi.org/10.1007/s00266-021-02306-3
2.Marinelli E, Montanari Vergallo G, Reale G, di Luca A, Catarinozzi I, et al. The role of fillers in aesthetic medicine: medico-legal aspects. Eur Rev Med Pharmacol Sci. 2016;20(22):4628-4634.
3.Di Girolamo M, Mattei M, Signore A, Grippaudo FR. MRI in the evaluation of facial dermal fillers in normal and complicated cases. Eur Radiol. 2015;25(5):1431-1442.
https://doi.org/10.1007/s00330-014-3513-2
17.Lemperle G, Morhenn V, Charrier U. Human histology and persistence of various injectable filler substances for soft tissue augmentation. Aesthet Plast Surg. 2003;27:354-366.
https://doi.org/10.1007/s00266-003-3022-1
18.Chen F, Carruthers A, Humphrey S, Carruthers J. HIV-associated facial lipoatrophy treated with injectable silicone oil: A pilot study. Dermatol Surg. 2013;69:431-437.
https://doi.org/10.1016/j.jaad.2013.03.025
19.Prather CL, Jones DH. Liquid injectable silicone for soft tissue augmentation. J Am Acad Dermatol. 2006;19:159-168. https://doi.org/10.1111/j.1529-8019.2006.00070.x
4.Rohrich RJ, Nguyen AT, Kenkel JM. Lexicon for soft tissue implants. Der- 20. Herrmann JL, Hoffmann RK, Ward CE, Schulman JM, Grekin RC. Bio-
matol Surg. 2009;35:1605-1611. https://doi.org/10.1111/j.1524-4725.2009.01337.x
5.Smith KC. Reversible vs. Nonreversible fillers in facial aesthetics: concerns and considerations. Dermatol Online J. 2008;14:3. https://doi.org/10.5070/D325v7q60x
6.Sherman RN. Sculptra: The new three-dimensional filler. Clin Plast Surg. 2006;33:539-550.
https://doi.org/10.1016/j.cps.2006.09.001
7.Shumaker PR, Sakas EL, Swann MH, Greenway HT Jr. Calcium hydroxylapatite tissue filler discovered 6 years after implantation into the nasolabial fold: case report and review. Dermatol Surg. 2009;35:375-379. https://doi.org/10.1111/j.1524-4725.2008.01050.x
8.Kim JS, In CH, Park NJ, Kim BJ, Yoon HS. Comparative study of rheological properties and preclinical data of porous polycaprolactone microsphere dermal fillers. J Cosmet Dermatol. 2020;19(3):596-604. https://doi.org/10.1111/jocd.13076
9.Lemperle G, Romano JJ, Busso M. Soft tissue augmentation with Artecoll: 10-year history, indications, techniques and complications. Dermatol Surg. 2003;29:573-587.
https://doi.org/10.1046/j.1524-4725.2003.29140.x
10.Kadouch JA, Vos W, Nijhuis EW, Hoekzema R. Granulomatous for- eign-body reactions to permanent fillers: detection of CD123+ plasmacytoid dendritic cells. Am J Dermatopathol. 2015;37(2):107-114. https://doi.org/10.1097/DAD.0000000000000239
11.Bergeret-Galley C, Latouche X, Illouz YG. The value of a new filler material in corrective and cosmetic surgery: Dermalive and Dermadeep. Aesthet Plast Surg. 2001;25:249-255.
https://doi.org/10.1007/s002660010131
12.Bello G, Jackson IT, Keskin M, Kelly C, Dajani K, Studinger R, et al. The use of polyacrylamide gel in soft tissue augmentation: an experimental assessment. Plast Reconstr Surg. 2007;119:1326-1336. https://doi.org/10.1097/01.prs.0000254824.13065.3b
13.Lahiri A, Waters R. Experience with Bio-Alcamid, a new soft tissue endoprosthesis. J Plast Reconstr Aesthet Surg. 2007;60:663-667. https://doi.org/10.1016/j.bjps.2006.07.010
14.Narins RS, Beer K. Liquid Injectable Silicone: a review of its history, immunology, technical considerations, complications and potential. Plast Reconstr Surg. 2006;118:77-84. https://doi.org/10.1097/01.prs.0000234919.25096.67
15.Scaranelo AM, de Fátima Ribeiro Maia M. Sonographic and mammographic findings of breast liquid silicone injection. J Clin Ultrasound. 2006; 34:273-277.
https://doi.org/10.1002/jcu.20235
16.Haneke E. Adverse effects of fillers and their histopathology. Facial Plast Surg. 2014;30(6):599-614.
https://doi.org/10.1055/s-0034-1396755
chemistry, physiology, and tissue interactions of contemporary biodegradable injectable dermal fillers. Dermatol Surg. 2018;44(1):19-31. https://doi.org/10.1097/DSS.0000000000001582
21.Anderson JM, Rodriguez A, Chang DT. Foreign body reaction to biomaterials. Semin Immunol. 2008;20(2):86-100. https://doi.org/10.1016/j.smim.2007.11.004
22.Decates T, Kadouch J, Velthuis P, Rustemeyer T. Immediate nor delayed type hypersensitivity plays a role in late inflammatory reactions after hyaluronic acid filler injections. Clin Cosmet Investig Dermatol. 2021;14:581-589. https://doi.org/10.2147/CCID.S312198
23.Morhenn VB, Lemperle G, Gallo RL. Phagocytosis of different particulate dermal filler substances by human macrophages and skin cells. Dermatol Surg. 2002;28(6):484-490. https://doi.org/10.1046/j.1524-4725.2002.01273.x
24.Bentkover SH. The biology of facial fillers. Facial Plast Surg. 2009;25:73-85. https://doi.org/10.1055/s-0029-1220646
25.Champion JA, Mitragotri S. Role of target geometry in phagocytosis. Proc Natl Acad Sci USA. 2006;103:4930-4934. https://doi.org/10.1073/pnas.0600997103
26.Alijotas-Reig J, Fernández-Figueras MT, Puig L. Inflammatory, im- mune-mediated adverse reactions related to soft tissue dermal fillers. Semin Arthritis Rheum. 2013;43(2):241-258. https://doi.org/10.1016/j.semarthrit.2013.02.001
27.Lemperle G, Gauthier-Hazan N, Wolters M, Eisemann-Klein M, Zimmermann U, Duffy DM. Foreign body granulomas after all injectable dermal fillers: part 1. Possible causes. Plast Reconstr Surg. 2009;123(6):1842-1863. https://doi.org/10.1097/PRS.0b013e31818236d7
28.Convery C, Davies E, Murray G, Walker L. Delayed-onset nodules (DONs) and considering their treatment following use of hyaluronic acid (HA) fillers. J Clin Aesthet Dermatol. 2021;14(7):59-67.
29.Dadzie OE, Mahalingam M, Parada M, El Helou T, Philips T, Bhawan J. Adverse reactions to soft tissue fillers — A review of the histological features. J Cutan Pathol. 2008;35:536-548. https://doi.org/10.1111/j.1600-0560.2007.00853.x
30.Manturova NE, Ikonnikova EV, Kruglova LS, Stenko AG. Therapy of delayed granulomatous inflammation after injection of permanent filler. 2020; EADV Virtual Congress. Abstract ID1689. e-poster Number P0452.
31.Thioly-Bensoussan D. Non-hyaluronic acid fillers. Clin Dermatol. 2008; 26(2):160-176.
https://doi.org/10.1016/j.clindermatol.2007.09.017
32.Zimmermann US, Clerici TJ. The histological aspects of fillers complications. Semin Cutan Med Surg. 2004;23(4):241-250. https://doi.org/10.1016/j.sder.2004.09.004
33.Cannata-Ortiz P, Gracia C, Aouad Y, Barat A, Martinez-Gonzalez MA, Rossello G, et al. Small vessel microembolization and acute glomerulonephritis following infection of aesthetic filler implants. Diagn Pathol. 2016;11:2. https://doi.org/10.1186/s13000-016-0453-y
74 |
Пластическая хирургия и эстетическая медицина 2023, № 1 |
Обзор |
Review |
34.Sidwell RU, Dhillon AP, Butler PE, Rustin MH. Localized granulomatous reaction to a semi-permanent hyaluronic acid and acrylic hydrogel cosmetic filler. Clin Exp Dermatol. 2004;29(6):630-632. https://doi.org/10.1111/j.1365-2230.2004.01625.x
53.Zarini E, Supino R, Pratesi G, Laccabue D, Laccabue D, Tortoreto M, et al. Biocompatibility and tissue interactions of a new filler material for medial use. Plast Reconstr Surg. 2004;114:934-942. https://doi.org/10.1097/01.prs.0000133425.22598.d0
35.Angus JE, Affleck AG, Leach IH, Millard LG. Two cases of delayed granu54. Kalantar-Hormozi A, Mozafari N, Rasti M. Adverse effects after use of poly-
lomatous reactions to the cosmetic filler Dermalive, a hyaluronic acid and acrylic hydrogel. Br J Dermatol. 2006;155(5):1077-1078. https://doi.org/10.1111/j.1365-2133.2006.07482.x
36.Rossner M, Rossner F, Bachmann F, Wiest L, Rzany B. Risk of severe adverse reactions to an injectable filler based on a fixed combination of hydroxyethylmethacrylate and ethylmethacrylate with hyaluronic acid. Dermatol Surg. 2009;35(1):367-374. https://doi.org/10.1111/j.1524-4725.2008.01062.x
37.Pollack S. Some new injectable dermal filler materials: Hylaform, Restylane and Artecoll. J Cutan Med Surg. 1999;3(4):27-35.
38.Lemperle G, Gauthier-Hazan N, Lemperle M. PMMA-Microspheres (Artecoll) for long-lasting correction of wrinkles: refinements and statistical results. Aesthetic Plast Surg. 1998;22(5):356-365. https://doi.org/10.1007/s002669900217
39.De Jesus LH, de Campos Hildebrand L, Martins MD, da Rosa FM, Danilevicz CK, Sant’Ana Filho M. Location of injected polymethylmethacrylate microspheres influences the onset of late adverse effects: An experimental and histopathologic study. Clin Cosmet Investig Dermatol. 2015;8:431-436. https://doi.org/10.2147/CCID.S81467
acrylamide gel as a facial soft tissue filler. Aesthet Surg J. 2008;28:139-142. https://doi.org/10.1016/j.asj.2007.12.005
55.Reda-Lari A. Augmentation of the malar area with polyacrylamide hydrogel: Experience with more than 1300 patients. Aesth Surg J. 2008;28:131-138. https://doi.org/10.1016/j.asj.2007.12.004
56.Cheng NX, Wang YL, Wang JH, Zhang XM, Zhong H. Complications of breast augmentation with injected hydrophilic polyacrylamide gel. Aesthetic Plast Surg. 2002;26:375-382.
https://doi.org/10.1007/s00266-002-2052-4
57.Lee CJ, Kim SG, Kim L, Choi MS, Lee SI. Unfavorable findings following breast augmentation using injected polyacrylamide hydrogel. Plast Reconstr Surg. 2004;114:1967-1968. https://doi.org/10.1097/01.prs.0000143922.64916.b3
58.Даненков А.С., Николаев Е.В., Бояринцев Н.И. Поздние осложнения после аугментационной пластики молочных желез полиакриламидным гелем. Дальневосточный медицинский журнал. 2011;1:24-26.
Danenkov AS, Nikolaev EV, Boyarintsev NI. Late complications after breast augmentation surgery with polyacrylamide gel. Far Eastern Medical Journal. 2011;1:24-26. (In Russ.).
40.Alijotas-Reig J, Garcia-Gimenez V, Miró-Mur F, Vilardell-Tarrés M. De59. Alhede M, Er Ö, Eickhardt S, Kragh K, Alhede M, Christensen LD, et al.
layed immune-mediated adverse effects of polyalkylimide dermal fillers: clinical findings and long-term follow-up. Arch Dermatol. 2008;144(5):637-642. https://doi.org/10.1001/archderm.144.5.637
Bacterial biofilm formation and treatment in soft tissue fillers. Pathogens and Disease. 2014;70(3):339-346.
https://doi.org/10.1111/2049-632X.12139
41.Lemperle G, Kind P. Biocompatibility of Artecoll. Plast Reconstr Surg. 60. Haneke E. Managing Complications of Fillers: Rare and Not-So-Rare.
1999;103:338-340. https://doi.org/10.1097/00006534-199901000-00079
42.Goldman A, Wollina U. Intralesional Neodymium YAG laser to Treat Complications of Polymethylmethacrylate. Open Access Maced J Med Sci. 2018; 6(9):1636-1641.
https://doi.org/10.3889/oamjms.2018.348
43.Gamo R, Pinedo F, Vicente J, Naz E, Calzado L, Ruiz-Genao D, et al. Ker- atoacanthoma-like reaction after a hyaluronic acid and acrylic hydrogel cosmetic filler. Dermatol Surg. 2008;34(7):954-959. https://doi.org/10.1111/j.1524-4725.2008.34186.x
44.Requena C, Izquierdo MJ, Navarro M, et al. Adverse reactions to injectable aesthetic microimplants. Am J Dermatopathol. 2001;23(3):197-202. https://doi.org/10.1097/00000372-200106000-00006
45.Wolkow N, Jakobiec FA, Yoon MK. Dermalive facial filler granulomas masquerading as neurofibromas. Ophthalmic Plast Reconstr Surg. 2018;34(3): 99-103.
https://doi.org/10.1097/IOP.0000000000001100
46.Kadouch JA, Kadouch DJ, Fortuin S, van Rozelaar L, Karim RB, Hoekzema R. Delayed-onset complications of facial soft tissue augmentation with permanent fillers in 85 patients. Dermatol Surg. 2013;39(10):1474-1485. https://doi.org/10.1111/dsu.12313
47.Cohen S, Dover J, Monheit G, et al. Five-year safety and satisfaction study of PMMA-collagen in the correction of nasolabial folds. Dermatol Surg. 2015;41(1):302-313.
https://doi.org/10.1097/DSS.0000000000000542
48.Gold MH, Sadick NS. Optimizing outcomes with polymethylmethacrylate fillers. J Cosmet Dermatol. 2018;17(3):298-304. https://doi.org/10.1111/jocd.12539
49.Wiest LG, Stolz W, Schroeder JA. Electron microscopic documentation of late changes in permanent fillers and clinical management of granulomas in affected patients. Dermatol Surg. 2009;35(2):1681-1688. https://doi.org/10.1111/j.1524-4725.2009.01347.x
50.Hevia O. Safety and efficacy of polymethylmethacrylate-collagen gel filler for correction of the pre-jowl sulcus: A 24-month prospective study. Aesthet Surg J Open Forum. 2022;4:ojac030. https://doi.org/10.1093/asjof/ojac030
51.Katz B, Lehman A, Misev V, Vachon G, Saeed S. A 12-month study to evaluate safety and efficacy of polymethylmethacrylate-collagen gel for correction of midface volume loss using a blunt cannula as measured by 3-D imaging. Dermatol Surg. 2021;47(3):365-369. https://doi.org/10.1097/DSS.0000000000002809
52.Christensen LH, Breiting VB, Aasted A, Jørgensen A, Kebuladze I. Longterm effects of polyacrylamide hydrogel on human breast tissue. Plast Reconstr Surg. 2003;111(6):1883-1890. https://doi.org/10.1097/01.PRS.0000056873.87165.5A
J Cutan Aesthet Surg. 2015;8(4):198-210. PMID: 26865784; PMCID: PMC4728901.
https://doi.org/10.4103/0974-2077.172191
61.Park K, Nishiwaki F, Kabashima K, Miyachi Y. A Case of Foreign-Body Granuloma of the Glabella due to Polyacrylamide Filler and an Intractable Ulcer after Skin Biopsy: An Immunohistochemical Evaluation of Inflammatory Changes. Case Rep Dermatol. 2013;5(2):181-185. https://doi.org/10.1159/000353346
62.Адамян А.А., Светухин А.М., Скуба Н.Д. и др. Полиакриламидный маммарный синдром: клиника, диагностика и лечение. Анналы пластической, реконструктивной и эстетической хирургии. 2001;4:20-32.
Adamyan AA, Svetukhin AM, Skuba ND, et al. Polyacrylamide mammary syndrome: Clinical features, diagnosis and treatment. Annaly plasticheskoj, rekonstruktivnoj i esteticheskoj khirurgii. 2001;4:20-32. (In Russ.).
63.Rongioletti F, Atzori L, Ferreli C, Pau M, Pinna AL, Mercuri SR, et al. Granulomatous reactions after injections of multiple aesthetic micro-im- plants in temporal combinations: A complication of filler addiction. J Eur Acad Dermatol Venereol. 2015;29(6):1188-1192. https://doi.org/10.1111/jdv.12788
64.Ramires PA, Miccoli MA, Panzarini E, Dini L, Protopapa C. In vitro and in vivo biocompatibility evaluation of a polyalkylimide hydrogel for soft tissue augmentation. J Biomed Mater Res — Part B Appl Biomater. 2005;72(2): 230-238. https://doi.org/10.1002/jbm.b.30157
65.AlHarbi ZA, Alkatan HM, Alsuhaibani AH. Long-term outcomes of surgically removed migrated polyalkylimide (bio-alcamid) filler to the periorbital area. Saudi J Ophthalmol. 2019;33(3):251-254. https://doi.org/10.1016/j.sjopt.2019.06.001
66.Malik S, Mehta P, Adesanya O, Ahluwalia HS. Migrated periocular filler masquerading as arteriovenous malformation: A diagnostic and therapeutic dilemma. Ophthal Plast Reconstr Surg. 2013;29:18-20. https://doi.org/10.1097/IOP.0b013e31825b34db
67.Jones DH, Carruthers A, Fitzgerald R, Sarantopoulos GP, Binder S. Lateappearing abscesses after injections of nonabsorbable hydrogel polymer for HIV-associated facial lipoatrophy. Dermatol Surg. 2007;33(2):193-198. https://doi.org/10.1111/j.1524-4725.2007.33360.x
68.Goldan O, Georgio I, Grabov-Nardini G, Regev E, Tessone A, Liran A, et al. Early and late complications after a nonabsorbable hydrogel polymer injection: A series of 14 patients and novel management. Dermatol Surg. 2007; 33(2):199-206.
https://doi.org/10.1111/j.1524-4725.2007.33361.x
69.Kontis TC, Rivkin A. The history of injectable facial fillers. Facial Plast Surg. 2009;25(2):67-72.
https://doi.org/10.1055/s-0029-1220645
70.FDA warns about illegal use of injectable silicone for body contouring and associated health risks. 2017. https://www.fda.gov/news-events/press-announcements/fda-warns-about- illegal-use-injectable-silicone-body-contouring-and-associated-health-risks
Plastic surgery and aesthetic medicine 2023, no 1 |
75 |
Обзор |
Review |
71.Liu A, Hoss E, Kollipara R, Goldman MP. Granulomatous reaction to silicone filler injections on the glabella and nasolabial folds. Dermatol Surg. 2021;47(6):851-853.
https://doi.org/10.1097/DSS.0000000000002707
72.Wang LL, Thomas WW, Friedman O. Granuloma formation secondary to silicone injection for soft-tissue augmentation in facial cosmetics: Mechanisms and literature review. Ear Nose Throat J. 2018;97(1-2):46-51. https://doi.org/10.1177/0145561318097001-211
73.Alijotas-Reig J, Esteve-Valverde E, Gil-Aliberas N, Garcia-Gimenez V. Autoimmune/inflammatory syndrome induced by adjuvants-ASIA-related to biomaterials: analysis of 45 cases and comprehensive review of the literature. Immunol Res. 2018;66(1):120-140. https://doi.org/10.1007/s12026-017-8980-5
74.Lee SH, Kim HC, Kim YJ. B-cell lymphoma in a patient with a history of foreign body injection. J Craniofac Surg. 2017;28(2):504-505.
75.Kassamali B, Kus KJB, Min MS, et al. Characteristics and treatment of silicone granulomas: A retrospective multicenter cohort of 21 patients. JAAD Int. 2021;3:111-114.
https://doi.org/10.1016/j.jdin.2021.03.007
76.Gonçales ES, dos Santos Almeida A, Soares S, Oliveira DT. Silicone implant for chin augmentation mimicking a low-grade liposarcoma. Oral Surg Oral Med Oral Pathol Oral Radiol. 2009;107(4):21-23. https://doi.org/10.1016/j.tripleo.2008.12.044
77.Соловьева Е.П., Муслимов С.А., Гурьянов А.С. Клинико-морфологи- ческие изменения кожи после инъекционной контурной пластики губ силиконом и гиалуроновой кислотой. Клиническая дерматология
и венерология. 2015;14(5):166-169.
Solovieva EP, Muslimov SA, Guryanov AS. Clinical and morphological changes of the skin after injectable lip contouring with silicone and hyaluronic acid. Clinical Dermatology and Venereology. 2015;14(5):166-169. (In Russ.). https://doi.org/10.17116/klinderma2015145166-169
78.Requena C, Requena L, Alegre V, et al. Adverse reaction to silicone simulating orofacial granulomatosis. J Eur Acad Dermatol Venereol. 2015;29(5): 998-1001.
https://doi.org/10.1111/jdv.12522
79.Shams MG, Motamedi MHK, Azizi T. Orofacial granulomatosis of the lower lip and cheek: Report of a case. Oral Surg Oral Med Oral Pathol Oral Radiol. 2007;104(4):42-44.
https://doi.org/10.1016/j.tripleo.2007.05.012
80.Иконникова Е.В., Круглова Л.С., Мантурова Н.Е., Щекочихин В.А. Гранулематозный хейлит Мишера или отсроченный воспалительный отек верхней губы после введения филлера: трудности дифференциальной диагностики. Фарматека. 2021;28(14):8-11.
Ikonnikova EV, Kruglova LS, Manturova NE, Shchekochikhin VA. Mischer’s granulomatous cheilitis or delayed inflammatory edema of the upper lip after filler injection: difficulties of differential diagnosis. Farmateka. 2021; 28(14):8-11. (In Russ.). https://doi.org/10.18565/pharmateca.2021.14.00-00
81.Friedmann DP, Kurian A, Fitzpatrick RE. Delayed granulomatous reactions to facial cosmetic injections of polymethylmethacrylate microspheres
and liquid injectable silicone: A case series. J Cosmet Laser Ther. 2016;18(3): 170-173.
https://doi.org/10.3109/14764172.2015.1114642
82.Pimentel L, Barnadas M, Vidal D, Sancho F, Fontarnau R, Alomar A. Simultaneous presentation of silicone and silica granuloma: A case report. Dermatology. 2002;205(2):162-165.
https://doi.org/10.1159/000063897
83.Glicenstein J. Les premiers «fillers», vaseline et paraffine. Du miracle à la catastrophe [The first “fillers”, vaseline and paraffin. From miracle to disaster]. Ann Chir Plast Esthet. 2007;52(2):157-161. (In French). https://doi.org/10.1016/j.anplas.2006.05.003
84.Hohaus K, Bley B, Köstler E, Schönlebe J, Wollina U. Mineral oil granuloma of the penis. J Eur Acad Dermatol Venereol. 2003;17:585-587. https://doi.org/10.1046/j.1468-3083.2003.00896.x
85.Akkus E, Iscimen A, Tasli L, Hattat H. Paraffinoma and ulcer of the external genitalia after self-injection of vaseline. J Sex Med. 2006;3:170-172. https://doi.org/10.1111/j.1743-6109.2005.00096.x
86.Nyirady P, Kelemen Z, Kiss A, Bánfi G, Borka K, Romics I. Treatment and outcome of vaseline-induced sclerosing lipogranuloma of the penis. Urology. 2008;71:1132-1137.
https://doi.org/10.1016/j.urology.2007.12.081
87.Downey AP, Osman NI, Mangera A, Inman RD, Reid SV, Chapple CR. Penile Paraffinoma. Eur Urol Focus. 2019;5(5):894-898. https://doi.org/10.1016/j.euf.2018.06.013
88.Lee JM, Kim YJ. Foreign body granulomas after the use of dermal fillers: pathophysiology, clinical appearance, histologic features, and treatment. Arch Plast Surg. 2015;42(2):232-239. https://doi.org/10.5999/aps.2015.42.2.232
89.Kamouna B, Kazandjieva J, Balabanova M, Dourmishev L, Negentsova Z, Etugov D, et al. Oil soluble vitamins: Illegal use for lip augmentation. Facial Plast Surg. 2014;30:635-643.
https://doi.org/10.1055/s-0034-1396903
90.Foucar E, Downing DT, Gerber WL. Sclerosing lipogranuloma of the male genitalia containing vitamin E: A comparison with classical “paraffinoma”.
J Am Acad Dermatol. 1983;9:103-110. https://doi.org/10.1016/s0190-9622(83)70114-3
91.Ehsani AH, Ansari MS, Ghanadan A, Mehdizade Rayeni N, Noormohammad Poor P, Ansari M. Serious complication as a result of lip augmentation with vitamin E. J Cosmet Dermatol. 2019;18(6):1632-1634. First published: 28 March 2019.
https://doi.org/10.1111/jocd.12926
92.Kamouna B, Litov I, Bardarov E, Broshtilova V, Miteva L, Kazandjieva J. Granuloma formation after oil-soluble vitamin D injection for lip augmentation — case report. J Eur Acad Dermatol Venereol. 2016;30(8):1435-1436. https://doi.org/10.1111/jdv.13277
93.Kamouna B, Darlenski R, Kazandjieva J, et al. Complications of injected vitamin E as a filler for lip augmentation: case series and therapeutic approach. Dermatol Ther. 2015;28(2):94-97.
https://doi.org/10.1111/dth.12203
Поступила 12.10.2022 Received 12.10.2022 Принята к печати 11.11.2022 Accepted 11.11.2022
76 |
Пластическая хирургия и эстетическая медицина 2023, № 1 |
