
6 курс / Гастроэнтерология / Хронический_билиарнозависимый_панкреатит_Казюлин_А_Н_,_Кучерявый
.pdf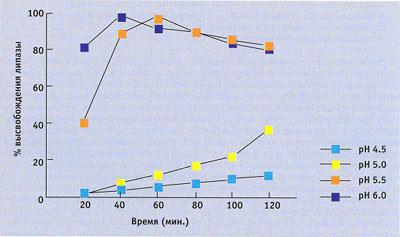
у этих пациентов в патогенезе экзокринной недостаточности более важна, чем при нормальной функции ПЖ. Следует отметить, что у больных алкогольным ХП часто используют панкреатические ферменты с высоким содержанием протеаз для купирования боли, однако, при этом усиливается инактивация эндогенной липазы. Этот факт достаточно часто отмечен в различных публикациях, где анализировались причины низкой эффективности коррекции стеатореи у больных ХП.
Рис. 24. Характеристика растворимости микросфер Креона, выраженные как процент высвобождения липазы от 4,5 до 6,0. (По S.N.Atkinson, 1991с изм.).
Для обеспечения быстрого и гомогенного смешивания ферментов с пищевым химусом, предотвращения внутрижелудочной инактивации и адекватного пассажа из желудка в ДПК были созданы ферментные препараты панкреатина нового поколения в виде микросфер, диаметр которых не превышает 2 мм. Препараты покрыты энтеросолюбильными оболочками и заключены в желатиновые капсулы. При попадании в желудок желатиновые капсулы быстро растворяются, микросферы смешиваются с пищей и постепенно поступают в ДПК. При рН дуоденального содержимого выше 5,5 оболочки растворяются, и ферменты начинают действовать на большой поверхности (Рисунок 25). При этом практически воспроизводятся физиологические процессы пищеварения, когда панкреатический сок выделяется порциями в ответ на периодическое поступление пищи из желудка.
Таким образом, именно микросферические препараты можно отнести к самым современным полиферментным средствам для заместительной ферментной терапии, в том числе отвечающим современным требованиям:
•препараты должны быть животного, преимущественно свиного происхождения;
•содержание достаточного количества ферментов, обеспечивающих полный гидролиз нутриентов в полости ДПК;
•наличие оболочки, защищающей ферменты от переваривания желудочным соком;
•равномерное и быстрое перемешивание с пищей;
•одновременный пассаж ферментов с пищей через привратник в ДПК;
•быстрое освобождение ферментов в верхних отделах тонкой кишки;
•отсутствие желчных кислот в составе препарата;
•безопасность, отсутствие токсичности.
Соответственно, лекарственным средством, полностью удовлетворяющим вышеуказанным требованиям и используемым в последнее время, является полиферментный препарат в виде минимикросфер (Креон 10000 и Креон 25000), покрытых энтеросолюбильной оболочкой. Этот препарат выгодно отличается от аналогичных препаратов других производителей тем, что средний размер минимикросфер уменьшен до 1 мм. Это обеспечивает иную, чем при применении микротаблеток фармакокинетику, способствует оптимальному перемешиванию с пищей и, соответственно, повышает эффективность препарата в среднем на 25%. Решение уменьшить размер микросфер опиралось на результаты исследований J.H.Meyer и соавт., показавших в эксперименте на здоровых добровольцах, что из желудка быстрее эвакуировались микросферы диаметром 1 мм независимо от количества принимаемой с ферментом пищи. Креон также характеризуется оптимальным соотношением активности липазы и колипазы, высоким содержанием карбоксилэстеролипазы и фосфолипазы А2 для наиболее эффективного расщепления жиров.
Побочные эффекты полиферментной терапии возникают нечасто и обычно не носят тяжелого характера. Наиболее показательны в этом отношении исследования H.Friess и соавт. применявших у здоровых добровольцев в течение 4 недель панкреатин в суточной дозе 360000 (!) ЕД липолитической активности. Авторами не только не найдено адаптационных изменений экзо- и эндокринной функции ПЖ, изменений ее размеров, но и не было отмечено существенных побочных эффектов, что лишний раз характеризует препараты панкреатина как достаточно безопасные.
К редким возможным побочным эффектам, возникающим при приеме полиферментных препаратов, следует отнести: болезненные ощущения в ротовой полости; раздражение кожи в перианальной области; дискомфорт в животе; гиперурикемию; аллергические реакции; нарушение всасывания фолиевой кислоты (образование комплексов). Наиболее тяжелое осложнение, возникающее при длительном приеме очень высоких доз полиферментных препаратов – фиброз терминальной части подвздошной кишки и правых отделов ободочной кишки, или фиброзная колонопатия.
Хотя ее патогенез до сих пор не известен, появление этой нозологии однозначно связано с длительным приемом высоких доз полиферментных препаратов, превышающих 50000 ЕД липазы на 1 кг веса в сутки. Фиброзная колонопатия наиболее часто проявляется метеоризмом и болевым абдоминальным синдромом, на рентгенограммах выявляется утолщение стенки кишечника с сужением просвета. При биопсии определяется выраженное разрастание в подслизистом слое зрелой фиброзной ткани. Считается, что это ятрогенное осложнение обусловлено кополимерами метакриловой кислоты, являющихся компонентами энтеросолюбильных оболочек большинства полиферментных препаратов. Поскольку в креоне кишечнорастворимая оболочка состоит из гидроксипропилметилцелюлозы, его прием является более безопасным. Ферментные препараты при ХП с внешнесекреторной недостаточностью назначают пожизненно, однако доза может варьировать в зависимости от многих факторов, в том числе и от соблюдения больным диеты. Таким образом, решение о выборе дозы ферментного препарата должно приниматься индивидуально для каждого больного. Мы считаем, что при выборе концентрации активности ферментов, входящих в состав препарата, можно руководствоваться данными активности фекальной эластазы. Ряд проведенных нами исследований, где использовалась методика подбора дозы полиферментного препарата у больных ХП, показал клиническую целесообразность ориентации на уровень фекальной эластазы при первичном выборе дозы. В зависимости от уровня
диагностированной по данным эластазного теста внешнесекреторной недостаточности назначается дифференцированная полиферментная терапия (Таблица 7). Так, больным ХП с нормальной экзокринной функцией ПЖ можно назначать курсовой прием креона в дозе до 50000 ЕД липазной активности в сутки с целью коррекции симптомов диспепсии, при метеоризме и болевом абдоминальном синдроме. Больным с экзокринной недостаточностью рекомендуются более высокие стартовые дозы полиферментных препаратов. Поскольку большинство больных, страдающих панкреатитом с внешнесекреторной недостаточностью, соблюдают диету, придерживаясь рекомендации частого дробного питания, у них, как правило, все приемы пищи равнозначны, и можно принимать ферменты по схеме, указанной в таблице 7. Если же диета пациента состоит из 3 традиционных приемов пищи и 2-3 промежуточных, то рекомендуется прием креона до 30000 ЕД липазы в основные приемы пищи и 10000-20000 ЕД – на промежуточные в зависимости от степени экзокринной недостаточности ПЖ. Для достижения максимального эффекта ферментные препараты должны приниматься в самом начале еды и, по возможности, фракционно во время еды (при приеме более 1 капсулы).
Таблица 7. Рекомендации по подбору дозы полиферментного препарата* у больных ХП в соответствии с данными фекальной эластазы
Состояние экзокринной |
Данные эластазы |
Рекомендуемая доза |
функции ПЖ |
кала (мкг/г) |
препарата ЕД FIP липазы в сутки |
Нормальная экзокринная |
Более 200 |
50 000 |
функция ПЖ |
|
(1 капсула креона 10 000 - |
|
|
5 раз в день) |
Умеренно выраженная |
100-199 |
100 000 (2 капсулы креона 10 000 - |
экзокринная |
|
5 раз в день) |
недостаточность |
|
|
Выраженная экзокринная |
Менее 100 |
150 000 (1 капсула креона 25 000 - |
недостаточность |
|
6 раз в день) |
|
|
|
Примечание: * только для микрокапсулированных препаратов панкреатина в энтеросолюбильной оболочке (креон).
Несмотря на правильный выбор ферментного препарата для заместительной терапии и его стартовой дозы, последнюю нередко приходится корректировать, как ввиду ее возможной неэффективности, так и при ее эффективности – с целью попытки уменьшения суточной дозы для достижения более экономичной схемы терапии (Рисунок 26). Для этого больные должны быть детально проинструктированы о режиме приема препаратов, поскольку для обеспечения оптимального воздействия лекарственных средств нужны определенные усилия со стороны пациентов - четкое выполнение данных им рекомендаций. Поэтому в последнее время большое значение придается достижению комплайнса – хорошей совместной работы врача и пациента.
В ряде случаев полностью устранить стеаторею не удается даже с помощью высоких доз препаратов, поэтому критерием адекватности подобранной дозы пищеварительных ферментов служит увеличение массы тела, нормализация стула (менее 3 раз в день), уменьшение метеоризма.
Причины неэффективности заместительной ферментной терапии могут быть следующими:

-неправильно установленный диагноз;
-наличие сопутствующей ХП патологии, утяжеляющей синдром мальабсорбции и требующий специфического лечения (глютеновая энтеропатия, воспалительные заболевания кишечника, тиреотоксикоз, глистные инвазии и т.д.); -назначение препаратов панкреатина, не имеющих кислотозащитной оболочки (панкреаль Киршнера) без блокаторов желудочной секреции;
-назначение таблетированных препаратов панкреатина в энтеросолюбильной оболочке (асинхронный гастродуоденальный транспорт);
-назначение желчьсодержащих препаратов, усиливающих перистальтику и вызывающих осмотическую диарею;
-назначение неадекватно низких доз ферментов (в том числе микрокапсулированных) для снижения общей стоимости лечения;
-нарушение комплайнса (нарушения в диете, произвольное изменение доз, времени и кратности приема полиферментных препаратов),
-недоучет возможных механизмов, приводящих к вторичной панкреатической недостаточности (желудочная гиперсекреция с ацидификацией ДПК, цирроз печени, синдром избыточного бактериального роста, гипермоторные кишечные нарушения, постгастрорезекционные расстройства и т.д.).
Как мы отмечали ранее, низкие значения интрадуоденального рН иногда приводят к инактивации принимаемых с заместительной целью полиферментных препаратов. Поэтому для достижения максимального терапевтического действия ферментов иногда рекомендуется сочетать их прием с антацидами, блокаторами Н2-рецепторов гистамина или ИПП, причем дозы и режим приема этих препаратов подбираются индивидуально. Было даже предложено ввести блокатары Н2рецепторов гистамина в качестве адъювантной терапии у больных ХП с внешнесекреторной недостаточностью ПЖ, однако опубликованные результаты были неоднозначны и отчасти противоречивы. Полная редукция стеатореи на фоне применения данных препаратов достигается редко, хотя желудочный и дуоденальный рН поддерживался на уровне рН 5 в течение долгого времени. В случае, если блокаторы Н2-рецепторов гистамина не эффективны в купировании стеатореи, показано применение ИПП, которые к настоящему времени себя хорошо зарекомендовали в комплексной терапии внешнесекреторной недостаточности ПЖ.
Рис. 25. Алгоритм заместительной терапии.
У части больных с синдромом внешнесекреторной недостаточности ПЖ ускорен транзит содержимого по кишечнику, что требует назначения препаратов, ослабляющих кишечную перистальтику (дюспаталин и др.). С симптоматическими целями могут применяться короткие курсы вяжущих и обволакивающих средств. Следует помнить, что моторика кишечника очень часто нарушена у больных сахарным диабетом и у пациентов, перенесших ваготомию (обе ситуации у пациентов с ХП, к сожалению, не редкость), кроме того, часто встречается синдром избыточного бактериального роста, снижающие эффективность заместительной полиферментной терапии. Поэтому считается, что для наиболее адекватной терапии экзокринной недостаточности необходимо обязательное включение в состав лечебного комплекса препаратов, устраняющих нарушения микробиоценоза кишечника (про- и пребиотики).
Нутритивная поддержка складывается из рекомендаций общего характера: высокое содержание белка в рационе (до 150 г/сутки), снижение на 50% от нормы содержания в пище жиров. Рекомендуются преимущественно среднецепочечные триглицериды, моно- и полиненасыщенные жирные кислоты, которые легче перевариваются панкреатической липазой и всасываются без образования мицелл. Пищевой рацион обогащается витаминами, в первую очередь жирорастворимыми. Рекомендуется принимать витаминно-минеральные комплексы, содержащие высокие дозы витаминов и микроэлементов с антиоксидантной активностью (триовит, тривиплюс и т.д.). У больных с развитием трофологической недостаточности в зависимости от тяжести состояния назначается парентеральное, энтеральное, либо комбинированное питание. В качестве парентерального питания используются растворы аминокислот, глюкозы, электролитов и микроэлементов, жировые эмульсии, витамины. Для энтерального питания используются специальные смеси, которые можно применять для зондового питания (в тяжелых случаях), в качестве добавки к пище, либо единственного источника перорального питания.
При проведении занятий школы на основании приведенных данных необходимо указать, что при выборе схемы консервативного лечения ХП необходим индивидуальный подход в каждом отдельно взятом случае с учетом степени экзокринной и трофологической недостаточности, выраженности болевого абдоминального синдрома и эндокринных расстройств. Разработанные в последние годы галенические формы ферментных препаратов, существенно улучшающие смешивание и сегрегацию протеаз и липазы непосредственно к их субстратам, значительно повышают качество заместительной терапии при панкреатической недостаточности. Применение таблетированных полиферментных препаратов, покрытых оболочкой, защищающей препарат от соляной кислоты в желудке практически бесполезно; только препараты последних поколений, содержащие минимикросферы панкреатина, покрытые энтеросолюбильной оболочкой, достоверно и дозозависимо уменьшают стеаторею. Знание практикующим врачом принципов заместительной ферментной терапии определяет адекватность назначенного лечения и прогноз течения болезни.
Список рекомендуемой литературы:
1.Багненко С.Ф., Курыгин А.А., Рухляда Н.В., Смирнов А.Д. Хронический панкреатит: руководство для врачей. - СПб.: «Питер», 2000. - 416 с.
2.Банифатов П.В. Ультразвуковая диагностика хронических панкреатитов//
Consilium medicum. - 2002. - №1. - С. 26-29.
3.Белоусова Е.А., Златкина А.Р., Морозова Н.А., Тишкина Н.Н. Старые и новые аспекты применения ферментных препаратов в гастроэнтерологии // Фарматека –
2003. - №7. - С.39-44.
4.Гребенев А.Л. Хронические панкреатиты // Руководство по гастроэнтерологии. Под. ред. Ф.И. Комарова, А.Л. Гребенева. - М.: Медицина, 1996. - Т.З. - С. 81-112.
5.Губергриц Н.Б., Христич Т.Н. Клиническая панкреатология. – Донецк - ООО
"Лебедь", 2000.-416 с.
6.Губергриц Н.Б. Лечение панкреатитов. Ферментные препараты в гастроэнтерологии. - М.: Медпрактика-М, 2003. - 100с.
7.ДиМагно Е.П. Межпищеварительная и стимулированная экзокринная панкреатическая секреция у человека в физиологических условиях и при патологии и последствия ее нарушений // Физиология и патофизиология желудочно-кишечного тракта / Под ред. Дж.М. Полак и др.; Пер. с англ. - М.: Медицина, 1989. - С.302-321.
8.Зикеева В.К. Лечебное питание при остром и хроническом панкреатите. В кн. Справочник по диетологии / Под. ред. В.А. Тутульяна, М.А. Самсонова. - 3-е изд., перераб. и доп. - М.: Медицина, 2002. - С.209-217.
9.Евтихов P.M., Журавлев В.А., Шулутко A.M. и соавт. Механическая желтуха. Хронический панкреатит. — Иваново, 1999. — 256 с.
10.Ивашкин В.Т. Современные проблемы клинической панкреатологии // Вестник РАМН. - 1993. - №4. - С.29-34.
11.Ивашкин В.Т., Минасян Г.А. Лечение хронического панкреатита // Рос. журн. гастроэнтерол., гепатол., колопроктол. - 1996. - №4. - С.10-17.
12.Ивашкин В.Т., Лапина Т.Л., Баранская Е.К., Буеверов А.О., Буклис Э.Р., Гуревич К.Г. и др. Рациональная фармакотерапия органов пищеварения: Рук. для практикующих врачей. Под общ. ред. В.Т. Ивашкина. - М.: Литтерра, 2003. - 1046с.
13.Ильченко А.А., Быстровская Е.В. Опыт применения дюспаталина при функциональных нарушениях сфинктера Одди у больных, перенесших холецистэктомию // Эксп. клин, гастроэнтерол. - 2002. - №4. - С.21-22.
14.Ильченко А.А., Вихрова ТВ. Проблема билиарного сладжа // Клин мед - 2003 - №8.-С. 17-22.
15.Калинин А.В. Хронический панкреатит: этиология, классификация, клиника, диагностика, лечение и профилактика: Метод, рекоменд. - М.: 1999. - 45с.
16.Коротько Г.Ф. Секреция поджелудочной железы. - М.: "Триада-Х", 2002. - С.24-
17.Костюченко А.Л., Филин В.И. Неотложная панкреатология: справочник для врачей, издание 2-е, исправленное и дополненное. — СПб.: Издательство «Деан»,
2000. - 480с.
18.Кузин М.И., Данилов М.В., Благовидов Д.Ф. Хронический панкреатит. - М.: Медицина, 1985. - 368 с.
19.Лопаткина Т.Н. Хронический панкреатит // Новый медицинский журнал. - 1997. - №2. -С.7-11.
20.Лопаткина Т.Н. Хронический панкреатит: проблемы диагностики, роль нарушений желевыделения и подходы к лечению // Клин, фармакол. тер. - 2004. -
№ 1. - С.9-11.
21.Маев И.В., Казюлин А.Н., Дичева Д.Т., Кучерявый Ю.А. и др. Хронический панкреатит // Учебное пособие. - М.: ВУНМЦ МЗ РФ, 2003. - 80с.
22.Маев И.В., Кучерявый Ю.А. Синдром внешнесекреторной панкреатической недостаточности // Врачебная газета. - 2003. - №11. — С.19-21.
23.Маев И.В., Кучерявый Ю.А. Полиферментные препараты в гастроэнтерологической практике // Врач. - 2003. - №10. - с.59-61.
24.Маев И.В., Кучерявый Ю.А. Дозозависимая терапия полиферментными препаратами в энтеросолюбильной оболочке при хроническом билиарнозависимом панкреатите // Врач. - 2003. - №12. - с.35-38.
25.Маев И.В., Кучерявый Ю.А. Современные подходы к диагностике и лечению хронического панкреатита// Качество жизни. Медицина. - 2004. - №2(5). - С.65-69.
26.Мараховский Ю.Х. Хронический панкреатит. Новые данные об этиологии и патогенезе. Современная классификация. Успехи в диагностике и лечении // РМЖ.
— 1996.-№3.-С.156-160.
27.Минушкин О.Н. Хронический панкреатит: некоторые аспекты патогенеза, диагностики и лечения // Consilium medicum. - 2002. - №1. - С.23-26.
28.Минушкин О.Н., Масловский Л.В., Гребенева Л.С. Диагностика и дифференцированное этапное лечение больных хроническим панкреатитом // Методические рекомендации - М.: 2002. - 31 с.
29.Охлобыстин А.В. Применение препаратов пищеварительных ферментов в гастроэнтерологии // Клин, перспект. гастроэнтерол., гепатол. — 2001. - №2. - с.34-
30.Охлобыстин А.В., Буклис Э.Р. Современные возможности терапии хронического панкреатита//Лечащий врач. - 2003. - №5. - С. 32-36.
31.Панфилов С.А., Панфилова Е.В. Диагностика заболеваний печени, билиарного тракта, поджелудочной железы, селезенки и надпочечников с курсом патологической анатомии. - М.: БИНОМ. Лаборатория знаний, 2003. - 215с.
32.Скуя Н.А. Заболевания поджелудочной железы. - М.: Медицина, 1986. - 240 с.
33.Хазанов А.И., Васильев А.П., Спесивцев В.Н. и др. Хронический панкреатит, его течение и исходы // Рос. журн. гастроэнтерол., гепатол., колопроктол. - 1999. - № 4. - С.24-30.
34.Хендерсон Д.М. Патофизиология органов пищеварения. Пер. с англ. - М. - СПб.: Бином-Невский Диалект, 1997. - С.197-224.
35.Щербаков П.Л. Ферментные препараты при заболеваниях поджелудочной железы// Клин. мед. - 2001. - №11. - С.71-74.
36.Циммерман Я.С. Очерки клинической гастроэнтерологии. - Пермь: Изд-во Пермского университета, 1992. - 336с.
37.Яковенко А.В. Клиника, диагностика и лечение хронического панкреатита // Клин. мед. - 2001. - №9. - С. 15-20.
