
6 курс / Гастроэнтерология / Демиденко_Т_П_,_Неверов_В_А_,_Лобзин_Ю_В_Вирусные_гепатиты
.pdf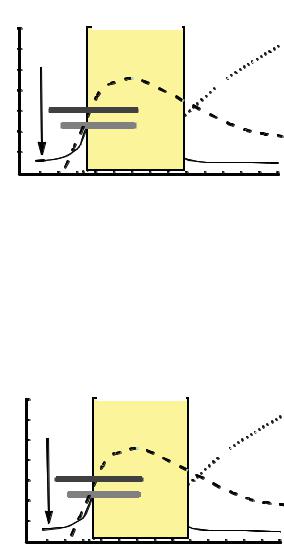
показателя |
|
СимптомыClinical illnessболезни |
Заражение |
AлАT |
|
|
Infect |
|
ResponseвеличинаОтносительная |
ion |
Anti-HAV-IgM |
|
||
|
|
|
|
|
Anti-HAV-IgG |
|
Виремия |
|
|
|
HAV |
|
|
в фекалиях |
0 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
|
|
|
|
|
Недели |
|
|
|
|
|
|
|
|
Рис.12. Динамика клинико-лабораторных маркеров при ВГВ-ВГD коинфекции.
Острая суперинфекция ВГD (острый дельта-гепатит) может быть подтвержден наличием маркеров репродукции ВГD: HDV-RNA и IgM анти-HDV при отсутствии (или низком титре) IgM анти-HBc (рис.13).
показателя |
|
СимптомыClinical illnessболезни |
Заражение |
AлАT |
|
|
Infect |
|
ResponseвеличинаОтносительная |
ion |
Anti-HAV-IgM |
|
|
|
|
|
Anti-HAV-IgG |
|
Виремия |
|
|
|
HAV |
|
|
в фекалиях |
0 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
|
|
|
|
|
Недели |
|
|
|
|
|
|
|
|
Рис.13. Динамика клинико-лабораторных маркеров при ВГВ-ВГD суперинфекции.
Хронический гепатит D
На основании взаимоотношений ВГВ и ВГD выделяют три фазы течения хронической инфекции ВГD:
–первая (ранняя, активная) стадия, когда ВГD подавляет репликацию ВГВ (в сыворотке крови обнаруживают РНК ВГD в высоком титре, ДНК ВГВ в низком титре или ниже порога определения);
–вторая стадия – умеренная репликативная активность ВГD и постепенная реактивация ВГВ (в сыворотке определяется как РНК ВГD, так и ДНК ВГВ);
–третья (поздняя) стадия характеризуется снижением репликативной активности обоих вирусов (РНК ВГD и ДНК ВГВ в низком титре или не определяются) и наблюдается, как правило, у больных на стадии цирроза печени или ГЦК.
Независимо от механизма возникновения, клиника хронического гепатита D отличается, по мнению большинства исследователей, прогрессирующим течением. Хронические носители HВsAg, ранее вполне компенсированные, начинают испытывать быструю утомляемость, слабость. Резко снижается трудоспособность, падает аппетит, развивается выраженное похудание, появляется чувство тяжести в правом подреберье. Характерна гепатоспленомегалия, нередко с синдромом гиперспленизма, непостоянная желтуха.
Клиническиепроявленияхроническогодельта-гепатита, как
илюбогохроническогодиффузногозаболеванияпечени, включают в себя симптомы и синдромы, связанные как с поражением печени, так и внепеченочными проявлениями. К первым относят астенический синдром, умеренную гепатомегалию, реже гепатоспленомегалию, а также клинико-лабораторные синдромы (от цитолиза до печеночноклеточной недостаточности). Внепеченочные проявления хронического дельта–гепа- тита могут быть представлены самыми разными синдромами, большинство из которых имеют аутоиммунную природу. Развитиеаутоиммунныхнарушенийутакихпациентовассоциируется с антителами – LKM-3 (микросомальные антитела к ткани печени/почек 3). Пока не установлена достоверная значи-
мость в развитии внепеченочных проявлений таких факторов, как вирусная нагрузка, пол пациента и длительность заболевания. Наличиеаутоиммунногосиндромаупациентовсхроническим дельта-гепатитом ухудшает прогноз. Данное обстоятельствосвязановосновномспозднейдиагностикойизачастуюневернойтрактовкойаутоиммунныхсиндромов. Крометого, внепеченочные проявления хронического дельта-гепатита значительноусложняютэтиотропнуютерапию.
Хронический ГD характеризуется, как правило, прогрессирующим течением заболевания с исходом в цирроз печени (у 70-80% больных) в течение 10-20 лет. В 5-10% случаев наблюдается быстро прогрессирующее течение с декомпенсацией печеночного процесса в течение нескольких лет после инфицирования. Значительно реже (в 10-15 % случаев), чем при хроническом ГВ, может наблюдаться непрогрессирующеетечениеГD (латентнаяинфекцияВГD). Частоубольных хроническим ГD в момент установления диагноза выставляют стадию цирроза печени.
Придельта-гепатитеизвестныдостаточнохарактерныемор- фологические изменения. Описывается феномен «песочноклеточных ядер» – как проявление цитопатического действия вируса. Гепатоциты могут становиться двуядерными или гигантоядерными. Однакоклеткисподобнымипатогномоничными признаками встречаются нечасто. Морфологические исследованияобычновыявляютпостоянновысокуюактивностьвоспаления в печеночной ткани при дельта-инфекции. Выражена инфильтрация портальных трактов, с некрозами разной степени, разрушениемпограничнойпластинки. Отмечаетсяповреждение желчных протоков, расширение синусоидов с их капилляризацией, дегенерация и дистрофия гепатоцитов в сочетании с разрастанием грубой фиброзной соединительной ткани. При переходе ХГ в ЦП появляются ложные дольки, портопортальныетяжиифиброзныеполя, инфильтрированныелимфоидными клетками. В единичных биоптатах обнаруживают целые поля дельта-позитивных гепатоцитов (иммунофлуоресценция). Но, восновном, дельта-антигенопределяетсятольков
отдельных клетках или небольших клеточных группах, расположенных центролобулярно. Их можно видеть среди внутридольковыхинфильтратов, взонахступенчатыхнекрозов, атакже среди неизмененных гепатоцитов. Выявление в биоптатах единичных некротизированных гепатоцитов, не окруженных элементами воспалительного инфильтрата, в отличие от гепатита B, подтверждает наличие прямого цитопатического действияВГD ииммунногоцитолиза, индуцированногоВГВ.
Некоторые авторы выделяют латентную инфекцию ВГD, когда маркеры активной инфекции ВГD (РНК ВГD и ВГDAg) выявляют только в ткани печени, а в сыворотке крови могут быть обнаружены только IgG анти ВГD в отсутствие HBsAg. Реактивация инфекции у этих пациентов может привести к прогрессированию заболевания в хронический гепатит и цирроз печени.
В целом, больные гепатитом D страдают от заболевания болеетяжелогоисклонногокпрогрессированию, чемпридругих формах вирусных гепатитов, с максимальным преобладанием фулминантныхформичастымразвитиемциррозапечени.
Противовирусное лечение ГD.
Показанием к лечению хронического ГD служит наличие вирусемии и повышение уровня АлАТ. Несколько более благоприятный прогноз лечения имеют пациенты с небольшой длительностьюзаболеванияиотсутствиемвыраженногофиброза.
Лечение проводят стандартным или пегинтерфероном. Доза ИФН-α 5 млн МЕ, кратность введения ежедневно или по 10 млн МЕ через день.
Пег-ИФН-α2α – 180 мкг/нед или пег-ИФН α2β - 1,5 мкг/кг /нед. Курс лечения 48 недель.
При достижении полного ответа (клиренс РНК ВГD и нормализация АлАТ) возможно прекращение лечения и динамическое наблюдение. В случае рецидива можно обсуждать вопрос о повторном курсе лечения.
Убольныхсчастичнымответом(снижениеуровняРНКВГD

болеечемна2 log10) лечениепродолжаютещевтечениегода. При лечении стандартным интерфероном альфа в течение 12 месяцев к концу лечения у 30-50% больных достигается вирусологический ответ, однако более чем у половины из них наблюдается рецидив заболевания. Стойкий ответ отме- чаютвсреднему15-25% больных. Использованиепегинтерферона альфа несколько повышает эффективность лечения. Применение аналогов нуклеиот(з)идов не является эф-
фективным.
Профилактика не отличается от профилактики ГВ. Существующая вакцинация против ГВ защищает и от ГD. РазрабатываетсяивакцинапротивГD, защищающаялиц, инфицированных ВГВ.
Вирусный гепатит С
СогласноМКБ-10 острыеихроническиегепатитыСрегистрируются под кодами:
B17 «Другие острые вирусные гепатиты»: В17.1 – «Острый гепатит С».
B18 «Хронический вирусный гепатит»:
B18.2 – «Хронический вирусный гепатит С».
Этиология. Вирус гепатит С (ВГС) — РНК, содержащий вирус, относящийся к семейству флавивирусов. Размеры вируса около 50 нм (рис.14).
Рис.14. ЭлектронограммыВГС(авторы: M. T. Catanese, M. Kopp, K. Uryu , Ch.Rice (Wikipedia) и PhD Dre at en.wikipedia)
Геном состоит из однонитевой линейной РНК. Нуклеокапсид окружен липидной оболочкой и включенными в нее белковыми структурами, кодированными РНК ВГС. Геном кодирует образование структурных и неструктурных белков вируса. К структурным белкам ВГС относятся: нуклеокапсидный белок C (core protein) и оболочечные (envelope)
— E1 и E2/ NS1 гликопротеин. Coreбелок (р22) принимает участие в образовании капсида и в репликации ВГС. Структурные белки, кодированные зоной Е1 и Е2 входят в состав наружнойоболочкивирусаинесутнасвоейповерхностиантигенные детерминанты вируса. Белки оболочки участвуют впроникновениивирусавклетку, атакжевразвитиииммунныхреакцийи«ускользании» отиммунногоответанавирус. Значительная изменчивость этих белков определяет трудности в создании эффективных вакцин против ГС. В участке гена Е2 выделяют гипервариабельный регион. Изменения, происходящие в этом регионе РНК ВГС и соответствующие изменения в антигенных детерминантах Е2 играют ключевую роль в «ускользании вируса» от первичного иммунного ответа на ВГС. В состав неструктурных белков (NS2, NS3, NS4А, NS4В, NS5А, NS5В) входят ферментативноактивные протеины. На все эти белки в организме больного вырабатываются антитела (анти-HCV), которые и определяются иммунохимическими методами.
Вирус гепатита С по сравнению с вирусом гепатита В менее устойчив к физико-химическим воздействиям, и для заражения ВГС необходима большая инфицирующая доза. Крометого, ВГСпосравнениюсВИЧиВГВимеетболеекороткий период времени полужизни вирусной частицы и более высокий уровень их продукции. Эти показатели для ВГС составляют около 3-х часов и 1,1 х 1012 синтезированных вирионов в день, а для ВГВ и ВИЧ соответственно 24 и около 6 часов при продукции 1011 и 1010 частиц вирусов.
Ключевым звеном в понимании вирусологии, патогенеза и эпидемиологии ГС является факт высокой генетической вариабельности РНК ВГС.
Выделяют 6 генотипов и более 100 субтипов ВГС. Кроме того, установлено наличие множественных вариантов ВГС или квазивидов этого вируса. Их существование объясняет его «ускользание» из-под иммунного контроля организма, а последнее обстоятельство определяет возможность появленияновых, постоянноменяющихсяантигенныхструктурвируса. ВысокаяизменчивостьВГСлежитвосноведлительного, возможнопожизненного, сохранениявирусаворганизме.
Высокая изменчивость РНК ВГС определяется появлением точечных мутаций, вставок и делеций, возникающих при репликации вируса. Другой механизм, обеспечивающий изменчивость генома вируса – рекомбинация между разными генотипами ВГС.
В России чаще всего обнаруживаются генотипы: 1 (a и b), 2a и 3a. С генотипом 1b большинство исследователей связывают случаи заболеваний с высоким уровнем виремии и низким ответом на интерферонотерапию.
Эпидемиология. Источники инфекции, механизм и пути передачи во многом соответствуют ГВ.
Источники ГС – больные хроническими и острыми формами инфекции. Наибольшее эпидемиологическое значение имеет парентеральный путь передачи. Чаще всего заражение ВГС происходит при переливании крови и ее препаратов. Считают, что возбудитель ГС является одним из основных этиологических факторов посттрансфузионного гепатита. Нередко инфекция встречается у больных гемофилией. Тестирование доноров, консервированной крови и ее дериватов на ВГС является обязательным.
Особое значение ГС имеет для наркоманов, использующих наркотики парентерально. В настоящее время это одна из самых многочисленных и эпидемиологически значимых групприскаинфицированияВГС. ВразныхрегионахРоссии обнаружение анти-HCV среди внутривенных пользователей наркотиков составляет 75-83%.
Передача возбудителя в быту при гетеро- и гомосексуаль-
ных контактах, а также от инфицированной матери к новорожденному может иметь место, но реализуется значительно реже, чем при ГВ.
Патогенез. После проникновения в организм человека ВГС, обладая гепатотропностью, реплицируется преимущественно в гепатоцитах. Белок NS5A является компонентом репликативного комплекса вируса. В инфицированной клетке этот белок обнаруживается около ядерной мембраны вместе с белком NS5B. Как известно, NS5B функционирует как РНК-зависимая РНК-полимераза. Из-за отсутствия 3' -5' –экзонуклеазной активности эта РНК-полимераза допускает много ошибок при репликации, что приводит к высокой скорости мутации. Доказано, что в течение инфекционного процесса у одного и того же пациента наблюдаются постоянные изменения в последовательности генома ВГС, что является результатом ухода от иммунного ответа и высокими адаптивными свойствами ВГС. Изменение набора квазивидов во время инфекции связано с отбором форм, устойчивых к иммунному ответу макроорганизма.
В настоящее время доказанным фактом является возможность внепеченочной репликации вируса. По мнению большинства исследователей, хотя печень и является основным органом, гдепроисходитвируснаярепликация, ВГСможетреплицироваться в периферических мононуклеарах, лимфатических узлах, поджелудочной железе, в клетках костного мозга. Внепеченочные очаги репликации ВГС являются дополнительным резервуаром вируса в организме. Предполагают, в частности, что инфицированные моноциты могут мигрировать в печень и способствовать развитию её патологии.
ВГСобладаетслабойиммуногенностью, чтоопределяетзамедленный, неинтенсивный Т-клеточный и гуморальный ответ иммуннойсистемынаинфекцию. Так, востройстадииГСсероконверсия возникает на 1-2 мес. позже появления признаков цитолиза гепатоцитов (повышения активности АлАТ). Лишь через 2-10 нед. от начала заболевания, в крови больных начинают определяться антитела к ядерному (core) антигену классов M, затем G.

Однакоониобладаютслабымвируснейтрализующимдействием. АнтителажекнеструктурнымбелкамВГСвостройфазеинфекцииобычноневыявляются. Вкровивтечениеостройстадииболезни(иприреактивации— вхронической) определяетсяприсутствиеРНКвируса. УстойчивостьВГСкспецифическимфакторам иммунитетаобусловленаеговысокойспособностьюк«ускользанию» из-под иммунологического надзора. Одним из механизмов этого является реплицирование ВГС с высоким уровнем мутаций, чтоопределяетприсутствиеворганизмемножествапостоянно изменяющихся антигенных вариантов вируса (квазиразновидности). Такимобразом, слабостьиммунногореагированияимутационнаяизменчивостьвирусавомногомобусловливаютвысокий хрониогенныйпотенциалданногозаболевания.
Клиника.
Инкубационный период от 2 до 26 недель (в среднем — 6-8 недель). В течении ГС выделяют острую и хроническую стадии болезни.
Острая стадия ГС чаще всего протекает в бессимптомной форме. Своевременная диагностика ее значительно затруднена. Диагноз может быть верифицирован путем индикацииРНКВГСметодомПЦРприналичиесерьезныхэпидемиологических предпосылок. Манифестное течение острой стадии ГС наблюдается лишь в 10-20% случаев (рис.15).
показателя |
|
СимптомыClinical illnessболезни |
ЗаражениеInfect |
AлАT |
|
ResponseвеличинаОтносительная |
ion |
Anti-HAV-IgM |
|
||
|
|
|
|
|
Anti-HAV-IgG |
|
Виремия |
|
|
|
HAV |
|
|
в фекалиях |
0 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
|
|
|
|
|
Недели |
|
|
|
|
|
|
|
|
Рис.15. Динамика клинико-лабораторных маркеров при остром течения ГС (по CDC).
Для продромального периода характерны диспепсический синдром (снижение аппетита, тошнота), нередко слабость, недомогание. В периоде разгара желтуха часто отсутствует, а если и развивается, то она умеренно выражена, интоксикация незначительная. Острый ГС протекает гораздо легче, чем ГВ и даже ГА, преимущественно в легкой, редко в среднетяжелой форме, с умеренным повышением активности аминотрансфераз (в 5-20 раз). Однако имеются сведения о фулминантном течении инфекции, особенно у хронических носителей HBsAg. Описаны случаи ГС, осложнившиеся апластической анемией.
Лечение острого гепатита С.
Показаниемдляпроведенияпротивовируснойтерапииявляется ОГС с наличием виремии. Лечение, начатое после 3 мес заболевания, может сопровождаться развитием устойчивого вирусологического ответа (УВО) более чем у 80% больных ОГС. Подобная закономерность отмечается при использовании интерферонов как короткого действия («коротких»), так и пегилированных интерферонов (Пег-ИФН). В настоящее время окончательно не определены оптимальный режим введения, дозы, длительность и тип ИФН, так как количествоисследований, построенныхнаосновепринциповдоказательной медицины, невелико.
Сучетомимеющихсянасегодняданныхрекомендациипо специфическому лечению острого гепатита С можно свести
кследующему:
–больным ОГС целесообразно назначать противовирусную терапию препаратами интерферонового ряда;
–противовирусное лечение может быть отложено на 8–12 нед от дебюта заболевания (отсрочка допустима в связи с возможностью спонтанного выздоровления);
–монотерапия стандартными интерферонами обладает высокой эффективностью, однако предпочтение может быть отдано пегилированным интерферонам, учитывая меньшую кратность их введения;
