

1. Катаболизм и анаболизм. Общая схема и этапы обмена веществ и энергии в организме человека. Специфические и общие п катаболизма.
Анаболизм - синтез более сложных молекул из простых.
Катаболизм - расщепление крупных молекул на более мелкие.
Катаболизм начинается в системе пищеварения, где основные классы молекул подвергаются ферментативному гидролизу и расщепляются до АК, жирных кислот и глицерина и моносахаридов.
После их всасывания, транспорта и распределения по клеткам организма начинаются специфические пути катаболизма, которые заключаются во внутриклеточных превращениях вышеперечисленных веществ в молекулы ПВК и ацетил-КоА.

ПВК и ацетил-КоА распадаются в общих путях метаболизма - окислительное декарбоксилирование ПВК и цикл Кребса
Первый этап
Происходит в кишечнике (переваривание пищи) или в лизосомах (самообновление клеток) при расщеплении уже ненужных или лишних молекул. При этом освобождается около 1% энергии, заключенной в молекуле. Она рассеивается в виде тепла.
Второй этап
Вещества, образованные при внутриклеточном гидролизе или проникающие в клетку из крови, на втором этапе обычно превращаются
●в пировиноградную кислоту (моносахариды в гликолизе),
●в ацетил-SKoA, в пируват и другие кетокислоты (в катаболизме аминокислот),
●в ацетил-SКоА (при β-окислении жирных кислот).
Локализация второго этапа – цитозоль и митохондрии. На этом этапе выделяется около 30% энергии, заключенной в молекуле, и при этом запасается около 13% от всей энергии вещества (или примерно 43% от выделенной на этом этапе энергии).
Третий этап
Все реакции этого этапа идут в митохондриях
Ацетил-SКоА (и кетокислоты) включается в реакции цикла трикарбоновых кислот, где углероды веществ окисляются до углекислого газа. Выделенные атомы водорода соединяются с НАД и ФАД, восстанавливают их и после этого НАДН и ФАДН2 переносят водород в цепь ферментов дыхательной цепи, расположенную на внутренней мембране митохондрий. Сюда же отдают свои атомы водорода молекулы НАДН и ФАДН2, образованные на втором этапе (гликолиз, окисление жирных кислот и аминокислот). В третьем этапе выделяется до 70% всей энергии вещества. Из этого количества усваивается почти две трети (66%), что составляет около 46% от общей. Таким образом, из 100% энергии окисляемой молекулы клетка запасает больше половины – 59%.
2. Окислительное декарбоксилирование пирувата. Строение пируватдегидрогеназного комплекса.
Пр-т в матриксе митохондрий
Осуществляется при участии специального белка переносчика по механизму симпорта с Н+
Суммарное уравнение -
Реакция необратима

Строение пируватдегидрогеназного комплекса:
3 фермента: пируватдекарбоксилаза (Е1), дигидролипоилтрансацетилаза (Е2), дигидролипоилдегидрогеназа (Е3)
5 коферментов: тиаминдифосфат, липоевая кислота, ФАД, НАД+, КоА
Регуляторные субъединицы: протеинкиназа и фосфопротеинфосфатаза
Вцентре Е2 (ядро), к Е2 присоединены Е1 и Е3
Е1 содержит ТДФ, а Е3 - ФАД

3. Стадии окислительного декарбоксилирования пирувата. Регуляция пируватдегидрогеназного комплекса.
Регуляция пируватдегидрогеназного комплекса:
доступность субстратов
ингибирование
аллостерический механизм
ковалентная модификация
ионы Ca через протеинфосфатазу
|
Фосфорилирование/дефосфорилирование |
Ковалентная модификация |
В состав ПДК входят: |
|
- киназа ПДК - фосфорилирует ферменты комплекса и |
|
инактивирует ПДК |
|
- фосфатаза - дефосфорилирует ферменты, активируя |
|
ПДК |
|
|
Ингибирование продуктами реакции |
Продукты пируватдегидрогеназной реакции аллостерически |
активируют киназу ПДК, она инактивирует ПДК => |
|
|
|

|
|
При накоплении НАДН и ацетил-КоА тормозится превращение |
|
|
|
пирувата в ацетил-КоА |
|
|
|
|
|
|
Аллостерический путь |
Пируват аллостерически активирует нефосфорилированную |
|
|
|
форму ПДК, действуя согласно с другими субстратами НАД+ и |
|
|
|
КоА |
|
|
|
|
|
|
|
|
|
4. Цикл трикарбоновых кислот. Общая схема, энергетическое значение.
●Цикл протекает в матриксе митохондрий
●представляет собой окисление молекулы ацетил-SКоА в восьми последовательных реакциях.
●1 моль ацетила = 10 моль АТФ
●генерация атомов водорода для работы дыхательной цепи, а именно трех молекул НАДН и одной молекулы ФАДН2,
●синтез одной молекулы ГТФ (эквивалентна АТФ).
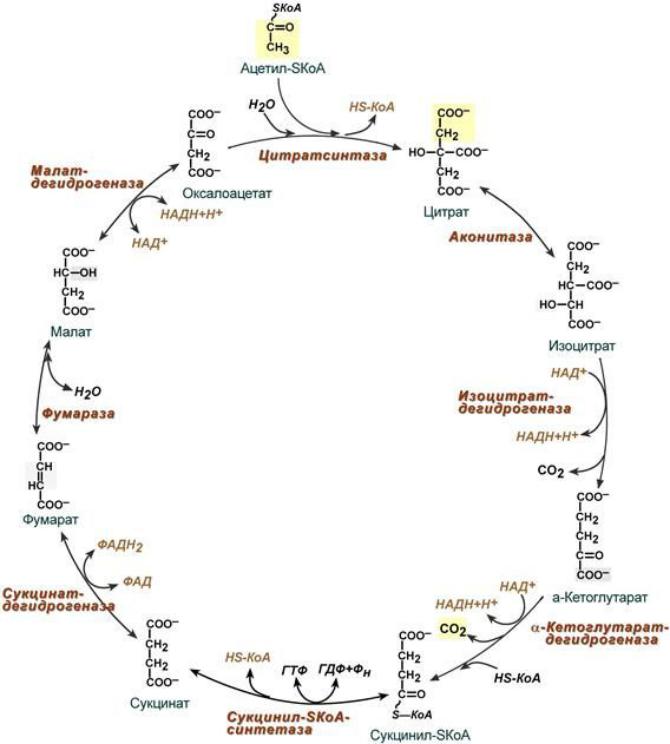
5. Последовательность реакций цикла трикарбоновых кислот. Реакции дегидрирования. Субстратное фосфорилировани
I.Образование цитрата
-углеродный атом метильной группы ацетил-КоА связывается с карбонильной группой оксалоацетата
-одновременно расщепляется тиоэфирная связь и высвобождается коэнзим А
-большая потеря энергии в виде теплоты
-фермент - цитратсинтаза (в матриксе митохондрий)
II.Превращение цитрата в изоцитрат
-фермент - изоцитратдегидрогеназа (2 формы - одна содержит в кач-ве кофермента НАД+, другая - НАДФ+)
-НАД-зависимый фермент в митохондриях, уч-т в цикле Кребса
-в р-те образуется -кетоглутарат
-самая медленная реакция
III.Окислительное декарбоксилирование -кетоглутарата
-конечные продукты: сукцинил-КоА, СО2, НАДН + Н+
-фермент - -кетоглутаратдегидрогеназный комплекс (похож на ПДК): из 3-х ферментов: -кетоглутараткарбоксилаза, дигидролипоилтранссукцинилаза, дигидролипоилдегидрогеназа; 5 коферментов: тиаминдифосфат, кофермент А, липоевая кислота, НАД+ и ФАД; Отличие от ПДК - нет сложного механизма регуляции
IV. Превращение сукцинил-КоА в сукцинат
-разрыв тиоэфирной связи сукцинил-КоА сопряжен с реакцией фосфорилирования ГДФ до ГТФ
-фермент - сукцинаттиокиназа
-промежуточный этап - фосфорилирование молекулы фермента по одному из гистидиновых остатков активного центра, затем остаток фосфорной кислоты присоединяется к ГДФ с образованием ГТФ
-с ГТФ концевая фосфатная группа может переноситься на АДФ с образованием АТФ, фермент - нуклеозидфосфаткиназа
-образование высокоэнергетической фосфоангидридной связи за счет энергии субстрата - пример субстратного фосфорилизования.
V.Дегидрирование сукцината
-сукцинат превращается в фумарат под действием фермента сукцинатдегидрогеназы
-сукцинатдегидрогеназа - флавопротеин, содержит ФАД
-сукцинатдегидрогеназа прочно связана с митохондриальной мембраной, состоит из 2-х субъединиц, одна содержит ФАД, обе содержат железо-серные центры. В этих центрах атомы железа меняют свою валентность, участвуя в транспорте электронов.
VI. Образование малата из фумарата
-фермент - фумаратгидратаза (фумараза)
-фумараза - олигомерный белок из 4-х идентичных полипептидный цепей, в матриксе митохондрий. Фермент с абсолютной специфичностью (только транс-формы фумарата)
VII. Дегидрирование малата
-образуется оксалоацетат
-фермент - НАД-зависимая малатдегидрогеназа (в матриксе митохондрий)

6. Регуляция цикла трикарбоновых кислот.
Главным и основным регулятором ЦТК является оксалоацетат (его доступность)
Источник оксалоацетата - глюкоза (через пируват), поступление из фруктовых кислот самого цикла (яблочная, лимонная), образование из аспарагиновой кислоты в результате трансаминирования или цикла АМФ-ИМФ
Реакции пополнения цикла новыми метаболитами называются анаплеротическими.
Ферменты, катализирующие 1-ю, 3-ю и 4-ю реакции ЦТК, являются чувствительными к аллостерической регуляции метаболитами:
|
Ингибиторы |
Активаторы |
|
|
|
Цитратсинтаза |
АТФ, цитрат, НАДН, ацил-S КоА |
|
|
|
|
Изоцитрат-дегидрогеназа |
АТФ, НАДН |
АМФ, АДФ |
|
|
|
α-Кетоглутарат-дегидрогеназа |
Сукцинил-SКоА, НАДН |
|
|
|
|
7. Анаболические функции цикла трикарбоновых кислот. Анаплеротические реакции.
Реакции пополнения цикла новыми метаболитами (оксалоацетат, цитрат, α-кетоглутарат и т.п) называются анаплеротическими.
ВЦТК образуются
●предшественник гема – сукцинил-SКоА,
●кетокислоты, способные превращаться в аминокислоты – α-кетоглутарат для глутаминовой кислоты, оксалоацетат для аспарагиновой,
●лимонная кислота, используемая для синтеза жирных кислот,
●оксалоацетат, используемый для синтеза глюкозы.

8. Роль коферментных форм витаминов В1, В2, В3, В5 в общих путях катаболизма.
1) Пируват- и 2-оксоглутаратдегидрогеназные комплексы: В1 - необходим для синтеза ТПФ; липоевая кислота (витаминоподобное вещество); пантотеновая кислота - необходима для синтеза HS-КоА; В2 - необходим для синтеза ФАД; РР - необходим для синтеза НАД.
2)Биотин катализирует реакцию карбоксилирования пирувата с образованием оксалоацетата.
3)В6 необходим для синтеза пиридоксальфосфата, являющегося кофактором аспартат- и аланинаминотрансфераз, катализирующих превращение аспарата в оксалоацетат и аланина в пируват, соответственно. Перечисленные выше витамины должны составлять
основу сбалансированных поливитаминных препаратов.
Бонус: то, что понадобится на контрольной
Обмен веществ (метаболизм) - совокупность химических процессов, обеспечивающих жизнедеятельность организма. Значение:
три специализированные функции:
1.Энергетическая – снабжение клетки химической энергией,
2.Пластическая – синтез макромолекул как строительных блоков,
3.Специфическая – синтез и распад биомолекул, необходимых для выполнения специфических клеточных функций.
Воснове лежат катаболизм и анаболизм
Взаимосвязь
Энергия, высвобождаемая в реакциях катаболизма, запасается в виде связей, называемых макроэргическими. Основной и универсальной молекулой, которая запасает энергию и при необходимости отдает ее, является АТФ.
Классификация макроэргов

Макроэргические соединения классифицируются по типу связи, несущей дополнительную энергию:
1.Фосфоангидридная связь. Такую связь имеют все нуклеотиды: нуклеозидтрифосфаты (АТФ, ГТФ, ЦТФ, УТФ, ТТФ) и нуклеозиддифосфаты (АДФ, ГДФ, ЦДФ, УДФ, ТДФ).
2.Тиоэфирная связь. Примером являются ацил-производные коэнзима А: ацетил-SКоА, сукцинил-SКоА, и другие соединения любой жирной кислоты c HS-КоА.
3.Гуанидинфосфатная связь – присутствует в креатинфосфате, запасном макроэрге мышечной и нервной ткани.
4.Ацилфосфатная связь. К таким макроэргам относится метаболит гликолиза 1,3-дифосфоглицериновая кислота
(1,3-дифосфоглицерат). Она обеспечивает синтез АТФ в реакции субстратного фосфорилирования.
5. Енолфосфатная связь. Представитель – фосфоенолпируват, метаболит гликолиза. Он также обеспечивает синтез АТФ в реакции субстратного фосфорилирования в гликолизе.
-общая схема катаболизма
