

ОБЩИЕВОПРОСЫ БИОХИМИИ:
КЛАССИФИКАЦИЯФЕРМЕНТОВ
Блок 1 Тема 2

2
СОДЕРЖАНИЕ
1.Названияферментов
2.Классыферментов
3.1-клаоксидоредуктазы
3.1.Оксидазы
3.2.Аэробныедегидрогеназы
3.3.Анаэробныедегидрогеназы
3.4.Оксигеназы
3.5.Гидропероксидазы
3.6.Оксидоредуктазы – антиоксиданты
4.2-класстрансферазы
5.3-классгидролазы
6.4-класслиазы
7.5-классизомеразы
7.1.Рацемазы
7.2.Эпимеразы
7.3.Цис-транс-изомеразы
7.4.Внутримолекулярныеоксидоредуктазы
7.5.Внутримолекулярныетрансферазы
8.6-клалигазыс( синтетазы)
8.1.C-C лигазы
8.2.C-N лигазы
8.3.C-S лигазы
8.4.C-O лигазы
9.Задачкидлясамоконтроля
НАЗВАНИЯФЕРМЕНТОВ
Рабочее
1. Субстрат + аза (сахараза, липаза итд)
2. Субстрат + типреакции + аза (лактатдегидрогеназа, пируваткарбоксилаза) –
наиболеечастоприменяется
3.Субстр+синтазат
4.Субстрат+синте аза
Тривиальноеисторич( ) ское
•Нап,три,пепсинм,рен,тромбин
•Недаетпредниосубстратетавления, отипе химическойреакции
Систематическое
•Систематическая классификация была предложена IUBMB (International Union of Biochemistry and Molecular Biology – международныйсоюзбиохимии
имолекубио) логииярной
•Каждыйфермимесвойиндивие-нт
дуальный EC-number (Enzyme
|
commission) илиКФкод(фермента) |
|
• |
Всеферменразбина ты |
7 классов |
• |
Длякаждогокласферментовсаисте- |
|
|
матическоеназваниимеет |
собствен- |
|
нуюформулу |
|
Субстрат + аза
•Карбоксипептидаза
•Амилаза (amylum – крахмал)
•Липаза
•РНКаза
•Альдолаза
•Енолаза
Чащевсеготакназываются |
|
ферменты,которыекатализи- |
|
руютрасщеплениесвязей |
|
(классы – гидролазылиазы |
) |
Продукт + синтаза
•Метионинсинтаза
•Цитратсинтаза
•Аминолевулинатсинтаза
•Гликогенсинтаза
Такназываютсяферменты,которыекатализируютперенгруппыатсомсдновлей
кулынадругуюкласс( трансферазы) Еслимыбудемназыватьэтиферментысо-
ответствииноменклатурой,тометионинсинтазабудетиметьназвание гомоцистеинмети-
лтрансфераза)
Продукт + синтетаза
•Ацил-СоА-синтетаза
•Глутамилсинтетаза
•Аминоацил-тРНК-синтетаза
Такназываютсяферменты,которыекатализируреакциобразо- ют ванияковалентныхсвязеймежду
двумясубстратамикласс( лигазы
(синтетазы) )

4
Поделилвсеферментынак асс |
КЛАССЫФЕРМЕНТОВ |
|
IUBMB (междунарсоюзбиохиммолекудныйи)и логииярной |
||
Основа делеферментовклассыия |
Типкаталбиохимическзируемойреакцииреакционная( й |
|
иликаталитичспецифичность)скаярментов |
||
|
Каждыйклассферимеетсвпенторядковый,котовмерстзакреплогоыйкаждымклассиенего-омбхо
димоза помнить
классовферментов:
Оксидоредуктазы
. Трансферазы 3. Гидролазы
4. Лиазы
5. Изомеразы
6. Лигазысинтетазы( )
7. транслоказы
Каждыйклассделитсянаподподклассы
|
|
Чтоозначаеткодфермента( |
EC-namber)? |
|
EC-namber: 1.1.1.1. – алкоголь: |
NAD+ оксидоредуктаза( |
алкогольдегидрогеназа) |
||
• |
1 |
– классферментаоксидоредуктазы( ) |
|
|
• |
1 |
– подклассферментадействующие( наСН |
-ОНгруппудонора) |
|
• |
1 |
– подпкофермент( дкласс |
NAD+ вкачествеакцепторапротонводорода) |
|
•1 – порядковыйномфергруппемента
CH3 CH2OH + NAD+ ↔CH 3CHO + NADH + H+

5
Чтонужнознатьиуметьприхарактерикаждогоклассаферментов?тике
Знать:
•Типкатализируемойреакцииферментамиданногокласса
•Принципделенияклассанаподклассыипримерыподклассов
•Кафактоикофеферментданымеклане(огтысонестьлиса)в
•Какобрназфуваниеданногтсярментклассаов
•Примерфе еакциимента,которуюон тализирует.Рольданнреакциивобменейвеществ.
Уметь:
• Поназваниюфермопрегосубстратнтаделять |
итипреакции,которуюонкатализирует |
•Побиохимичреакцииопрназваниескойделятьферм,которыйкатализируетнта
1КЛАСС – ОСИДОРЕДУКТАЗЫ
Типкатализируемойреакции |
|
– окислительно-восстановитреакцииперенос( электроновНльные |
+ содногосубстратана |
|||
другой). |
|
|
|
|
|
|
Принципделениянаподклассы |
|
– делениенаподклассыосуществляетзависимоот сяти |
группыдонораи |
видаакцептора |
||
электроновиН |
+. |
|
|
|
|
|
Реакциисучастиемферментовклассаоксидоредуктазы |
|
: |
|
|
||
1. РеакциисучастиемО |
2 вкачествеокис |
лителяакцепто( электиН ронова |
+) |
|
||
a.О2 – акцепторэлеки водроном,ковторыедаотсовотокиединяютсяубстраталяемого
•Оксидазы
•Аэробныедегидрогеназы
b.О2 – встрасубстратиокислстепваетсяегоизменя( окисленияаньтС)ома
•Оксигеназы
2. РеакциибезучастияО |
2 - вкачествеакцептоэл иктводромоновавыступаютркодаферменты( |
NAD+, NADP, FAD, |
FMN) |
|
|
•Анаэробныедегидрогеназы
3. РеакциисучастиемН |
2О2 вкачествеокислитакцепто( эл ипротоновлякт Н+)онова |
Н2О2 преобразуетсявН |
2О |
•Гидропероксидазы
6
|
Оксидоредуктазыделятся |
нагруппы внеструктурыклассификатора(есть |
ненаподклассы |
)В.одн ой группемогут |
находитсяферментыразныхподклассов.: |
|
|
|
|
1. |
Оксидазы |
|
|
|
2. |
Аэробныедегидрогеназы |
|
|
|
3. |
Анаэробныедегидрогеназы |
|
|
|
4. |
Оксигеназы |
|
|
|
5. |
Гидропероксидазы |
|
|
|
Типкатализируемойреакции |
|
ОКСИДАЗЫ |
|
|
– переносэлектрпротонови ддеги( )содногорированиесубстратанадругой. |
|
|||
Акцепторводорода |
|
– О2 |
|
|
Продуреакцииты |
|
– окисленныйсубстрат+вода |
|
|
Кофакторы – Cu2+, Fe3+ (входятсоставАЦфе |
рм,непосредственнонт участвуютпереносе |
электронов) |
||
Названиеферм нтов |
|
– субстрат+оксидаза |
|
|
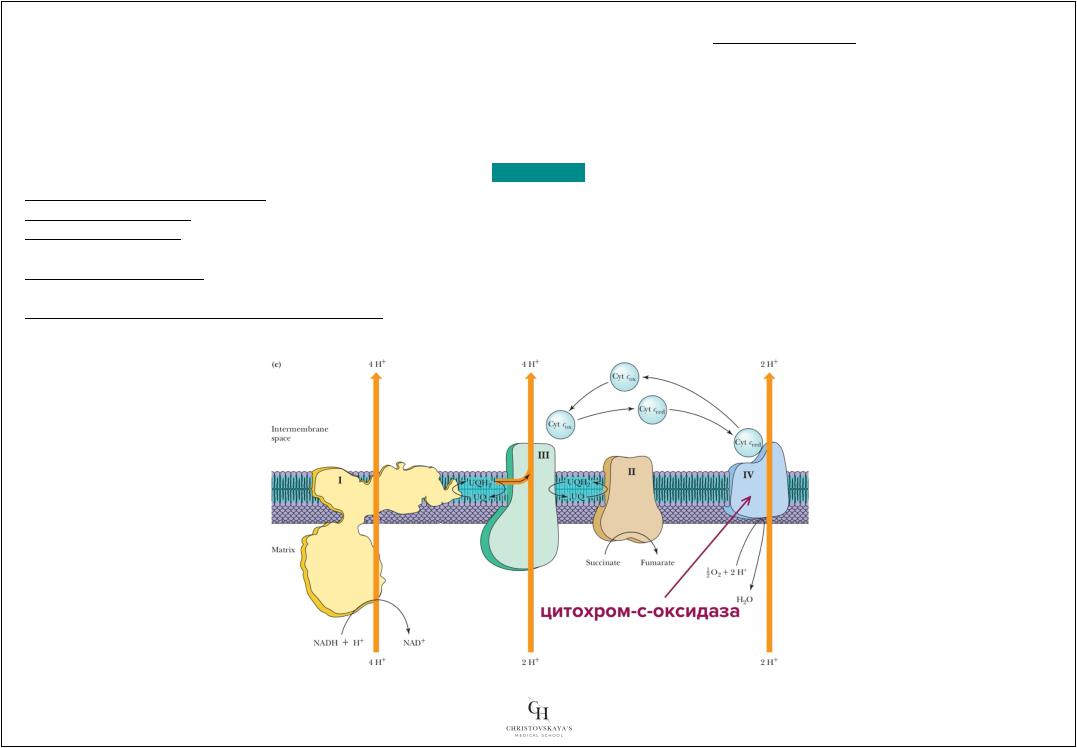
Пример – цитохром-Соксидаза |
|
|
||
Биохимическаярольцитохром |
|
-Соксидазы |
- являепоследнерминальнымт(ся )ферментомпроцессатканевогодыхания |
|
вмитохондриях. |
Катализируетреакциюпереносаэлектронов |
сцитохрСнакисоломабразованиемметаболическойод |
|
|
воды. |
|
|
|
|

7
• Окисленнформацитохромоксидазы( я |
Fe3+) принимаетэлектронотвоссцитанохромавленного |
Сипереходитввос- |
||
становленнуюформу( |
Fe2+) |
|
Fe3+ + e- ↔ Fe2+ |
|
|
|
|
|
|
• Восстановленнаяформазатемвновьокисляется |
|
Fe3+ формумолекукислоярнымодом |
|
|
• Обрактзовавшийсявныйслорприсатома2 водедизиняеткружающейродасреды |
|
Fe2+ +½O 2 ↔ Fe3+ + O- |
образуетсяметаболиче- |
|
|
|
|||
скаявода |
|
|
O- + 2Н + Н2О |
|
|
|
|
|
|
Типкатализируемойреакции |
|
|
АЭРОБНЫЕДЕГИДРОГЕНАЗЫ |
|
- переносэлектрпротоновви ддеги( )содногорированиесубстратанадругой. |
|
|||
Акцепторводорода |
– О2 |
|
|
|
Продуреакцииты |
– окисленныйсубстрат+Н |
2О2 |
|
|
Коферменты – FAD, FMN (простетическиегруппы) |
|
|
||
Кофакторы – ионыметаллов |
|
|
|
|
Название ферментов – субстрат+оксидаза |
|
|
|
|
Пример - ксантиноксидаза (FAD, Mo2+, Fe3+) |
|
|
||
Биохимическаярольксантиноксидазы |
– катализирреакциюкатаболизмапуриновыхетнуклеотидов. |
|
||
|
|
ксантин+ |
O2 + H2O →мочеваякислота+Н |
2О2 |
8
Тип катализируемойреакции |
|
АНАЭРОБНЫЕДЕГИДРОГЕНАЗЫ |
|||
|
- переносэлектрпротоновви ддеги( )содногорированиесубстратанадругой |
||||
Акцепторводорода |
|
– коферменты: |
|
||
§ |
Чащевсего |
– NAD+, NADP+ (провитаминазводныеРРВ( |
3) – никотинкисл) отывой |
||
§ Реже – FAD, FMN (провитаминазводныеВ |
2 – рибофлавина) |
||||
Продуреакцииты |
– окисленныйсубстрат+восстановленныеформыкоферментов( |
NADH+H+, NADPH+H+, FADH2, FMNH2) |
|||
Названиеферм нтов |
|
– субстрат+дегидрогенилиредукт: аза |
|
||
§ |
Субстрат+дегидрогеназа |
– подчеркиваетважную |
рольреакцииокислениясубстрата |
||
§ Субстрат+редук аза |
|
– подчеважнуюрольреакциикиваетвосстановлениясубстрата |
|||
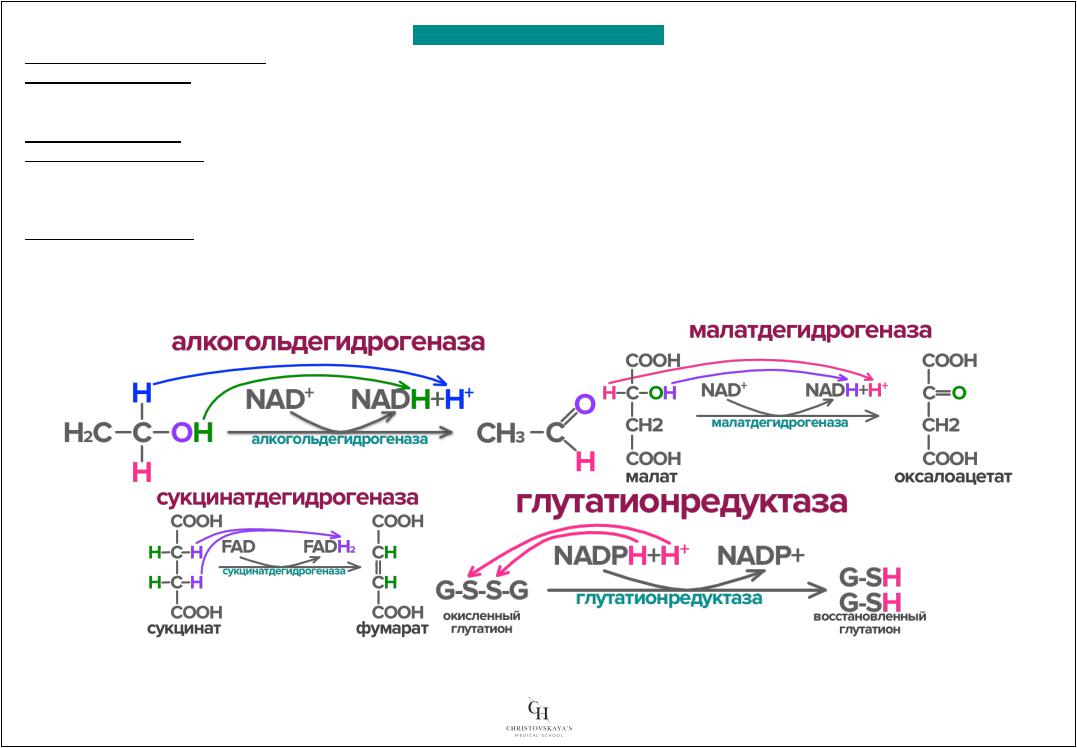
Примеры – алкогольдегидрогеназа, малатдегидрогеназа, сукцинатдегидрогеназа, глутатионредуктаза |
|||||
Биохимическаяроль |
|
: |
|
|
|
§Алкогольдегидрогеназа – фермент,которыйнаходвгепатоцитахучаствуетсядетоксикацииэтанола
§ |
Малатисукцинатдегидрогеназа – фермциклаКребсанты |
|
§ |
Глутатионредуктаза – фермент,котвосстанавливаетрыйокисленнформглутатиона,необходимогоюдля |
безвре- |
|
живанияперекисиводорода |
|
9
Типкатализируемойреакции |
|
|
|
ОКСИГЕНАЗЫ |
|
|
– окислениесубспуптремисоединенияатаодногоилидвухатомовкислородаизмолекулы |
|
|||||
кислмосубстратародалекуле. |
|
|
|
|
|
|
Кофакторы – Fe3+ и Cu2+ |
|
|
|
|
|
|
Коферменты - NADPH+H+,витаминС |
(аскорбиноваякислота) |
,тетрагидробиоптеринН( |
4-БП) |
|||
Видыоксигеназ |
взависимос тиотколичествавключаемыхатомовкислородысубстрат: |
|
|
|||
1. Монооксигеназыгидроксилазы( ) |
|
– включаютмолекулусубстратаатомкисло1 образованиемода |
-ОНгидрок( - |
|||
сильной)группыотсюда( |
второеназвание |
– гидрокс)Второй. атомислородалазывосстанавливает |
ся доН 2Осуча- |
|||
стиемкоферментакакдонатомовНра |
|
|
+ (обычновкачествекоферментавыступает |
NADPH+H+). |
||
2. Диоксигеназы – включаютмолекулусубстратаатома2 кислорода |
|
|
|
|||
Названиеферм нтов |
: |
|
|
|
|
|
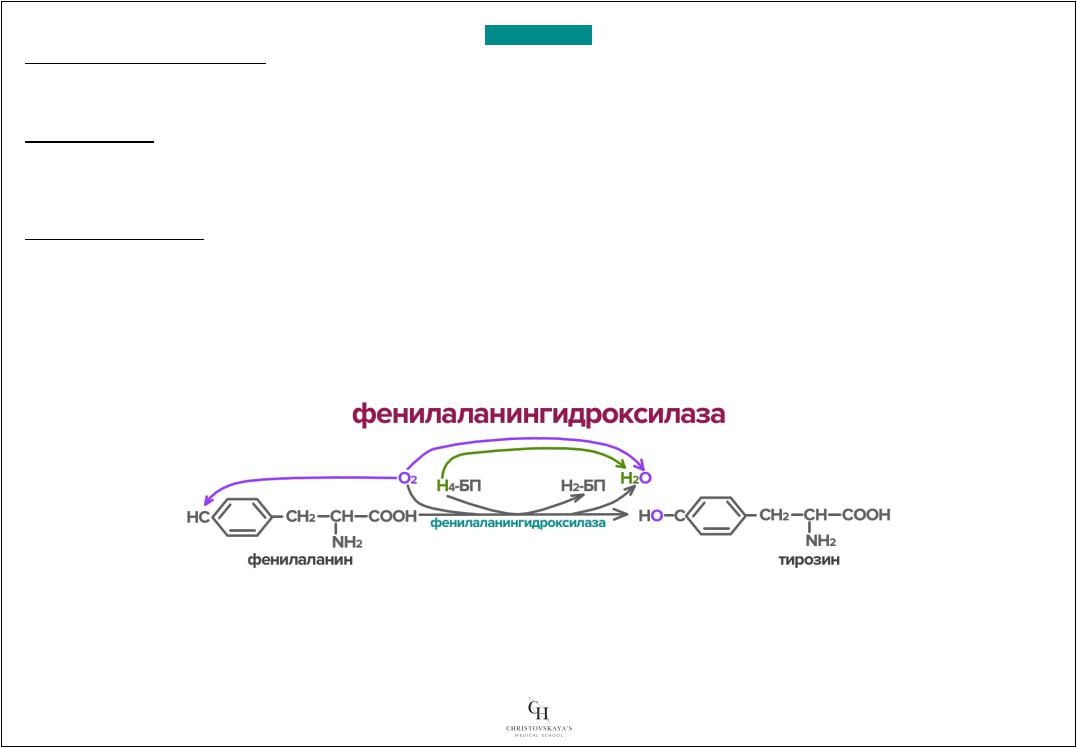
§Монооксигеназы – субстрат+монооксигеназагидроксилаза( )
§Диоксигеназы – диоксигеназа+субстрат Примерыферментихбиохимическаяроль: в
§ |
Фенилаланингидроксилаза – реакцияокислеамифенилаланинаокислотыия |
собразовадругойаминиемокислоты |
||
|
– тирозина.Тирозин |
– условнозаменимАК,к необходитордляаясинтезагорщитовидноймоноважелезы,катехо- |
|
|
|
ламиновнорадреналина( )меланина. |
|
|
|
§ |
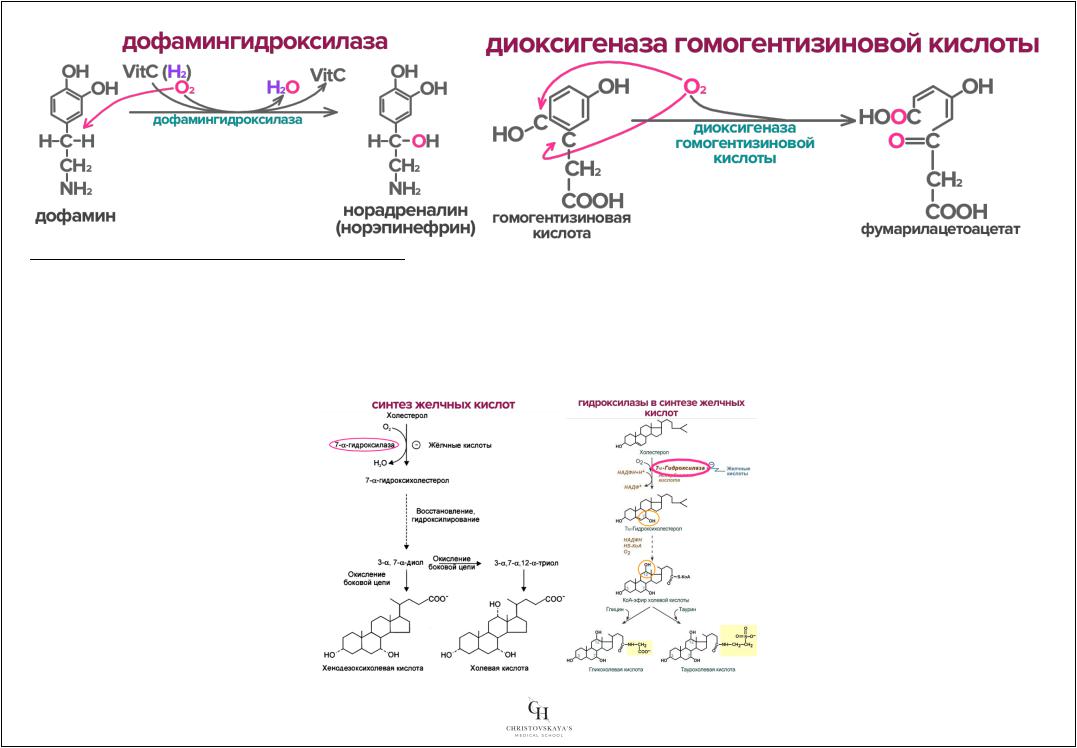
Дофамингидроксилаза – катализреакциюокислдофаминарутния |
собразованиемнорадреналина |
||
§ |
Диоксигеназагомогентизиновойкислоты |
– катализируетоднуреакцийболминокислотытирозиназма |
|
|
10
Рольмонооксиреакцийаворг низменых |
: |
|
|
1. |
Участвуютокисхолениистерола |
собразоважелчныхкисл,котоиемеобходтрыедляассимиляциип щевогоы |
|
|
жира |
|
|
2. |
Окисхолекальцифероланв( таминаД |
3)собразованиемкальцитриола |
– горегулирующего, монаобменкальция |
|
ифосфора |
|
|
3. |
Окислепрегпрогестернение бразованиемлонастерна |
|
оидныхгормоновкортизола( ,альд,п стероналовых |
|
гормонов) |
|
|
4. |
Окисенобиотиковление,вк ючапря степараты,процессеенныеихобезвреживаниячени |
|
|
