
Клинические рекомендации 2023 / Эпилепсия и эпилептический статус у взрослых и детей
.pdf
Комментарий: Имеется несколько мишеней для стимуляции: ANT (переднее ядро таламуса), HP (гиппокамп), CN (центромедианное ядро таламуса), STN (субталамическое ядро), однако наиболее перспективной мишенью признаны передние ядра таламуса (ANT).Стимуляция проводится пациентам в возрасте от 18 до 65 лет [402]. Снизить частоту приступов ≥ 50% после DBSANT удается в среднем у 56% (40,4 – 66%) пациентов, а добиться полного контроля над приступами - у 29% (14 – 40%) [403].
Другие мишени для DBS является менее изученными, имеются немногочисленные публикации с небольшим количеством пациентов. DBSHP - позволяет снизить частоту приступов на 30-90% у пациентов с височной эпилепсией [377], DBSCN -показало эффективность только в отношении генерализованных приступов – снижение приступов на 30-98% [404], DBSSTN в среднем позволяет снизить приступы на 50% [405].
Стереотаксическая радиочастотная деструкция (SRT) эпилептогенных поражений
SRT - локальное малоинвазивное разрушение, применяемое в лечении фармакорезистентной эпилепсии, ассоциированной с глубинными ограниченными эпилептогенными поражениями головного мозга, такими как гипоталамическая гамартома и узловая гетеротопия.
· |
Рекомендуется стереотаксическая радиочастотная деструкция эпилептогенных |
поражений |
(SRT) пациентам с фармакорезистентными формами эпилепсии, которым |
резекционное вмешательство не может быть проведено ввиду большого риска послеоперационных неврологических осложнений, обусловленных локализацией эпилептогенных очагов [406 - 408].
Уровень убедительности рекомендаций – С (уровень достоверности доказательств – 4).
Комментарий: SRT проводится электродом для радиочастотной термодеструкции, доставляемым к эпилептогенному поражению при помощи стереотаксической рамы, что обеспечивает высокую точность деструкции самого очага при минимальном риске повреждения окружающей ткани мозга. Это позволяет безопасно проводить деструкцию локальных глубинно расположенных эпилептогенных очагов [406]. SRT гипоталамических гамартом позволяет достичь контроля над приступами у 71 - 80% пациентов [407]. SRT узловых гетеротопий приводит к снижению частоты приступов > 50% у 48,7% больных [408].
В зависимости от объема эпилептогенного очага и эпилептогенной зоны, их локализации, форм и размеров выбирают тот или иной тип хирургического вмешательства (рис. 6).
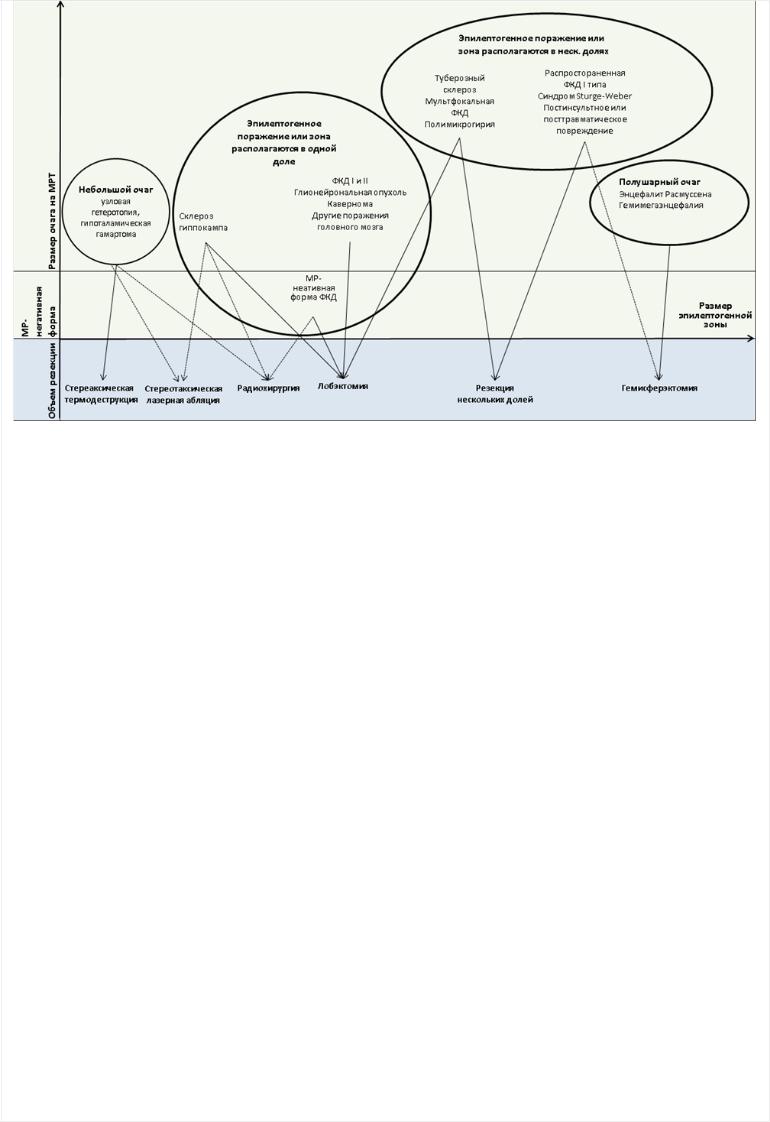
Рис. 6. Схема различных форм хирургического лечения в зависимости от этиологии эпилепсии, объема и локализации поражения, размера эпилептогенной зоны [376].
Использование интраоперационного нейрофизиологического мониторинга во время хирургического лечения фармакорезистентной эпилепсии.
· Рекомендуется проведение интраоперационного нейрофизиологического мониторинга с картированием функций резецируемой коры головного мозга у пациентов с фармакорезистентной фокальной эпилепсией при расположении эпилептогенной зоны вблизи функционально значимой коры или подкорковых проводящих путей [409].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
Комментарий: Применение интраоперационного нейрофизиологического мониторирования (ИОМ) и картирования коры во время резекции эпилептогенной зоны позволяет локализовать функциональные зоны с помощью прямой электростимуляции коры. При расположении эпилептогенной зоны возле моторной коры, проведение электростимуляции возможно во время наркоза, а для проведения картирования речевых зон необходимо пробуждение пациента. У детей локализацию центральной борозды возможно проводить методом соматосенсорных вызванных потенциалов с анализом реверсии фазы над Роландовой бороздой.
Нарушения психики различного спектра весьма частое явление при эпилепсии.
· Рекомендуется консультация врача-психиатра для пациентов с эпилепсией при наличии у него коморбидных психических расстройств, поведенческих, эмоциональных, когнитивных нарушений [6].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).

· |
Рекомендуется назначение антидепрессантов из группы селективных ингибиторов |
обратного захвата серотонина (СИОЗС) для лечения депрессивного расстройства у ПЭ старше
18 лет [410, 411].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 3).
Комментарий: Общие подходы к лечению депрессий у ПЭ аналогичны таковым у пациентов с депрессией без эпилепсии. Результаты проспективного открытого исследования показали, что на фоне приема СИОЗС 7 из 8 пациентов с эпилепсией и депрессией к 12 неделе терапии достигают ремиссии [411]. При недостаточной эффективности СИОЗС целесообразно рассмотреть вопрос о назначении антидепрессантов из других групп.
· Рекомендуется назначение пароксетина** пациентам с эпилепсией 18 лет и старше при наличии депрессии [412, 413].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: Результаты рандомизированного контролируемого сравнительного исследования пароксетина** в дозе 20 - 40 мг в сутки и других антидепрессантов, проведенного на 67 ПЭ и депрессией показали, что в течении 8 недель терапии, 82% достигли первичного ответа на лечение [412]. При этом из группы пароксетина** не выбыл ни один человек.
· Рекомендуется назначение циталопрама пациентам с эпилепсией 18 лет и старше при наличии депрессии [414–416].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
Комментарии: В открытом проспективном исследовании 43 ПЭ и депрессией было показано, что на прием циталопрама в дозировке 10 - 40 мг в сутки в течении 8 недель ответило 65% ПЭ и депрессией [414]. В 16-недельном исследовании 45 ПЭ и депрессией похожего дизайна уровень ответа на терапию циталопрамом составил 86%. [415]. В проспективном открытом исследовании циталопрама, проведенного на пациентах с височной эпилепсией и депрессией, показано, что уровень ответа на терапию составил 53,3%, а 21,2% пациентов достигли ремиссии к 20 - 30 неделе терапии [416]. Ни в одном из приведённых выше исследований прием циталопрама не сопровождался учащением приступов.
· Рекомендуется назначение сертралина** пациентам с эпилепсией старше 18 лет при наличии депрессии [417, 418].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
Комментарии: В рандомизированном исследовании сертралина** и когнитивно-поведенческой психотерапии было показано, что на фоне приема сертралина** в дозе 50 - 200 мг в сутки (N = 75) к 16 неделе терапии ремиссии достигли 53% пациентов [417]. Ни у одного пациента прием сертралина** не сопровождался учащением приступов. В течении 12 месяцев наблюдения за

100 пациентами с эпилепсией с депрессивными/обсессивными расстройствами (97/3) на фоне приема сертралина** лишь у 6 пациентов отмечалось учащение приступов, при этом причинную связь между приемом сертралина** и учащением приступов авторы смогли выявить лишь у одного пациента [418].
· Рекомендуется назначение венлафаксина для лечения депрессивного расстройства пациентам с эпилепсией 18 лет и старше [419, 420].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарий: В результате рандомизированного контролируемого исследования было установлено, что в течении 8 недель терапии значимо большее число пациентов, получавших венлафаксин (25 - 75 мг в сутки) достигли первичного ответа на терапию по сравнению с теми, кто не получал какого-либо лечения депрессии (69% vs 19%). При этом авторами не проводилась оценка влияния венлафаксина на эпилептические приступы [419].
· Рекомендуется назначение миртазапина для лечения депрессивного расстройства у пациентов с эпилепсией 18 лет и старше [416, 420].
Уровень убедительности рекомендаций C (уровень достоверности доказательств – 5).
Комментарий: По данным проспективного открытого исследования назначение миртазапина в средней дозе 32,2 (6,8) мг в сутки привело к уменьшению симптомов депрессии у 51,9%, а около 15% достигли ремиссии к 20 - 30 неделе терапии [416]. Прием миртазапина не сопровождался учащением приступов.
· Не рекомендуется назначение амитриптилина** для лечения депрессивного расстройства у ПЭ 18 лет и старше [421].
Уровень убедительности рекомендаций В (уровень достоверности доказательств – 2).
Комментарий: В результате двойного слепого плацебо контролируемого исследования к 6 неделе терапии не было выявлено значимых различий по уровню ответа на 25 мг амитриптилина** и плацебо [421].
· Не рекомендуется назначение кломипрамина** для лечения депрессивного расстройства у ПЭ 18 лет и старше [422].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4).
Комментарий: результаты метанализа [422] показали, что кломипрамин** ассоциирован с повышенным риском эпилептических приступов у людей, не болеющих эпилепсией, со стандартизированным показателем заболеваемости 4 (95% CI 2,6 - 6,0).
· Рекомендовано при назначении антидепрессантов пациентам с эпилепсией и депрессией 18 лет и старше учитывать их лекарственные взаимодействия с противоэпилептическими препаратами [410].

Уровень убедительности рекомендаций С (уровень достоверности доказательств – 3).
Комментарии: карбамазепин**, фенитоин** и фенобарбитал** снижают концентрации СИОЗС примерно на 25% [423], а вальпроевая кислота** незначительно повышают концентрацию активного метаболита венлафаксина - О-десметилвенлафаксин [424]. Флувоксамин, флуоксетин** и в меньшей степени сертралин** незначительно повышают концентрацию вальпроевой кислоты** [425, 426]. Некоторым пациентам может потребоваться изменение режима дозирования ПЭП.
· |
Рекомендуется взрослым пациентам c эпилепсией с симптомами тревоги проведение |
когнитивно-поведенческой психотерапии [427, 428]. |
|
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 4). |
|
· |
Рекомендуется взрослым пациентам c эпилепсией и в зависимости от вида тревожных |
расстройств назначение антидепрессантов из группы СИОЗС (сертралин**, пароксетин**, флувоксамин, циталопрам, эсциталопрам, флуоксетин**) в качестве препаратов первой линии
[430].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: Терапия антидепрессантами из группы СИОЗС безопасна для пациентов с эпилепсией, так как они не влияют на частоту эпилептических приступов. Тем не менее, стоит учитывать возможные лекарственные взаимодействия с ПЭП, которые среди СИОЗС наиболее выражены у пароксетина**.
Рекомендуемая суточная дозировка сертралина** – 50 - 150 мг в сутки, циталопрама и пароксетина** – 20 - 60 мг в сутки, эсциталопрама – 10 - 20 мг в сутки, флуоксетина** – 20 - 40 мг в сутки, флувоксамина – 100 — 300 мг в сутки. Обычно начинают с минимальных терапевтических доз, поднимая их при отсутствии эффекта.
· Рекомендуется пациентам c эпилепсией старше 18 лет и генерализованным тревожным расстройством назначение прегабалина** [431].
Уровень убедительности рекомендаций С (уровень достоверности доказательств – 5).
Комментарии: механизм действия препарата заключается в связывании с альфа-2-дельта- субъединицей потенциалзависимых кальциевых каналов, что блокирует передачу болевых импульсов и снижает вероятность судорожных приступов, связывает пресинаптические N и P/Q кальциевые каналы, уменьшая их чрезмерную активность, таким образом снижая проявления тревожной симптоматики. Режим дозирования для лечения генерализованного тревожного расстройства: начальная доза — 150 мг/сут. В зависимости от достигнутого эффекта и переносимости, через одну неделю дозу можно увеличить до 300 мг/сут. Длительное применение препарата безопасно для пациента. Побочными эффектами прегабалина** являются такие явления, как: седация, головокружение, тремор, дизартрия, парестезии, нарушение памяти, нарушение координации, нарушение внимания, спутанность

сознания, эйфория, раздражительность, сухость во рту, запор, увеличение веса, повышенный аппетит, метеоризм, помутнение зрения, диплопия, периферические отеки, снижение либидо, эректильная дисфункция.
Паллиативная помощь – подход, целью которого является улучшение качества жизни пациентов и членов их семей, оказавшихся перед лицом угрожающего жизни заболевания. Эта цель достигается путем предупреждения и облегчения страданий благодаря раннему выявлению, тщательной оценке и купированию боли и других тягостных физических симптомов, а также оказанию психосоциальной и духовной поддержки [432]. Главная задача паллиативной помощи
– достижение, поддержка, сохранение и повышение, насколько это возможно, качества жизни пациента. Однако определить, что такое «качество жизни», может только сам пациент, нуждающийся в паллиативной помощи [433].
· Рекомендуется оказание паллиативной медицинской помощи детям с формами эпилепсии, относящимися к заболеваниям, ограничивающим продолжительность жизни (коды МКБ G 40.4, G 40.5, G 40.9) [268–270] и детям с фармакорезистентной эпилепсией, которым выполнены паллиативные нейрохирургические вмешательства (каллозотомия и субпиальные транссекции) [271, 272], осуществляемой сотрудниками медицинских организаций и их подразделений, оказывающих специализированную паллиативную медицинскую помощь детям, для обеспечения потребностей пациента и его законных представителей.
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
· Рекомендуется введение защечного раствора мидазолама детям при эпилептическом статусе для купирования приступа судорог [434].
Уровень убедительности рекомендаций C (уровень достоверности доказательств - 5).
· |
Рекомендуется введение ректального раствора диазепама детям при эпилептическом |
статусе для купирования приступа судорог [434].
Уровень убедительности рекомендаций C (уровень достоверности доказательств 5).
К наблюдению за детьми с формами эпилепсии, относящимися к заболеваниям, ограничивающим продолжительность жизни (коды МКБ G 40.4, G 40.5, G 40.9) и детям с фармакорезистентной эпилепсией, которым выполнены паллиативные нейрохирургические вмешательства (каллозотомия и субпиальные транссекции), должны привлекаться сотрудники медицинских организаций и их подразделений, оказывающих специализированную паллиативную медицинскую помощь детям.
Паллиативная помощь детям с эпилепсией оказывается на основании соответствующих нормативных документов (см. Приложение «Связанные документы»).
3.5 Кетогенная диета

Кетогенная диета (КД) - это хорошо зарекомендовавший себя нефармакологический метод лечения детей и взрослых с лекарственно-устойчивой эпилепсией, который основывается на изменении рациона с увеличением доли жиров и уменьшением углеводов и белков. Из-за очень высокой потребности в жирах классическую КД может быть трудно поддерживать, что приводит к необходимости использовать ее альтернативные варианты. Модифицированная КД, по-видимому, почти так же эффективна, но обеспечивает больший выбор продуктов питания. Различные альтернативы КД включают модифицированную диету Аткинса (МДА), диету со среднецепочечными триглицеридами (ДСЦТ) и терапию с низким гликемическим индексом (НУД или низкоуглеводная диета) [435].
Типы КД
(1)Классическая КД состоит преимущественно из жиров (до 90%) и низкого содержания углеводов и белков, что приводит к кетозу и имитирует состояние голодания. Это жесткая диета, рассчитывается математически для каждого пациента индивидуально. Из-за ограничения рациона пациенту необходимо обеспечивать организм достаточным количеством витаминов и минералов.
(2)МДА направлена на обеспечение разнообразия продуктов и вкусовых качеств с соотношением жиров к углеводам и белку 1 : 1 и содержит около 65% жира, 25% белка и 10% углеводов. Поощряется употребление жиров, а потребление углеводов ограничивается до 10 – 20 г/день для детей и 15 – 20 г/день для взрослых. МДА не требует взвешивания пищи на граммовых весах или ограничения калорий, белков или жидкостей и может быть хорошим вариантом для пациентов, которые не могут переносить более строгую диету, такую как классическая КД. При МДА рекомендуется прием поливитаминов с низким содержанием углеводов и карбоната кальция.
(3)НУД основана на соотношении жира к углеводам и белку 0,6 : 1, содержит 60% жиров, 30% белка и 10% углеводов с низким гликемическим индексом (ГИ), ГИ < 50. ГИ измеряет тенденцию еды повышать уровень глюкозы в крови по сравнению с эквивалентным количеством эталонного углевода (глюкозы). По сравнению с классической КД, НУД дает меньшее повышение уровня кетоновых тел, но имеет сопоставимую эффективность, лучшую переносимость и более простую реализацию.
· |
Рекомендуется |
применение кетогенной диеты |
детям |
с любой формой |
||
фармакорезистентной |
эпилепсии |
при |
неэффективности |
обычно |
применяемых |
|
противоэпилептических препаратов с целью альтернативного лечения эпилепсии [349, 535].
Уровень убедительности рекомендаций А (уровень достоверности доказательств – 1).
Комментарии: Кетогенная терапия не должна быть терапией «отчаяния». Кетогенную диету следует рассмотреть как лечебную опцию у детей после неэффективности двух противоэпилептических препаратов, а при некоторых синдромах эпилепсии (при синдроме дефицита GLUT1 и пиридоксин-зависимой эпилепсии), как можно раньше.

Показания [436]
КД считается золотым стандартом для лечения метаболических заболеваний, таких как синдром дефицита белка-переносчика глюкозы 1 (GLUT-1) и дефицит пируватдегидрогеназы. В настоящее время КД показала высокую эффективность относительно лечения синдрома Веста. КД также может использовался при других эпилептических синдромах и является важным альтернативным лечением для пациентов с лекарственно-устойчивой эпилепсией, которые не являются кандидатами на хирургическое лечение.
Эпилептические синдромы с вероятной эффективностью КД: синдром Ангельмана,
митохондриопатии с нарушением комплекса 1, синдром Драве, МАЭ (синдром Доозе), синдром дефицита белка-переносчика глюкозы 1 (Glut-1), синдром эпилепсии, связанный с фебрильной инфекцией (FIRES), дети или младенцы на искусственном вскармливании (исключительно), инфантильные спазмы, синдром Отахара, дефицит пируватдегидрогеназы, суперрефрактерный эпилептический статус, туберозный склероз.
Эпилептические синдромы с возможной эффективностью КД: дефицит аденилосукцинатлиазы, CDKL5-энцефалопатия, ДАЭ, пороки развития головного мозга, эпилепсия младенчества с мигрирующими фокальными приступами, эпилептическая энцефалопатия с продолженной спайк-волновой активностью во сне (CSWS), гликогеноз типа V,ЮМЭ, болезнь Лафора, синдром Ландау - Клеффнера, синдром Леннокса - Гасто, дефицит фосфофруктокиназы, синдром Ретта, подострый склерозирующий панэнцефалит.
Абсолютные противопоказания
Дефицит карнитина (первичный), дефицит карнитин-пальмитоилтрансферазы (CPT) I или II, дефицит карнитинтранслоказы, β-окислительные дефекты, дефицит среднецепочечной ацилдегидрогеназы (MCAD), дефицит длинноцепочечной ацилдегидрогеназы (LCAD), дефицит короткоцепочечной ацилдегидрогеназы (SCAD), дефицит длинноцепочечного 3-гидроксиацил- КоА, дефицит среднецепочечного 3-гидроксиацил-КоА, дефицит пируваткарбоксилазы, порфирия.
К относительным противопоказаниям относятся неспособность поддерживать полноценное питание, возможное хирургическое лечение эпилепсии, низкая приверженность диеты родителями или опекуном, одновременное применение пропофола.
Подготовка к введению КД
Перед тем, как начать диету, пациент должен вести дневник приступов, чтобы установить параметр их частоты. Необходимо провести общий анализ крови с тромбоцитами, электролиты, КЩС включая бикарбонат сыворотки, общий белок, кальций, цинк, селен, магний и фосфаты, биохимический анализ крови (включая альбумин, аммиак и креатинин), липидный профиль натощак, ацилкарнитиновый профиль в сыворотке крови, общий анализ мочи, кальций и креатинин в моче, концентрацию противоэпилептического препарата, уровень витамина D.

Определение органических кислот в моче и аминокислот в сыворотке крови рекомендуются в случае неясной природы эпилепсии.
Также необходимы ЭЭГ и МРТ головного мозга. В случае риска нефролитиаза необходимо сделать УЗИ почек; электрокардиограмма и ультразвуковое исследование сонной артерии считаются необязательными. Оценка питания включает пищевой дневник, включая отчет о питании за 3 дня, пищевые привычки, аллергию, отвращение и непереносимость. Исходный вес, рост и идеальный вес для роста и индекса массы тела (ИМТ) необходимы для расчета кетогенного соотношения, калорий и потребления жидкости. Состав диеты следует подбирать в соответствии с возрастом пациента и способом кормления.
Методика проведения КД
Цель терапии состоит в том, чтобы достичь соотношения четырех частей жира к одной порции белка и углеводов, описываемого как «4 : 1». Чтобы достичь этого уровня, можно использовать один из двух подходов, с голоданием или без него. При первом подходе пациент должен быть госпитализирован на 12 – 48 часов или при наличии кетонов в моче, чтобы предотвратить развитие гипогликемии и обезвоживания. Этот метод имеет тенденцию ускорять развитие кетоза, хотя может вызвать больший стресс у пациента. Когда достигается кетоз, питание рассчитывается так, чтобы поддерживать постоянное соотношение КД.
Последний подход не требует госпитализации, и коэффициент КД поэтапно увеличивается еженедельно с 1 : 1, 2 : 1 и 3 : 1 до 4 : 1. Большая часть литературы предполагает, что нет значительной разницы между двумя подходами с точки зрения времени, необходимого для достижения кетоза и возникновения гипогликемии, поэтому в настоящее время пациенты, как правило, не голодают перед началом КД.
Принимая во внимание, что КД обеспечивает лишь небольшое количество фруктов, овощей, зерна, молока и сыра, необходимы пищевые добавки: мультивитаминные и минеральные комплексы с низким содержанием углеводов следует принимать ежедневно. К основным пищевым добавкам, необходимым для всех пациентов любого возраста, относят мультивитамины с минералами (включая микроэлементы, особенно селен), препараты кальция, витамин D и его аналоги (в соответствие с суточной потребностью, реже рекомендуют выше рекомендованной суточной нормы цитраты для перорального применения, слабительные средства для профилактики или лечения (лаурилсульфоацетат натрия, минеральное масло, глицериновые свечи), дополнительные селен, магний, цинк, фосфор, железо, медь, карнитин, масло MCT или кокосовое масло, соль (старше 1 года).
Фонд Чарли (Charlie Foundation) разработал программу «KetoDietCalculator», чтобы помочь специалистам и лицам, осуществляющим уход, управлять диетической терапией. Эта онлайнбаза данных рассчитывает планы питания для всех возрастов, от младенцев до взрослых, от твердой пищи до жидких смесей, и доступна в Интернете и на мобильных устройствах по ссылке http://www.ketodietcalculator.org.
Наблюдение

Пациентов, придерживающихся КД, следует регулярно осматривать каждые 3 месяца, и члены семьи или опекун должны иметь доступную связь с командой диетологов, чтобы разрешить возможные сомнения и обсудить побочные эффекты. При каждом визите следует оценивать дневник приступов, а также когнитивное развитие и поведение ребенка.
При посещении клиники необходимы следующие обследования: оценка питания (дипломированный диетолог), роста, веса, идеальный вес для ИМТ, при необходимости - окружность головы у младенцев; оценка соответствия рецептов, используемых семьей или опекуном, рассчитанным калориям, белкам и жидкости; пересмотр дополнительных витаминных и минеральных добавок; оценка приверженности КД.
При необходимости – изменение схемы рациона для улучшения приверженности диетическому лечению и контроля над приступами.
Также необходимы: неврологический осмотр, оценка побочных эффектов КД, решение об изменении количества ПЭП (если применимо), оценка целесообразности дальнейшего продолжения КД. К лабораторной оценке относится общий анализ крови с тромбоцитами, электролиты, КЩС, включая бикарбонат сыворотки, общий белок, кальций, цинк, селен, магний
ифосфаты, биохимический анализ крови (включая альбумин, аммиак и креатинин), липидный профиль натощак, ацилкарнитиновый профиль в сыворотке крови, общий анализ мочи, кальций
икреатинин в моче, концентрацию ПЭП, уровень витамина D. ЭЭГ проводится для оценки эффективности КД или при рассмотрении вопроса о прекращении КД. При длительном нахождении на КД рекомендуется исследование минеральной плотности костной ткани (сканирование DEXA) через 2 года от начала КД.
Следует помнить, что для достижения эффективности КД требуется период не менее 3 месяцев с момента достижения пациентом кетоза, поэтому важно побудить пациента и его семью продолжать диету в течение этого периода без изменения лекарства.
Отмена КД
Как указывалось ранее, КД следует использовать в среднем как минимум 3 месяца, чтобы сделать справедливую оценку эффективности терапии, прежде чем рассматривать вопрос о прекращении лечения. Если приступы учащаются через 1 - 2 недели после начала КД, диету следует немедленно прекратить.
Если семья решает оставить своего ребенка на КД более 6 месяцев, несмотря на отсутствие очевидного контроля над приступами, решение в конечном итоге остается за ними и должно поддерживаться до тех пор, пока будут отслеживаться и устраняться побочные эффекты.
У детей со снижением частоты приступов более чем на 50% КД прекращают ориентировочно через 2 года; однако у детей, у которых контроль приступов почти завершен (например, снижение приступов более чем на 90%) и побочные эффекты незначительны, КД можно продолжать в течение нескольких лет.
