
3873
.pdf
Исследования токсичности исходных и обработанных осадков сточных вод (на биотестах) проводились по стандартным методикам в лаборатории экологической и промышленной токсикологии Нижегородского государственного университета им. Лобачевского; в группе цитогенетической безопасности лаборатории радиационной экологии ИТЭБ РАН. Эксперименты по выращиванию растительной продукции проводились в стеллаже оранжереи ИФПБ РАН и лаборатории ННГАСУ.
Втретьей главе приведены результаты экспериментальных исследований по обезвреживанию осадков городских сточных вод.
Всоответствии с поставленными задачами были проведены следующие исследования: определены характеристики исходного ОГСВ станции аэрации города Нижнего Новгорода; изучены свойства предлагаемых реагентов и эффективность обезвреживания ОГСВ; установлены оптимальные параметры процесса обезвреживания ОГСВ; изучены санитарно-гигиенические и токсикологические характеристики обезвреженного ОГСВ; установлена возможность и эффективность использования обезвреженного ОГСВ в качестве почвоулучшающей добавки при рекультивации нарушенных грунтов, в зеленом строительстве и в сельском хозяйстве.
Для определения доз реагента ММЭ-Т |
использовался |
исходный |
||
сброженный осадок (рН=7,1 - 7,4; влажность |
~ |
98%) |
и обезвоженный с |
|
применением флокулянта Praestol 611 осадок |
(влажность ~ 80%), |
содержащий |
||
представителей патогенной микрофлоры и жизнеспособные яйца гельминтов. |
||||
Согласно результатам исследований (рис. |
1), |
доза |
реагента, при которой |
|
начинает происходить гибель микрофлоры и яиц гельминтов, составляет соответственно 2,5 и 5 ммоль/кг сух.в-ва. Гибель 100% бактерий наступает при дозе 15-17,5 ммоль/кг сух.в-ва; гибель 100% яиц гельминтов наступает при дозе 17,5-20 ммоль/кг сух.в-ва.
В процессе исследований замечено, что после добавления комплексов в количествах более 15 ммоль/кг сух.в-ва у осадка снижается интенсивность специфического фекального и гнилостного запаха и появляется запах прелой земли, что объясняется снижением интенсивности процессов брожения.
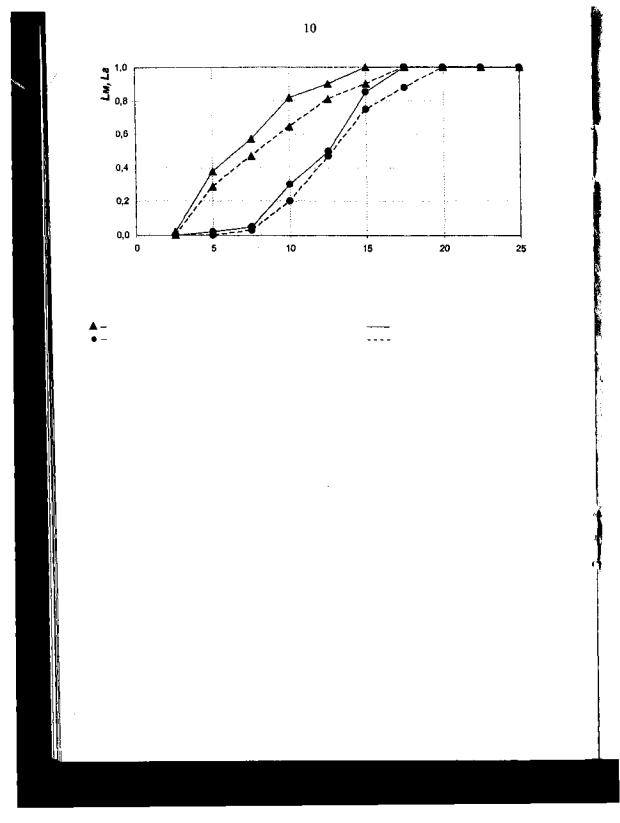
Доза реагента, ммоль/кг в пересчете на сух. вещество
Рис. 1. Зависимость доли нежизнеспособных яиц гельминтов и микроорганизмов от дозы вносимого в осадок реагента ММЭ-Т:
LM, доля нежизнеспособных микроорганизмов; |
- |
Влажность |
осадка -80%; |
Lr, доля нежизнеспособных яиц гельминтов; |
- |
Влажность |
осадка -98% |
Организмы подавленной микрофлоры слипаются в друзы и |
сжимаются. |
||
Яйца гельминтов изменяют форму или «стекают». Погибшие микроорганизмы окрашены в голубой или в синий цвет. Жизнедеятельность микроорганизмов и яиц гельминтов не возобновляется.
При изучении кинетики процесса обеззараживания пробы осадка обрабатывались дозой реагента, дающей 100%-ный эффект обеззараживания (20 ммоль/кг сух.в-ва). Результаты определения доли погибших яиц гельминтов и микрофлоры после экспозиции представлены на рисунке 2. В результате исследований определено, что при установленной дозе полная дезактивация яиц гельминтов происходит через 35-40 минут. Подавление патогенной микрофлоры на 100% завершается за 20-25 минут.
Известно, что при определенных избытках анионов аминокислот гидроксоаминокислотные комплексы меди могут частично разлагаться, поэтому совместное введение реагентов ММЭ-Т и АК-ЗЭ неэффективно. Для определения временного разрыва между дозированием реагентов в осадок через разные промежутки времени после введения реагента ММЭ-Т была добавлена расчетная доза реагента АК-ЗЭ (в количестве 0,12 ммоль/кг сух.в-ва).
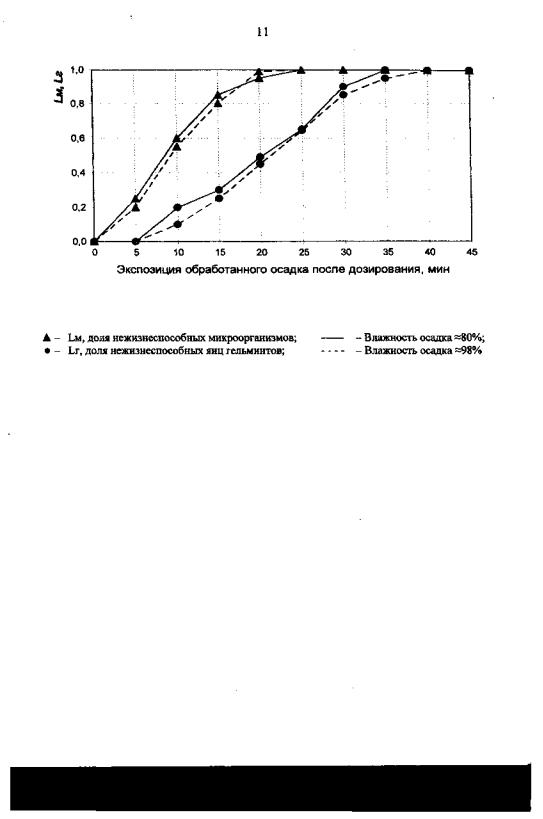
Рис. 2. Зависимость доли погибшей микрофлоры и яиц гельминтов от времени действия реагента ММЭ-Т (доза реагента 20 ммоль/кг сух.в-ва):
Результаты эксперимента показали, что дозирование детоксицирующего реагента в осадок через 10 и более минут после обработки реагентом ММЭ-Т не оказывает существенного влияния на завершение процесса обеззараживания осадка.
Для построения математической модели процесса дегельминтизации, а также для определения влияния температуры и влажности проводилось планирование полнофакторного эксперимента 2(4-0). В качестве зависимой переменной выступала доля погибших яиц гельминтов (Lг). Полученные результаты представлены в виде математической модели процесса, которая описывается уравнением
Lг = 0,3827 + 0,0033 · d . τ- 0,0269 · d - 0,0231 · τ + 0,0009 · t - 0,0024 · w , (2)
где d - доза реагента ММЭ-Т; τ - время действия реагента; t - температура реакционной среды; w - влажность осадка.
На первом этапе исследований процессов детоксикации ионов тяжелых металлов изучалось образование аминокислотных комплексов металлов на

12
модельных растворах ТМ; определялась эффективность детоксикации с использованием биотестов на обработанных детоксицирующим реагентом
модельных растворах.
Взаимодействие композиции АК-ЗЭ (жидких гидратов натриевых солей
аминокислот) с ионами металлов происходит в соответствии с реакциями |
|
Ме2+ + 2L- -> |MeL2 (для Me = Со2+, Рb2+, Ni2+, Cu2+, Zn2+, Cd2+); |
(3) |
Cr3++3L-->|CrL3 . |
(4) |
Растворы солей, в которых концентрация анионов аминокислот недостаточна для полного связывания ионов металлов в нерастворимый комплекс, будут нейтральными или слабокислыми, поэтому связывание ионов металлов в нерастворимые комплексы сопровождается скачком или повышением рН, что подтверждено экспериментальными данными, представленными на рисунке 3. Графики рН-метрического титрования растворов солей металлов композицией АК-ЗЭ имеют точку перегиба. Для Со2+, Ni2+, Cu2+, Zn2+, Cd2+ и Рb2+ этой точке отвечает значение СL/СМ ~2, а для Сг3+ - СL /СМ ~3. После точки перегиба наблюдается скачок рН, свидетельствующий о завершении процесса комплексообразования.
Рис. 3 Результаты рН-метрического титрования растворов нитратов металлов композициейАК-ЗЭ:
СL-концентрация анионов аминокислот, моль; См-концентрация ионов металлов, моль. Металлы: 1-Сг 3+ ,2-Со2+, 3-Ni2+, 4-Cu2+, 5-Zn2+,6-Cd2+, 7-Pb2+

13
При взаимодействии ионов металлов с композицией натриевых солей аминокислот образуется сложная смесь однородных и смешанных соединений - малорастворимых комплексов - CrL3, NiL2, CuL2, ZnL2, CdL2, MnL2, PbL2.
Согласно значениям констант устойчивости эти комплексы образуются практически со 100%-ным выходом при соотношении Μ : L = 1 : 3 для CrL3 и
1 : 2 для других комплексов.
Необходимое количество анионов аминокислот (V, моль/кг сух.в-ва), требуемых для связывания всех катионов тяжелых металлов, рассчитывается по формуле
(5)
где Me - металл, подлежащий детоксикации, Ме={1, 2, ... N};
N - число тяжелых металлов, подлежащих детоксикации, в осадке; |
|
||
тме |
- масса металла Me, в пересчете на сухое вещество осадка, мг/кг; |
|
|
ММе |
- молярная масса металла Me, мг/моль; |
|
|
λΜe - валентность металла Me. |
|
|
|
Содержание тяжелых металлов в осадке определяли по стандартной |
|||
методике на атомно-абсорбционном спектрофотометре. |
|
||
Содержание тяжелых металлов в пробе сброженных осадков городских очистных |
|||
|
сооружений Г.Н.Новгорода, мг на 1 кг сухого вещества: |
|
|
кадмий |
16,4 |
никель |
345,1 |
кобальт |
3,2 |
свинец |
125,5 |
марганец |
480,3 |
цинк |
2120 |
медь |
425,1 |
хром |
702,4 |
Расчетная доза детоксицирующего реагента АК-ЗЭ составляет 0,15 моль/кг сухого в-ва осадка. При использовании 1-молярного реагента АК-ЗЭ расчетная доза для осадка влажностью ~98% составляет 3 мл на 1 литр

14
влажного осадка; для осадка влажностью ~80% - 30 мл. Результаты исследований процесса детоксикации тяжелых металлов реагентом АК-ЗЭ могут быть проиллюстрированы (рис. 4).
На рисунке 4-а график рН-метрического титрования имеет точку перегиба при введенной дозе реагента более 3 ммоль/л. При увеличении дозы наблюдается резкое повышение рН. Таким образом, можно сделать вывод о том, что при введении реагента в количестве меньшем расчетной дозы все количество реагента расходуется на связывание металлов в аминокислотные комплексы.
рН
а)
|
|
Рис. 4. Графики рН- |
|
|
метрического титрования |
|
|
осадкареагентомАК-ЗЭ: |
|
|
а) - для сброженного |
|
|
осадка влажностью ~98%; |
|
Количество реагента, ммоль/л |
б) - для сброженного |
|
б) |
осадка влажностью ~80%; |
рН |
1 - осадок, обезвоженный |
|
|
||
|
|
без применения флокулянта; |
|
|
2 - осадок, обезвоженный с |
|
|
применением флокулянта |
Количество реагента, ммоль/л
При превышении расчетной дозы в результате гидролиза натриевых солей аминокислот происходит повышение рН, причем избыток анионов аминокислот остается незадействованным в реакциях комплексообразования. Графики
15
титрования композицией АК-ЗЭ осадка, обезвоженного с применением флокулянта и без него, практически совпадают (рис. 4-6). Это свидетельствует о том, что полиакриламидный флокулянт незначительно влияет на реакции образования аминокислотных комплексов в результате снижения скорости прохождения реакции из-за плохого доступа реагента в образовавшиеся хлопья осадка.
На основании определения количества аминокислотных комплексов ТМ и свободных анионов аминокислот установлено, что мольное содержание аминокислотных комплексов каждого металла в осадке после обработки композицией АК-ЗЭ практически совпадает с мольным содержанием соответствующих металлов в осадке до обработки, что свидетельствует об образовании аминокислотных комплексов непосредственно в частицах осадка.
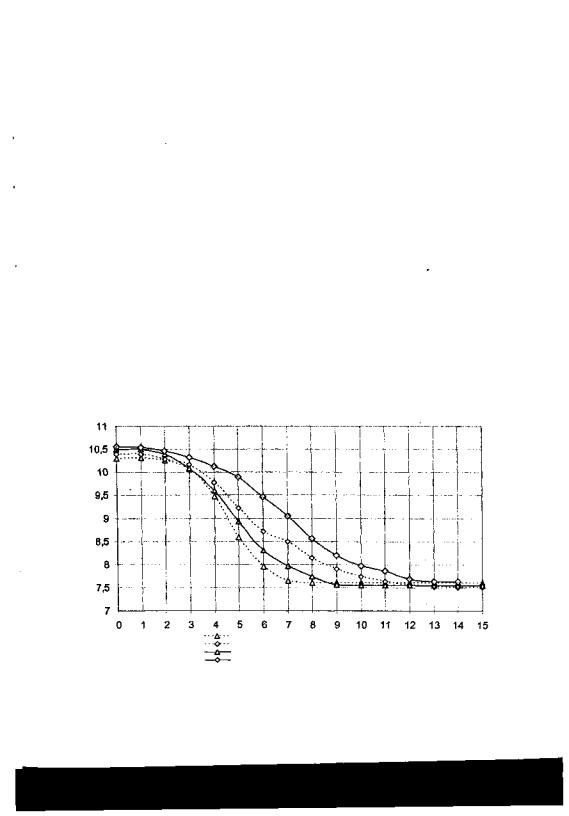
При исследования кинетики процессов комплексообразования проводили единовременные дозирования всего расчетного количества реагента в осадок: влажный и обезвоженный без применения флокулянта, с определением рН осадка. Результаты эксперимента представлены на рис. 5.
рН
Время, мин.
влажный осадок (W=98%)
влажный осадок с флокулянтом (W=98%) осадок обезвоженный без флокулянта (W=80%) осадок обезвоженный с флокулянтом (W=80%)
Рис. 5. Зависимости изменения рН осадков от времени выдержки после добавления расчетной дозы реагента

16
Из полученных данных следует, что после смешения обезвоженного без флокулянта осадка с композицией АК-ЗЭ превращение ионов металлов в аминокислотные комплексы происходит в течение 9-11 минут, а в случае использования флокулянта - в течение 12-14 минут. Вероятно, молекулы полиакриламида, внедряясь в структуру коллоидных частиц осадка, замедляют проникновение анионов аминокислот.
В случае детоксицирования необезвоженного осадка (влажность ~98%) значение рН снижается до первоначального через 7-8 минут. Этого времени оказывается достаточно для поглощения солей аминокислот коллоидными частицами, где происходит образование аминокислотных комплексов металлов.
Таким образом, если влажный осадок, обработанный композицией АК-ЗЭ и флокулянтом, или обработанный их смесью направляется на механическое обезвоживание, то время между дозировкой и подачей на устройство для обезвоживания должно быть не менее 10 минут.
Важным этапом исследований являлось изучение влагоотдающей способности осадков, обработанных реагентами. Для определения влияния реагентов на изменение удельного сопротивления ОГСВ (влажность в пределах 97,5-:- 98,5%) использовались следующие дозы реагентов: флокулянт70 мл 0,1 %- го раствора на 1 л осадка; ММЭ-Т - 0,3 ммоль/л; АК-ЗЭ - 2,7 ммоль/л. Эксперименты показали, что внесение обеззараживающего реагента снижает удельное сопротивление осадков фильтрованию на 35-45% для активного ила, на 25-35% для сырого осадка, на 10-15% для осадка, сброженного в термофильных условиях. Таким образом, установлено, что бактерицидная композиция влияет на уплотненный осадок аналогично коагулянтам или флокулянтам, что позволяет сократить затраты на обезвоживание осадков. Влияние детоксицирующего реагента АК-ЗЭ на удельное сопротивление осадка не выявлено.
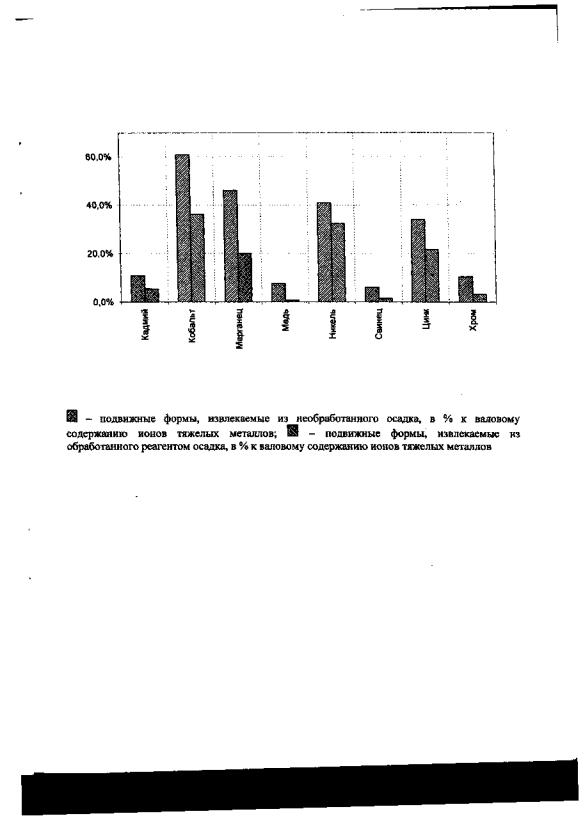
Для определения подвижности аминокислотных комплексов металлов осадок влажностью ~ 80% обрабатывали расчетной дозой реагента АК-ЗЭ. После выдержки определяли валовое содержание ТМ, и содержание подвижных форм ТМ (водная вытяжка и фосфатно-ацетатный буфер). Результаты, представленные на рис. 6, подтверждают снижение подвижности в фосфатно-ацетатном буфере аминокислотных комплексов по сравнению с подвижностью ионов металлов в необработанном осадке.
17
Наиболее подвижны комплексы никеля, кобальта и цинка. Доля подвижных комплексов кадмия не превышает 6 % (ион металла до 11 %), комплексов хрома - 2-3 % (ион металла до 11 %), комплексов свинца - 1-1,5 % (ион металла до 8 %).
Рис. 6. Диаграмма снижения подвижных форм соединений тяжелых металлов, %, извлекаемых фосфатно-ацетатным буфером, при обработке осадка
аминокислотным реагентом (АК-ЗЭ):
Эффективность детоксикации ионов тяжелых металлов подтверждена методами биотестирования, которые позволяют получить оценку токсичности вещества и косвенную оценку его влияния на элементы естественных экосистем. Для определения эффекта детоксикации тяжелых металлов рассматриваемым реагентом (АК-ЗЭ) были проведены эксперименты в модельных растворах солей тяжелых металлов.
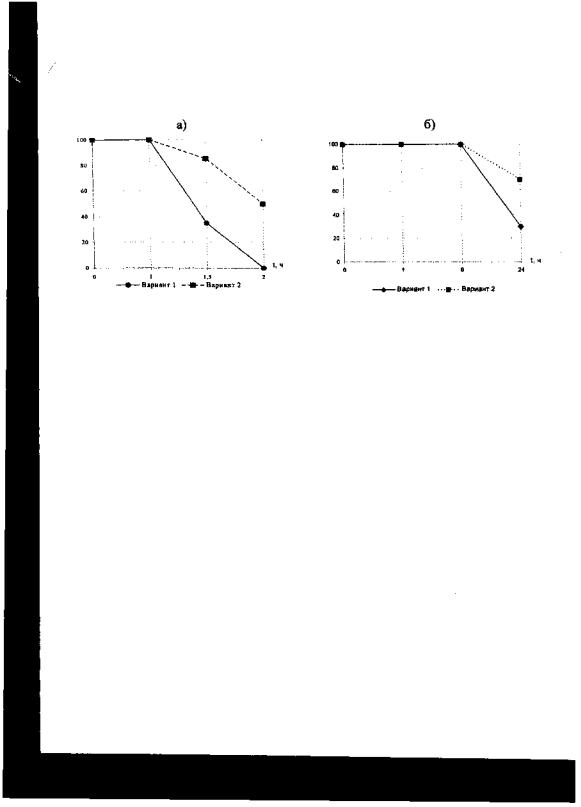
Сравнение результатов биотестирования на Daphnia magna исходных растворов солей тяжелых металлов и обработанных реагентом АК-ЗЭ (рис.7) доказывает эффективность детоксикации тяжелых металлов этим реагентом.
Результаты биологического тестирования проб исходного и обработанного расчетной дозой реагента АК-ЗЭ осадков по стандартной методике
18
биологического тестирования ΦΡ. 1.39.2001.00283 показывают снижение
показателя токсичности (Бкр10) на50-:-60% для осадка, обработанного реагентом АК-ЗЭ.
Количество |
Количество |
дафний, % |
дафний, % |
Рис.7. Результаты биотестирования при оценке токсичности растворов солей тяжелых металлов:
а) - изменение численности дафний при оценке острой токсичности растворов соли меди CuSO4 .5H2O (концентрация 0,2 г/дм3); б) - изменение численности дафний при оценке острой токсичности водной вытяжки из осадка; вариант 1 - «чистый» раствор соли металла (или вытяжка из осадка); вариант 2 - обработанный реагентом АК-ЗЭ растворсолиметалла(иливытяжкаизосадка).
Для установления воздействия детоксицированного осадка на почвенные
беспозвоночные использовались красные черви (Оболенский гибрид Eisenia
fetida). Оценка токсичности заключалась в определении процента смертности и
воздействия на рост и размножение взрослых земляных червей после опыта в
течение 28 дней. В результате эксперимента выявлено, что черви в
тестировавшихся субстратах не гибнут, что свидетельствует о приемлемых
условиях для жизнедеятельности червей в субстратах с использованием
обработанных ОГСВ.
Оценка генотоксичности исходного и детоксицированного осадка на
теплокровных проводилась исследованием действия суспензии осадков на клетки
костного мозга мышей при его введении per.os животным in vivo. Результаты
эксперимента показали отсутствие генотоксического действия обработанного
