
книги / Химические реакторы.-1
.pdf
ρC |
T |
wρC |
T |
F K T r H |
|
, |
(7.4) |
|
P τ |
|
P l |
|
R |
|
|
где τ – условное время пребывания компонентов в реакторе (см. уравнение (5.17)).
Полученное уравнение (7.4) является математическим описани-
ем потоков тепла, или уравнением теплового баланса РИВ-Н.
Для РИС-П с учётом гидродинамической обстановки в реакторе уравнение (7.1) можно записать так:
ρC |
|
dT |
F K T r H |
|
. |
(7.5) |
P |
|
R |
||||
|
dt |
|
|
|||
|
|
|
|
|
||
Для РИС-Н характерно отсутствие градиента параметров как во времени, так и по объёму реактора. Поэтому уравнение теплового баланса можно составить в целом для реактора, заменяя градиенты параметров их конечными значениями на входе и выходе из реактора и умножая на объём реактора VR :
V ρC |
|
dT |
VρC |
|
T T |
KF T T |
r H V , |
(7.6) |
P dτ |
|
|||||||
R |
|
P |
0 |
хл |
R R |
|
||
где F – общая поверхность теплообмена; T – температура в реакторе (или на выходе); Т0 – температура на входе в реактор; Тхл – температура теплоносителя (хладоагента); VR – объём реактора; V – объёмная скорость потока.
Уравнение (7.6) можно записать таким образом:
Qнак Qк |
Qт |
QR , |
(7.7) |
|||
где Qнак – накопление тепла в реакторе, |
|
|
||||
Q |
V ρC |
|
dT |
; |
(7.8) |
|
|
|
|||||
нак |
R |
|
P |
dτ |
|
|
Qк – конвективный поток тепла, т.е. разность между теплом, уно-
симым из реактора с реакционной массой, и теплом, вносимым в реактор с поступающими компонентами,
101
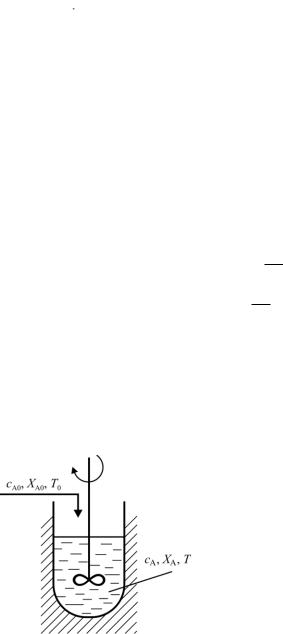
Qк VρCP T T0 ; |
(7.9) |
Qт – поток тепла, отводимый из реактора в результате теплообмена,
Qт KF T Tхл ; |
(7.10) |
QR – тепло, образующееся при химической реакции (экзотермической),
QR r HRVR , |
(7.11) |
где HR – тепловой эффект реакции, отнесённый к 1 моль исходно-
го компонента при температуре в реакторе.
Все уравнения теплового баланса (7.1), (7.4)–(7.6) являются математическими описаниями потоков тепла при нестационарном режиме, когда имеет место накопление тепла.
Для непрерывных реакторов в стационарном состоянии dTdτ 0.
Впериодических реакторах имеет место накопление тепла и dTdt 0.
7.3.Адиабатические реакторы
7.3.1. Адиабатический реактор идеального смешения периодического действия (А-РИС-П)
А-РИС-П – реактор с мешалкой, стенки которого изолированы
(рис. 23).
Рис. 23. Схема А-РИС-П
102
В соответствии с уравнением (7.5) запишем для РИС-П уравнение теплового баланса:
ρC |
|
dT |
F K T r H |
|
|
P |
dt |
R |
|||
|
|
||||
|
|
|
|
||
или |
|
|
|
|
|
|
|
Qнак Qт QR . |
(7.12) |
||
Поскольку при адиабатическом режиме отвод тепла отсутствует, то
Qт F K T 0. |
(7.13) |
Тогда уравнение теплового баланса примет вид |
|
Qнак QR , |
(7.14) |
т.е. тепло, образующееся при химической реакции, идёт на нагревание реакционной массы.
Для простой необратимой экзотермической реакции
А B HR |
(7.15) |
температура реакционной массы повышается с уменьшением концентрации реагента А, поэтому
QR rА HR . |
(а) |
||
Для РИС-П при проведении в нём реакции (7.15) характеристи- |
|||
ческое уравнение (5.8) запишем в виде |
|
||
r |
cА0 dX А |
. |
(б) |
|
|||
А |
dt |
|
|
|
|
||
Подставим (а) с учётом (б) в уравнение (7.14):
|
|
|
|
ρC |
|
dT |
|
cА0 dX А |
H |
|
, |
|
|
(7.16) |
||||
|
|
P |
|
|
|
R |
|
|
||||||||||
|
|
|
|
|
|
dt |
|
|
dt |
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
откуда находим: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
dT |
cА0 |
HR |
dX |
|
HR dX |
|
, |
(7.17) |
|||||||
|
|
|
|
А |
А |
|||||||||||||
|
|
|
|
|
|
ρCP |
|
|
|
|
C'P |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
где C |
– теплоёмкость реакционной массы, отнесённая к 1 моль |
|||||||||||||||||
P |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
реагента А, C |
|
ρCP |
. |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
P |
|
сА0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
103

Примем: HR const.
C
P
Проинтегрировав уравнение (7.17) от Т0 до Т и от 0 до ХА, получим:
T T T |
HR X , |
(7.18) |
|
0 |
C |
А |
|
|
|
||
P
где Т0, Т – температура реакционной массы на входе в реактор и в реакторе.
Из |
уравнения (7.18) |
следует |
уравнение теплового |
баланса |
||
А-РИС-П: |
|
|
|
|
|
|
|
|
|
|
|
|
(7.19) |
|
HR XA CP T T0 . |
|||||
При проведении реакции до конца, т.е. при ХА = 1, из уравнения |
||||||
(7.19) получаем: |
|
|
|
|
|
|
|
T |
T * T HR ; |
(7.20) |
|||
|
ад |
|
0 |
C |
|
|
|
|
|
|
|
||
|
|
|
|
P |
|
|
|
T * T |
T |
HR |
T , |
(7.21) |
|
|
|
ад |
0 |
C |
0 |
|
|
|
|
|
|||
|
|
|
|
P |
|
|
где T |
– адиабатическое изменение температуры; T * |
– макси- |
||||
ад |
|
|
|
|
|
|
мально возможная температура в адиабатическом процессе (т.е.
при ХА = 1).
7.3.2. Адиабатический реактор идеального смешения непрерывный (А-РИС-Н)
В соответствии с уравнениями (7.6) и (7.7) запишем уравнения теплового баланса для РИС-Н:
V ρC |
|
dT |
VρC |
|
T T |
KF T T |
r H V ; |
P dτ |
|
||||||
R |
|
P |
0 |
хл |
A R R |
||
|
|
|
Qнак |
Qк |
Qт QR . |
|
|
104

При стационарных условиях температура постоянна во времени в любой точке реактора, поэтому в уравнениях (7.6) и (7.7):
Q V ρC |
|
dT |
0. |
(а) |
|
|
|||
нак R |
P dτ |
|
||
Теплообмен в адиабатическом реакторе отсутствует: |
|
|||
Qт KF T Tхл 0. |
(б) |
|||
Подставим значения (а) и (б) в уравнение (7.6): |
|
|||
rА HRVR VρCP T T0 , |
(7.22) |
|||
или |
|
|
|
|
QR Qк . |
(7.23) |
|||
Из уравнения (7.23) видно, что в рассматриваемом случае тепло, выделяющееся в процессе реакции, расходуется на нагревание реакционной массы и уносится ею из реактора.
С учётом уравнения (5.34) уравнение (7.22) принимает вид
|
cА0 |
X А |
V |
HR |
VR VρCP T |
T0 |
. |
(7.24) |
|
|
|
VR |
|
||||||
|
|
|
|
|
|
|
|
|
|
Произведя сокращения и |
перестановки |
в |
уравнении |
(7.24), |
|||||
а также учитывая, |
что |
ρCP |
C , получаем уравнение теплового |
||||||
|
|||||||||
|
|
|
cA0 |
P |
|
|
|
||
|
|
|
|
|
|
|
|||
баланса А-РИС-Н: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(7.25) |
|
|
HR XA CP T T0 . |
|
|
|||||
7.3.3. Адиабатический реактор идеального вытеснения непрерывный (А-РИВ-Н)
Запишем полученное ранее уравнение теплового баланса (7.4) для РИВ-Н:
ρC |
|
dT |
wρC |
|
dT |
KF T r H |
|
, |
P dτ |
P dl |
|
||||||
|
|
A |
R |
|
||||
105
или с учётом (7.7):
|
|
Qнак Qк Qт |
QR . |
|
|||||||||||||||||
При стационарных условиях работы РИВ-Н: |
|
||||||||||||||||||||
|
|
|
|
Qнак |
0; |
Qт 0. |
|
|
|
|
|
||||||||||
Тогда из уравнения (7.4) следует: |
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
r H |
|
wρC |
|
dT |
. |
|
|
(7.26) |
|||||||||||
|
|
|
|
|
|
||||||||||||||||
|
|
А |
|
|
R |
|
|
|
|
P |
dl |
|
|
|
|
|
|||||
С учётом характеристического уравнения (5.25) для РИВ-Н |
|||||||||||||||||||||
уравнение (7.26) примет вид |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
с |
|
dX А |
H |
|
wρC |
|
|
|
dT |
. |
(7.27) |
|||||||||
|
|
|
|
|
|
|
|
||||||||||||||
|
А0 |
|
|
dτ |
|
|
|
|
|
R |
|
|
|
|
P |
|
dl |
|
|||
Учитывая, что l wτ |
и |
dl wdτ, |
уравнение (7.27) представим |
||||||||||||||||||
в виде |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
с |
|
dX А |
H |
|
|
wρC |
|
|
|
dT |
. |
(7.28) |
||||||||
|
|
|
|
|
|
|
|
||||||||||||||
|
А0 |
|
|
dτ |
|
|
|
|
R |
|
|
|
P wdτ |
|
|||||||
После |
преобразования уравнения |
(7.28) с |
учётом того, что |
||||||||||||||||||
CP C , |
получим уравнение теплового баланса А-РИВ-Н: |
||||||||||||||||||||
P |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
сА0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
R |
dX |
A |
C dT. |
|
|
|
|
(7.29) |
||||||||
|
|
|
|
|
|
|
|
P |
|
|
|
|
|
|
|
|
|
||||
Интегрирование этого уравнения представляет значительную трудность, что связано со сложной функциональной зависимостью значений HR , ρ, СР от температуры и степени превра-
щения.
В отдельных случаях эти величины могут незначительно меняться в ходе реакции, и тогда уравнение (7.29) можно записать в таком виде:
HR X |
|
. |
(7.30) |
А CP T T0 |
106
Если при температуре Т0 степень превращения XA0 = 0, то нетрудно получить следующее:
HR X |
|
. |
(7.31) |
А CP T T0 |
Таким образом, для всех типов реакторов (РИС-П, РИС-Н, РИВ-Н) при адиабатическом режиме их работы тепловой баланс выражается в виде одинаковых уравнений (7.19), (7.25), (7.31). Это связано с тем, что в адиабатических условиях тепло химической реакции расходуется только на нагревание реакционной массы.
7.4. Изотермические реакторы
Изотермические реакции можно проводить только в непрерывных реакторах, так как для поддержания постоянной температуры в РИС-П отвод тепла должен изменяться во времени, что в промышленных условиях осуществить трудно.
В изотермических реакторах температура в течение всего процесса остается постоянной вследствие подвода или отвода тепла.
7.4.1. Изотермический реактор идеального смешения непрерывный (И-РИС-Н)
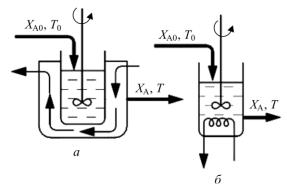
В этом реакторе теплоотвод осуществляется через стенку, которая охлаждается каким-либо хладоагентом (рис. 24, а), или же с помощью теплообменных элементов, расположенных внутри реактора (рис. 24, б).
Рис. 24. Схема И-РИС-Н
107

В стационарных условиях, а также в тех случаях, когда температура реакционной массы на входе в реактор равна температуре на выходе из него (т.е. Т = Т0), уравнения (7.8) и (7.9) теплового баланса РИС-Н примут вид:
Q V ρC |
|
dT |
0; |
(а) |
|
|
|||
нак R |
P dτ |
|
||
Qк VρCP T T0 0. |
(б) |
|||
Подставим значения (а) и (б) в уравнение (7.6), получим: |
|
|||
rА HRVR KF T Tхл , |
(7.32) |
|||
или |
|
|
|
|
QR Qт . |
(7.33) |
|||
Таким образом, тепло реакции в рассматриваемом случае отводится в результате теплообмена.
С учётом уравнения (5.34) уравнение (7.32) примет вид
|
сА0 X А |
V |
HR |
VR |
KF T Tхл . |
(7.34) |
|
VR |
|
||||
|
|
|
|
|
|
|
После преобразования уравнения (7.34) с учётом |
того, что |
|||||
сA0 nVA0 , получим уравнение теплового баланса И-РИС-Н:
H |
|
X |
|
|
KF T Tхл |
, |
(7.35) |
|
R |
A |
nA0 |
||||||
|
|
|
|
|
||||
|
|
|
|
|
|
|
здесь nA0 – мольный расход компонента А на входе в реактор.
7.4.2. Изотермический реактор идеального вытеснения непрерывный (И-РИВ-Н)
Для РИВ-Н, как и для РИС-Н, в изотермическом режиме:
Qнак 0; |
Qк 0; |
QR Qт . |
108

Тогда уравнение (7.4) теплового баланса РИВ-Н принимает вид:
|
|
(7.36) |
rА· HR F K T F K T Tхл . |
||
Учитывая, что в соответствии с уравнением (5.25)
rсА0·dX А ,
Аdτ
можно записать:
|
сА0·dX А |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
· HR |
F K T |
Tхл , |
(7.37) |
|||||||||||||||
|
dτ |
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
отсюда |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
H |
|
dX |
|
|
F K T Tхл |
dτ. |
|
(7.38) |
|||||||||||||
|
R |
А |
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
сА0 |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
Далее учтём следующее: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
F |
F |
; |
|
|
|
|
|
(а) |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
VR |
|
|
|
|
|
|
||||||
|
|
|
|
|
с |
|
|
|
|
|
nА0 |
; |
|
|
|
|
|
(б) |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
А0 |
|
|
|
V |
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
dτ |
dl |
. |
|
|
|
|
|
(в) |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
w |
|
|
|
|
|
|
|||
После подстановки (а), (б) и (в) в уравнение (7.38) оно примет вид: |
||||||||||||||||||||||
HR dX А |
|
|
KF T Tхл |
dl·V |
|
. |
(7.39) |
|||||||||||||||
|
|
|
|
|
|
|
VR ·nА0·w |
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
С учётом преобразований уравнения (7.39) находим: |
|
|||||||||||||||||||||
|
HR dX A |
|
KF T Tхл dl |
, |
|
(7.40) |
||||||||||||||||
|
|
|
|
|
|
|
|
nA0 |
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
где F" Fl .
Уравнение (7.40) – уравнение теплового баланса И-РИВ-Н.
109

7.5.Политропические реакторы
Вполитропическом реакторе имеет место теплообмен, и температура реакционной массы меняется. Изменение температуры может происходить по любому закону независимо от величины теплового эффекта протекающих в нём реакций и степени превращения.
Расчёт политропического реактора заключается в определении оптимального профиля (во времени или в пространстве) температу-
ры, при которой скорость процесса в любой момент времени в РИС-П или в любом сечении РИВ-Н была бы максимальной.
7.5.1. Политропический реактор идеального смешения непрерывный (П-РИС-Н)
Для стационарных условий с учётом особенностей политропического режима из уравнений (7.6) и (7.7) теплового баланса РИС-Н следует:
rА· HR·VR VρCP T T0 FK T Tхл ; |
(7.41) |
|||||||||
|
|
|
|
QR Qк |
Qт . |
|
|
(7.42) |
||
Учитывая характеристическое |
уравнение |
(5.34) для |
РИС-Н, |
|||||||
а также то, что |
VR |
, |
C |
CP и с |
|
·V n |
, преобразуем урав- |
|||
|
|
|||||||||
|
V |
P |
сА0 |
А0 |
А0 |
|
|
|
||
|
|
|
|
|
|
|
|
|||
нение (7.41): |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
FK T Tхл |
. |
(7.43) |
||
|
|
|
|
|
|
|
||||
HR X A CP T T0 |
|
nA0 |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
Мы получили уравнение теплового баланса П-РИС-Н.
Из приведённых уравнений видно, что в политропическом реакторе тепло химической реакции частично расходуется на нагревание реакционной массы, а частично отводится путём теплообмена. Меняя соотношение между Qк и Qт, в политропическом реакторе можно создавать любой температурный режим.
110
