
Лекции / Лекция №21. Биохимия свертывающей системы, фибринолитической и антикоагулянтной систем
.pdf
Военно-медицинская академия имени С.М. Кирова
Кафедра клинической биохимии и лабораторной диагностики
Экз.№__
УТВЕРЖДАЮ Заведующий кафедрой клинической биохимии и лабораторной диагностики член-корреспондент РАН
А. Иванов
" ___ " _____________ 201 г.
Профессор доктор медицинских наук доцент Р. Грашин
____________________________________________________________________________
(должность, ученая степень, ученое звание, воинское звание, фамилия автора, инициалы)
ЛЕКЦИЯ № 21
_________________________________
(номер по тематическому плану изучения дисциплины)
по биохимии
__________________________________
(наименование дисциплины)
на тему: Биохимия свертывающей системы, фибринолитической и антикоагулянтной систем
__________________________________________________________________
(наименование темы занятий по тематическому плану изучения дисциплины)
для обучающихся 2 курса ФП(Г)В по специальности «Лечебное дело»
(факультета, курса, цикла)
Обсуждена и одобрена на заседании кафедры Протокол №__ «_____»_____________ 20__ г. Уточнено (дополнено): «_____»_____________ 20__ г.
(воинское звание, подпись, инициал имени, фамилия.)
2
СОДЕРЖАНИЕ ПЛАНА ЛЕКЦИИ
№ |
Учебные вопросы |
Время |
п/п |
(согласно тематическому плану изучения дисциплины) |
(мин.) |
1 |
Введение |
5 |
|
|
|
2 |
Сосудисто-тромбоцитарный (первичный) гемостаз. |
30 |
3 |
Плазменно-коагуляционный (вторичный) гемостаз. |
20 |
4 |
Противосвёртывающая (антитромботическая) система крови. |
15 |
5 |
Общие представления о нарушениях системы гемостаза. |
15 |
Объем первичных лабораторных тестов для диагностики. |
||
6 |
Выводы и заключение |
5 |
ЛИТЕРАТУРА
1.Березов Т.Т., Коровкин Б.Ф. Биологическая химия: Учебник.-3-е изд., стереотипное.-М.: ОАО «Издательство «Медицина», 2012.-704с.
2.Биохимия: Учебник / Под ред. Е. С. Северина. - 3 изд - е., испр. - М: ГЭОТАР-МЕД, 2009. - 768с.: ил.
НАГЛЯДНЫЕ ПОСОБИЯ
Презентация к лекции №21
ТЕХНИЧЕСКИЕ СРЕДСТВА ОБУЧЕНИЯ
1)Мультимедийный проектор
2)Интерактивная доска
3)Ноутбук
4)Программное и мультимедийное обеспечение
3
ТЕКСТ ЛЕКЦИИ
Введение.
Система гемостаза представляет собой совокупность морфофункциональных и биохимических механизмов, обеспечивающих остановку кровотечения и, вместе с тем, поддерживающих кровь в жидком состоянии внутри сосудов. Видимо можно сказать, что это система поддержания крови в физиологическом агрегатном состоянии.
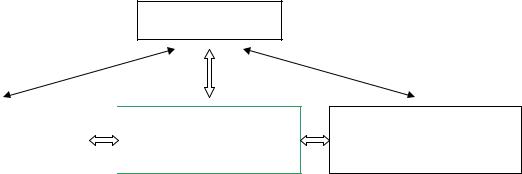
Основными компонентами системы гемостаза являются сосудистая стенка (особенно её эндотелиальная выстилка и субэндотелий), клетки крови, а также плазменные и клеточные ферментные системы: свёртывающая, фибринолитическая, антикоагулянтная, калликреин-кининовая, комплемента. Схематически эти чрезвычайно тесно связанные и взаимозависимые по своим функциональным и регуляторным позициям компоненты можно представить в виде трёх составных частей (рис.1).
ЦНС
Свёртывающая |
|
Антикоагулянтная |
система |
|
система |
|
|
|
Фибринолитическая
система
Рис. 1. Общая схема системы гемостаза.
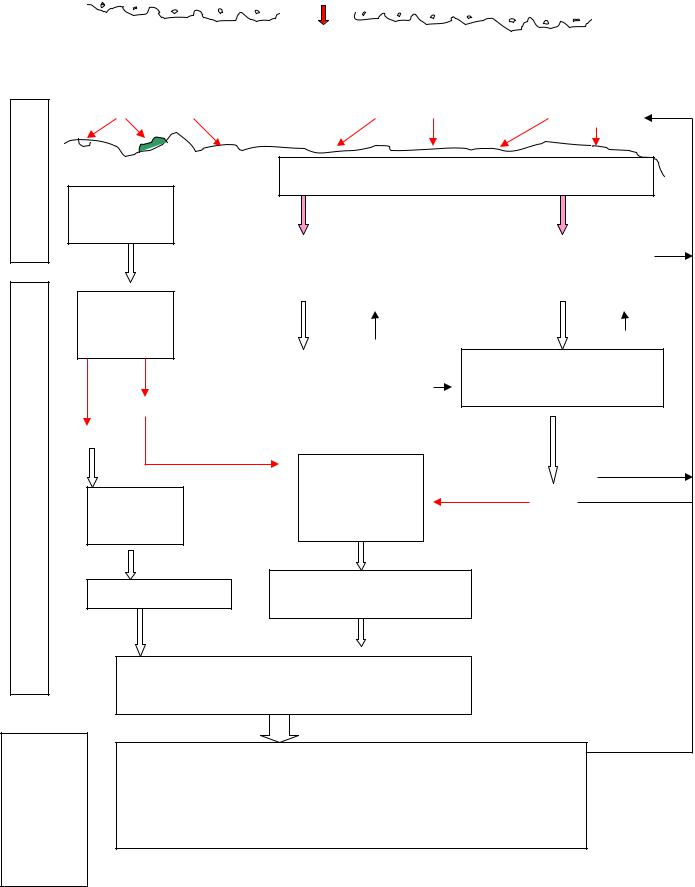
Формирование тромба – многокомпонентный процесс, состоящий из двух этапов: первичного - микроциркуляторного или сосудисто-тромбоцитарного (рис.2) и вторичного - макроциркуляторного или плазменно – коагуляционного (рис.3). Инициация этих двух этапов начинается одновременно и идёт параллельно, но первичный гемостаз завершается быстрее, создавая основу для последующих реакций плазменно-коагуляционного звена.
|
|
4 |
|
|
|
СОСУДИСТО-ТРОМБОЦИТАРНЫЙ (ПЕРВИЧНЫЙ) ГЕМОСТАЗ |
|||
|
Повреждение стенки сосуда |
|
||
|
Активирующие воздействия на рецепторы |
мембраны |
||
__________________________________________________________________ |
||||
|
сильные агонисты |
слабые агонисты |
||
А |
связываются со своими рецепторпми на тромбоцитарной мембране |
|||
(коллаген, тромбин) |
(ТхА2, тромбин (малые дозы), АДФ, серотонин) |
|||
Д |
|
|
|
|
Г |
|
|
|
|
Е |
|
Высвобождение Са+2 из системы плотных гранул |
||
З |
|
|||
И |
Активация |
|
|
|
Я |
|
|
||
|
ФлС |
|
|
|
|
|
Доступность рецептора |
Мобилизация мембранных |
|
|
|
тромбоцитов IIb-IIIa |
фосфолипидов тромбоцита |
|
О |
ФИ-4-Фт |
для фибриногена |
ФС,ФХ,ФЭ |
|
|
|
|||
Б |
Са+2 |
Са+2 |
||
Р |
ФИ-4,5-Фт |
|||
А |
ФИ |
|
|
|
Т |
Взаимодействие тромбоцитов |
Активация ФлА2 и моби- |
||
И |
||||
М |
между собой, их связывание |
лизация мембранных ФЛ |
||
А |
ИЛ-3ф-т |
фибриногеновыми мостами |
|
|
Я |
ДГ |
|
Циклооксигеназа |
|
А |
|
Тромбоксансинтаза |
||
Г |
|
Увеличение |
ПГG2; ПГН2 |
|
Р |
|
концентрации |
||
Е |
Активация |
ТхА2 |
||
Са+2 |
||||
Г |
||||
А |
ПкС |
+кальмодулин |
|
|
Ц |
|
|
|
|
И |
|
|
|
|
Я |
|
Активация киназы лёгкой |
||
|
Р47 (Плекстрин) |
|||
|
цепи миозина |
|
||
|
|
|
||
|
Фосфорилирование белков сократительной |
|
||
|
системы тромбоцита и сокращение актомиозина |
|||
Секре-ция |
Выделение из δ-гранул АДФ, серотонина, эпинефрина, Са +2; |
|||
и необ- |
||||
рати- |
из γ-гранул – лизосомальных ферментов, для последующей река- |
|||
мая агре- |
нализации сосуда; |
|
||
гация |
из α-гранул – фибриногена, ф.Вилебранда, тромбоспондина, вит- |
|||
|
ронектина и др. белков |
|
||
Ретракция тромбоцитарного тромба, армирование фибрином.
5
Рис. 2. Тромбоцитарное звено гемостаза.
Первичный гемостаз обеспечивает остановку кровотечения из мелких сосудов за счёт обеспечения спазма мелких сосудов адгезии, агрегации, секреции из тромбоцитов биологически активных веществ, с образованием белого тромбоцитарного тромба, его сокращения (ретракции) и уплотненения.
Сосудисто-тромбоцитарный гемостаз осуществляется на основе взаимодействия тромбоцитов с сосудистой стенкой в местах её повреждения. Благодаря своим уникальным свойствам неповреждённый эндотелий интактен. Он несмачивается, в нём синтезируются биологически активные вещества, определяющие его общий антитромботический потенциал: дезагрегирующая эндоперекись - простациклин (PgI2), оксид азота (NO), антитромбин III - основной эндогенный антикоагулянт, активатор плазминогена тканевого типа (ТАП), ингибитор тканевого пути свёртывания (TFPI – Tissue Factor Pathway Inhibitor) , тромбомодулин и, наконец, на рецепторах эндотелиоцитов фиксируются комплексы гепарин-антитромбин III.
Так как ламинарная сторона эндотелиоцитов и тромбоциты заряжены отрицательно, то адгезии (прилипания) последних к стенке сосудов не происходит. Отрицательный заряд мембран сформирован так называемым Z- потенциалом. При изменении отрицательного заряда на эндотелии как в след-
ствие |
деполяризации мембран эндотелиоцитов, так и при их повреждении, |
|
создаются условия для усиления |
адгезии тромбоцитов. Несмотря на отрица- |
|
тельно заряженную поверхность |
эндотелий активно поглощает тромбоциты |
|
- до |
35000/мкл в сутки. Это, так называемая, ангиотрофическая функция |
|
тромбоцитов. Считается, что при тромбоцитопениях одной из причин возникновения дистрофии эндотелия, ломкости сосудов, кровотечений, является частичная утрата данной функции.
Процесс свёртывания крови в целом, как и первичный гемостаз в частности, инициируются вследствие повреждения сосудистой стенки. При повреждении эндотелия создаётся чужеродная «тромбогенная» контактная поверхность, которая активирует тромбоциты и тем самым инициирует процесс их взаимодействия со стенкой сосудов.
В первые секунды после повреждения сосуда происходит активация и адгезия тромбоцитов к его краям, микрофибриллам, эластиновым и коллагеновым волокнам. Процесс адгезии сходен с распластыванием клеток на чужеродной поверхности (стекле и др.). Активация томбоцита происходит под действием разнообразных физических и химических веществ. В процессе активации тромбоцит резко увеличивается в размерах, при этом делая доступными для воздействия свои многочисленные гликопротеиновые мембранные рецепторы, которые можно разделить на первичные и вторичные. Первичные рецепторы реагируют непосредственно на действие активирующего фактора, вторичные открываются только после активации тромбоцита. Так при помощи рецепторов ГП Ia/IIa тромбоцит непосредственно связывается с коллагеном сосудистой стенки. Причём эта связь возможна только в местах с малой
6
скоростью тока крови (т.н. низкое напряжение сдвига). При высокой скорости кровотока (т.н. высокое напряжение сдвига) взаимосвязь тромбоцита с коллагеном осуществляется при помощи рецептора ГП Ib и высокомолекулярного кофактора адгезии - фактора Виллебранда (vWF). Последний в зону повреждения поступает из плазмы, секретируется эндотелием и самими тромбоцитами.
В кровотоке здорового взрослого человека количество тромбоцитов от 150 до 450
. 109/л, из них изначально активированных от 20 до 40 %. Это, как бы, "дежурные" клетки, которые в любой момент готовы мгновенно инициировать процесс свёртывания крови. В гранулах и в тубулярной системе тромбоцита содержится более 30 активных веществ, которые моментально могут быть выделены в кровоток (реакция высвобождения). Помимо этого на мембране тромбоцита адсорбированы почти все плазменные факторы свёртывания крови, включая фибриноген.
Параллельно с адгезией идёт агрегация тромбоцитов - наслаивание друг на друга и сцепление их между собой. Процесс агрегации усиливается под действием АДФ, выделяющегося из повреждённых эритроцитов и сосудистой стенки. Агрегация и адгезия тромбоцитов в значительной степени определяются соотношением тромбоксана ТхА2 и простациклина PgI2. Первое вещество выделяется в основном из тромбоцитов, а второе синтезируется преимущественно эндотелием. Синтез простациклина и тромбоксана осуществляется под действием циклооксигеназы из арахидоновой кислоты, которая в свою очередь входит в состав фосфолипидов клеточных мембран. Действие этих метаболитов носит противоположный характер. PgI2 расширяет кровеносные сосуды, активизирует тромбоцитарную аденилатциклазу, увеличивая концентрацию цАМФ, снижает уровень цитоплазматического кальция и таким образом способствует дезагрегации тромбоцитов. ТхА2 наоборот, сужает кровеносные сосуды, ингибирует тромбоцитарную аденилатциклазу, активирует фосфодиэстеразу. Всё это приводит к уменьшению содержания цАМФ, способствуя увеличению уровня Са+2 в цитоплазме тромбоцита и доступности его рецепторов для фибриногена, что в свою очередь активирует процесс агрегации тромбоцитов. Соотношение количества простациклина в эндотелиальных клетках и тромбоксана в тромбоцитах при локальном тромбообразовании имеет большой физиологический смысл: тромбоци-
тарный тромб, формируясь в месте повреждения сосуда, не должен распространяться по неповреждённой сосудистой стенке, а местная активация тромбоцитов не должна становиться системно диссеми-
нированной. Стимулированные эндотелиоциты у края повреждения, синтезируя и секретируя простациклин, вынуждают тромбоциты вернуться к своей первоначальной, неактивной форме.
Одновременно с агрегацией осуществляются реакции высвобождения содержимого гранул тромбоцитов, что значительно усиливает агрегацию и делает её необратимой. Исследование агрегации тромбоцитов в клинике имеет важное практическое значение, так как позволяет диагностировать и оценивать эффективность лечения многих форм кровоточивости, проводить контролируемое лечение дезагрегантами. Агрегация бывает первичной (обрати-
7
мой) и вторичной (необратимой). Обратимая агрегация развивается под действием слабых стимуляторов (агонистов), таких как АДФ, ТхА2. Для ос у- ществления вторичной агрегации необходимо дополнительное действие ТхА2, повышение концентрации ионизированного внутриклеточного Са+2 или влияние крайне сильных индукторов-стимуляторов типа коллагена и тромбина. Тонкий механизм агрегации заключается в том, что в процессе действия стимуляторов на тромбоцит осуществляется представление фибриногеновых гликопротеиновых рецепторов (ГП IIb-IIIa) тромбоцитов друг другу. Благодаря этому феномену кровяные пластинки соединяются (агрегируют). Чем больше рецепторов - тем больше контактов, тем мощнее агрегация. Мостиком между рецепторами тромбоцитов является фибриноген. Именно в процессе вторичной необратимой агрегации образуется своеобразная гемостатическая пробка, которая, вначале отличается малой плотностью и легко проходима для плазмы и форменных элементов крови. Для того, чтобы этого не происходило существует ретракция - процесс стягивания тромбоцитарного агрегата в абсолютно непроницаемый конгломерат. По своим функциональным характеристикам такая гемостатическая пробка ничем не отличается от нормальной сосудистой стенки.
Ретракция, как и реакции высвобождения, обеспечивается сократительными элементами тромбоцитов при участии Са+2. Именно последовательное, поэтапное повышение концентрации внутриклеточного ионизированного кальция приводит к развитию функциональной активности тромбоцитов.
Биохимический механизм развития агрегационно-ретракционного процесса на сегодняшний день предствляется следующим образом.
Взаимосвязь тромбоцитов друг с другом в процессе первичной агрегации, равно как и воздействия различных индукторов в крови типа адреналина, серотонина, тромбоксана на соответстсвующие рецепторы тромбоцитарной мембраны, ведут к передаче возникающего сигнала внутрь клетки. В клетке происходит первоначальное повышение концентрации внутриклеточного Са+2, что в свою очередь ведёт к активации мембранной фосфолипазы А2 (ФлА2). Этот фермент запускает каскад реакций простагландинтромбоксановой системы, начиная с высвобождения арахидоновой кислоты из мембранных фосфолипидов и заканчивая образованием простагландинов (PGG2, PGH2) и тромбоксана А2. Данные биологически активные вещества, выделяясь из тромбоцитов, воздействуют на другие тромбоциты, привлекая их в очаг повреждения, и одновременно усиливают сигнал активации, передаваемый внутрь эффекторным структурам клетки. При этом ТхА2 способен активировать фосфолипазу С (ФлС), включая таким образом полифосфоинозитольный путь активации ферментных систем тромбоцитов. Являясь сильнейшим ионофором, ТхА2 способствует выделению Са+2 из плотной тубулярной системы (δ-гранулы) тромбоцитов и попаданию их в кровь. Повсеместное повышение уровня Са+2 создаёт условия для финальных ферментативных реакций тромбоцитарного гемостаза. Прежде всего это стимуляция тромбоцитарной актомиозиновой системы - тромбостенина, которая осуществляется через
8
активацию фосфолипазы С. Действие этого фермента ведёт к появлению продуктов расщепления фосфолипидов – инозитолтрифосфата (ИФ3) и диацилглицерола (ДГ). (ИФ3) способен извлечь Са+2 из саркоплазматического ретикулума и таким образом активировать актомиозиновый ком плекс и одновременно фосфорилировать его белки образовавшимся мультимолекулярным комплексом Са+2 + кальмодулин + протеинкиназа С (ПкС). Диацилглицерол приводит к непосредственной активации протеинкиназы С и фосфорилированию тех же белков. В результате комплекса биохимических реакций в тромбоцитах резко возрастает содержание актина, актинсвязывающего белка, тяжёлого миозина и фибрина. Находящиеся в цитоплазме ионы Са2+ быстро вступают во взаимодействие с кальмодулином (кальцийсвязывающим белком), который активирует лёгкую цепь киназы миозина, обеспечивая её связь с актином. Благодаря этому происходит секреция (реакции высвобождения) и развивается процесс ретракции образовавшейся тромбоцитарной пробки.
В ходе секреции из δ гранул высвобождаются биологически активные вещества, необходимые для усиления активации и агрегации тромбоцитов в зоне сосудистого повреждения. Адреналин, серотонин, гистамин, АДФ по механизмам положительной обратной связи усиливают агрегацию и делают её необратимой даже при воздействии слабых агонистов.
Из α гранул секретируется более 30 протеинов, играющих важную роль как в гемостатических реакциях, так и в других физиологических и патологических процессах организма. Такие белки, как фибриноген, факторы V, XIII, антигепариновый фактор принимают участие в процессах гемокоагуляции. Адгезивные протеины (фибриноген, vFW, тромбоспондин, фибронектин, витронектин) участвуют в дальнейшем развитии процесса адгезии и укреплении фибриногеновох связей агрегировавших тромбоцитов. Из γ гранул выделяются лизосомальные ферменты, принимающие участие в реканализации сосуда после завершения гемостаза.
Так как актомиозиновые филаменты пересекают всю цитопазму тромбоцита и связаны с внутренней стороны мембраны с гликопротеиновыми комплексами IIb-IIIa, а снаружи к этим комплексам прикреплены межтромбоцитарные фибриногеновые мостики, то сокращение актомиозинового комплекса приводит к сокращению и уплотнению всей тромбоцитарно-фибриновой пробки.
Как правило, патология, связанная с нарушением сосудистотромбоцитарного звена гемостаза, обусловлена нарушением синтеза того или иного рецептора на поверхности тромбоцитарной мембраны. В качестве примера приведём следующие два заболевания:
- наследственную геморрагическую дистрофию тромбоцитов - синдром Бернара-Сулье; при этом заболевании на мембране отсутствует рецептор ГП Ib, который в норме присоединяет плазменный фактор Виллебранда (vFW), а последний, в свою очередь, фиксируется к краям повреждённого эндотелия, осуществляя таким образом адгезию тромбоцитов;
9
- тромбастению Гланцмана-Негли; в этом случае на поверхности тромбоцита отсутствует белок-рецептор (вероятно ГП IIb) к фибриногену, что ведёт к невозможности установления контакта между клетками, даже несмотря на наличие у них псевдоподий; такие тромбоциты не агрегируют и не подвержены последующей ретракции (стягиванию).
ПЛАЗМЕННО-КОАГУЛЯЦИОННЫЙ (ВТОРИЧНЫЙ) ГЕМОСТАЗ Процесс свёртывания крови
|
Внутренняя система |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Внешняя система |
|||||||||||||||
|
(кровяная) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(тканевая) |
||||||||||||||
|
Активируется контактной |
|
|
|
|
|
|
|
|
|
|
|
Тканевый тромбопластин - ф.III |
|||||||||||||||||||
|
поверхностью, катехоламинами, коллагеном, |
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
фосфолипидами клеточных мембран (ФЛ) в т.ч. тромбоцитов |
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
XII |
|
|
|
|
|
Прекалликреин (ф. Флетчера) |
|
|
|
|
|
|
||||||||||||||||
А |
Г |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
Н |
Е |
|
|
|
|
|
XIIf |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
Т |
П |
|
|
XII a |
|
|
|
|
|
|
|
|
Калликреин |
|
|
|
|
|
|
VII VIIa+Ca+2 |
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
И |
А |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Т |
Р |
|
|
XI |
|
|
|
|
|
Кининоген (ВМК, ф.Фицжеральда) |
|
|
|
|||||||||||||||||||
Р |
И |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
О + Н |
|
|
XI a |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
Кинин |
|
|
|
|
|
|
|
|
|
|
|||||||||||
М |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
Б |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
IX |
|
IXa+ VIIIa +ФЛ+ Сa+2 |
|
|
|
|
|
VIIa + III + Ca+2 |
|
|
|||||||||||||||||||
И |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
Н |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
III |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Протеин С |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
X |
|
Xa |
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ПрСакт+S+ФЛ+Са+2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Протеин Сакт |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
Тромбомодулин |
|
|
|
|
|
Xa+ Va+ ФЛ+ Ca+2 |
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Эндотелий
Протромбин (ф.II)  Тромбин (ф.IIa)
Тромбин (ф.IIa) 
 Фибриноген (ф.1)
Фибриноген (ф.1)
 Фибрин – мономер XIII
Фибрин – мономер XIII 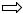 XIIIa
XIIIa
 Фибрин-полимер (растворимый)
Фибрин-полимер (растворимый)
 Фибрин-полимер (нерастворимый)
Фибрин-полимер (нерастворимый)
ПЛАЗМИНОГЕН  ПЛАЗМИН
ПЛАЗМИН
|
10 |
|
|
|
||
Тканевый активатор |
|
Плазменный активатор |
||||
плазминогена (ТАП) |
|
плазминогена |
|
|
||
|
|
|||||
|
|
|
|
|
|
|
Условные обозначения: |
|
|
|
|
|
|
- активация ; |
|
- активация; |
|
|
- ингибирование |
|
|
|
|
||||
Рис. 3. Плазменно-коагуляционный гемостаз По современным представлениям, свёртывание крови - цепная фермента-
тивная реакция, в которой происходит последовательная активация и взаимодействие ряда сериновых протеаз (факторов коагуляции) на фосфолипидных матрицах. Этот процесс ускоряется в тысячи раз неферментными факто-
рами VIII и V.
Процесс плазменно-коагуляционого гемостаза, именно так называется сам процесс свёртывания крови, протекает в три стадии (рис.3).
Первая - образование протромбиназы. Вторая - образование тромбина. Третья - образование фибрина.
Первая стадия наиболее сложная и продолжительная, представляет собой комплекс ферментативных реакций, приводящих к образованию протромбиназы. Протромбиназа может образовываться по внешнему и по внутреннему механизмам (путям). Во внутреннем пути все необходимые факторы присутствуют в движущейся крови, и реакция свёртывания начинается при контакте крови с чужеродной (изменённой) поверхностью (например, коллагеном субэндотелия), и этот путь связан с обязательным вовлечением в процесс свёртывания тромбоцитов. Внешний механизм осуществляется при обязательном участии фактора III - тканевого тромбопластина, который находится в межклеточной жидкости. Образование протромбиназы обычно осуществляется с вовлечением этих двух путей, так как они пересекаются и дополняют друг друга.
Начиная с образования активного фактора X, оба пути имеют одинаковое развитие.
Формирование протромбиназы по внешнему пути начинается с активизации фактора VII - проконвертина и превращения его в фактор VIIa.
Активация проконвертина наиболее активно осуществляется в присутствии фосфолипидов, которые в данном случае, как правило, представлены тканевым тромбопластином – ф.III. В настоящее время считается, что в крови фактор VII уже циркулирует в виде активного фермента, но его ферментативная активность значительно увеличивается в присутствии тканевого тромбопластина.
Далее под воздействием образовавшегося комплекса (ф.VIIa+ф.III+Са+2) происходит гидролиз тяжёлой цепи фактора X, в результате чего образуется активизированный фактор α-Xa, который посредством аутокатализа превращается в фактор β-Xa. Эти изоформы с одинаковой активностью во з- действуют на протромбин (ф.II).
