
Adsorbtsia_polimerov
.docx
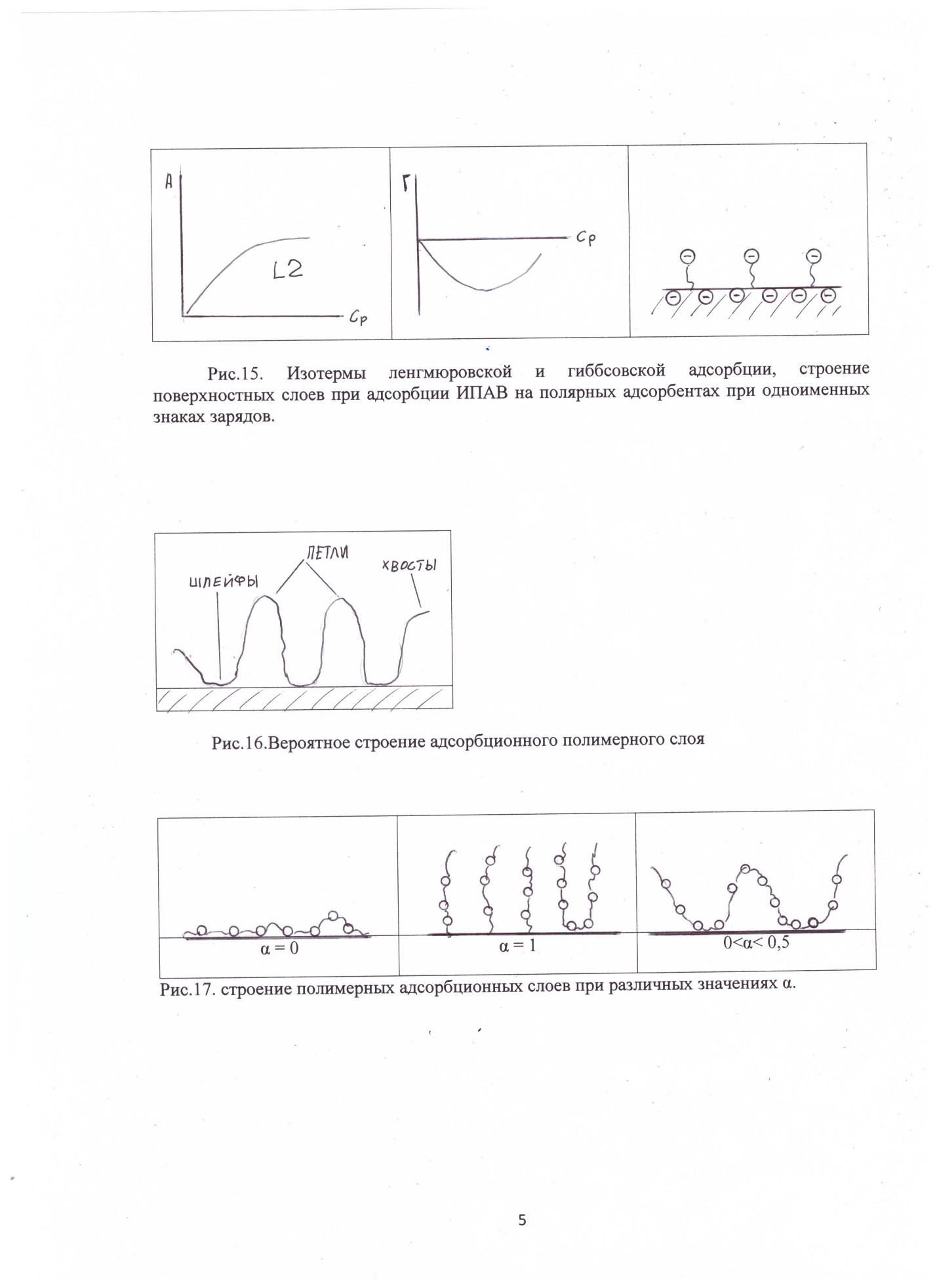
Адсорбция полимеров.
Спецификой строения макромолекул являются их большая молекулярная масса (до нескольких миллионов) и гибкость, т.е. способность к конформационным превращениям. В результате чего, при адсорбции с поверхностью адсорбента может взаимодействовать не вся макромолекула, а только ее отдельные части. Общий вид полимерного адсорбционного слоя представлен на рис. 16.
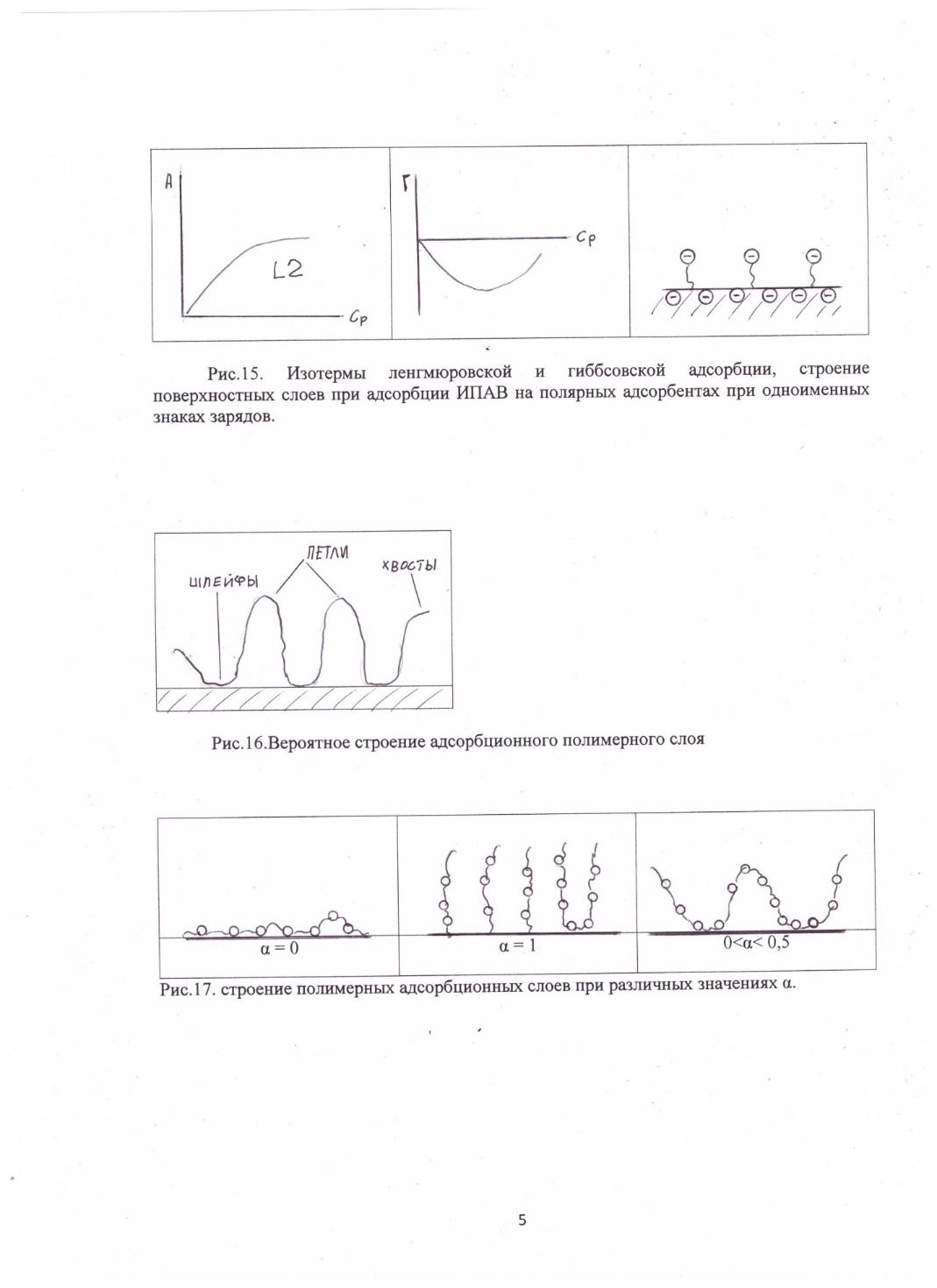
Те части макромолекулы, которые непосредственно взаимодействуют с поверхностью называются шлейфами. Части макромолекулы, находящиеся в дисперсионной среде, образуют петли и хвосты. Соотношение между шлейфами, петлями и хвостами зависит от природы полимера (гибкоцепной или жесткоцепной), термодинамического качества растворителя. Часто для создания адсорбционных слоев используют блок-сополимеры, в которых одни блоки имеют повышенное сродство к адсорбенту и образуют шлейфы (якорные группы), другие блоки имеют высокое сродство к растворителю и образуют петли. Оценить вероятное расположение макромолекул на поверхности адсорбента можно используя уравнение Перкеля-Алмана:
Амах = КМα, где Амах[кг/м2] – максимальная адсорбция, К-константа, М- молекулярная масса, α- константа, величина которой зависит от строения адсорбционного слоя.
В том случае, когда макромолекулы преимущественно связаны с поверхностью (т.е адсорбционный слой состоит из шлейфов) коэффициент α=0 (см. рис.17). Когда макромолекулы ориентированы по нормали к поверхности (хвосты) коэффициент α=1. В наиболее вероятном случае, когда в адсорбционном слое имеются шлейфы, петли и хвосты коэффициент 0<α<0,5
В логарифмическом виде уравнение представляет собой:
lgAmax=lgK +αlgM.
Для нескольких фракций полимера с узким молекулярно-массовым распределением определяется величина Амах и строится зависимость lgAmax от lgM, тангенс угла которой по отношению к оси абсцисс дает искомое значение α (см. рис.18).

Основные закономерности адсорбции полимеров.
1.Полимеры адсорбируются на поверхности самых различных адсорбентов вне зависимости от их природы (сродства).
2. Адсорбция полимеров как правило необратима.
3. Для адсорбции полимеров характерны изотермы класса Н2
4.На изотермах адсорбции вместо плато часто наблюдается восходящий участок, появление которого связано с полидисперсностью макромолекул.
5.Адсорбция из хороших растворителей (А2˃0) увеличивается с ростом молекулярной массы и слабо зависит от молекулярной массы при адсорбции из плохих растворителей.
6.Адорбционные равновесия устанавливаются очень медленно (сутки, недели).
Первые три пункта связаны с высокой молекулярной массой макромолекул и действием кооперативного эффекта, когда одна макромолекула может образовывать с поверхностью адсорбента огромное число пусть и очень слабых связей. Поэтому при малых концентрациях практически все макромолекулы переходят на межфазную поверхность и на изотерме возникает участок, совпадающий с осью ординат.
Рис.19. Изотерма адсорбции полимеров из растворов.
Поскольку синтетические полимеры, как правило, полидисперсны, первыми с поверхностью адсорбента взаимодействуют молекулы с наименьшей молекулярной массой (они имеют более высокий коэффициент диффузии). Затем подходят молекулы с более высокой молекулярной массой, которые могут образовать с поверхностью адсорбента большое число связей и постепенно вытесняют молекулы с меньшей молекулярной массой. В результате на изотерме появляется вместо плато восходящий участок.
Высокие молекулярные массы полимеров обусловливают медленное установление адсорбционных равновесий, что учитывается в технологии фармацевтических и косметических композиций. Например, зубные пасты содержащие водорастворимые полимеры для регулирования консистенции выдерживаются на складе в течение двух недель для установления физико-химических характеристик.
Адсорбции
полиэлектролитов подчиняется тем же
закономерностям, что и адсорбция ИПАВ.
В этом случае так же действует
электростатическая составляющая энергии
адсорбции (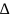 Gадс=
Gспециф.
+
Gэл.
стат.),
а сама адсорбция может быть, как физической
так и химической.
Gадс=
Gспециф.
+
Gэл.
стат.),
а сама адсорбция может быть, как физической
так и химической.
