
Лаб1_окисление_SO2
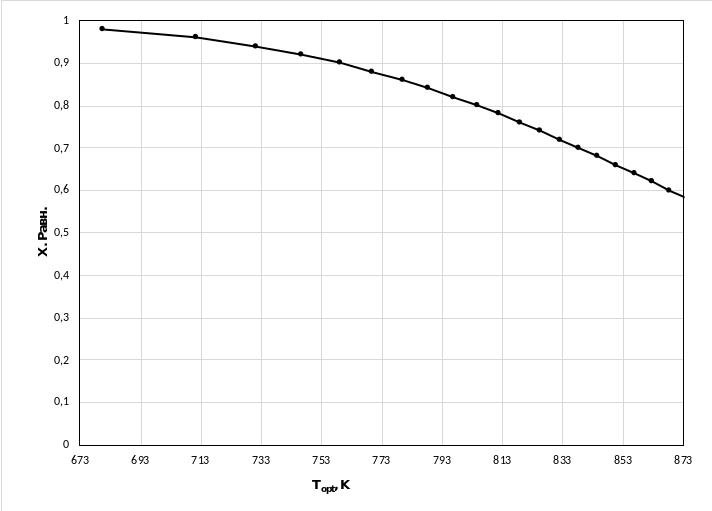
.docxОбъемный процент кислорода O2 в смеси при CSO2=9,5% об. при получении смеси в результате следующих процессов:
при сжигании S в воздухе
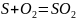
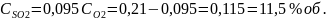
при обжиге FeS2

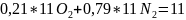
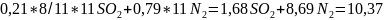
-
10,37 — 100%
x = 16,2% = CSO2
1,68 — x

при смешении SO2 c воздухом
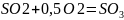
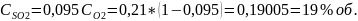
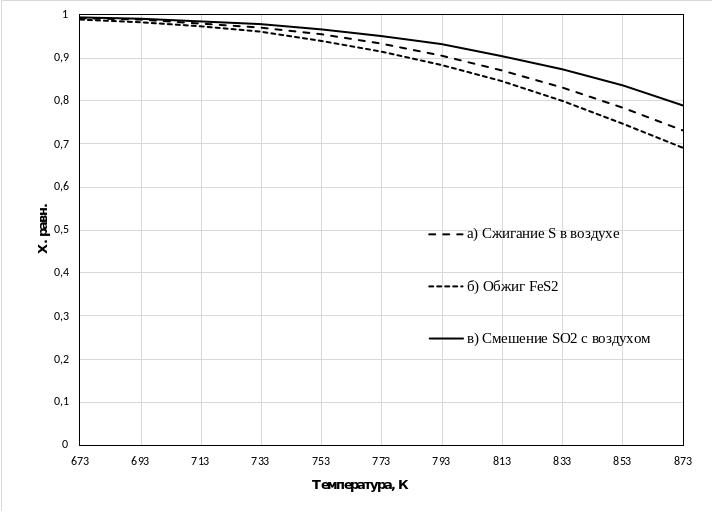
Зависимость равновесной степени превращения SO2 от температуры при постоянном давлении и заданной концентрации исходных реагентов:
СSO2 = 0,095 об., P = 1 атм., T = 673 – 873 К
-
T, К
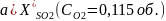
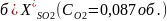
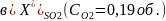
673
0,9915
0,989
0,9942
693
0,9864
0,9823
0,9906
713
0,9787
0,9725
0,9852
733
0,9677
0,9586
0,9773
753
0,9523
0,9395
0,9663
773
0,9317
0,9144
0,9512
793
0,9048
0,8825
0,9312
813
0,8712
0,8436
0,9054
833
0,8307
0,7979
0,8732
853
0,7835
0,7462
0,8343
873
0,7305
0,6897
0,7891
Зависимость равновесной степени превращения SO2 при сжигании S в воздухе от температуры при различных давлениях
СSO2 = 0,095 об., CO2 = 0,115 об., T = 673 – 873 К
-
T, К
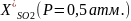
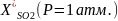

673
0,9881
0,9915
0,9982
693
0,9809
0,9864
0,997
713
0,9702
0,9787
0,9953
733
0,955
0,9677
0,9927
753
0,9342
0,9523
0,9891
773
0,9067
0,9317
0,984
793
0,8717
0,9048
0,977
813
0,8289
0,8712
0,9678
833
0,7788
0,8307
0,9556
853
0,7224
0,7835
0,9401
873
0,6613
0,7305
0,9208

Зависимость скорости окисления SO2 от температуры при постоянном давлении и различных равновесных степенях превращения
СSO2 = 0,095 об., CO2 = 0,115 об., P = 1 атм., T = 673 – 873 К, катализатор – Classik
-
Т, К
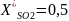
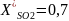
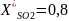

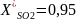
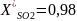
673
0,233
0,132
0,085
0,041
0,02
0,007
693
0,322
0,183
0,118
0,056
0,026
0,006
713
0,437
0,248
0,159
0,075
0,032
-0,002
733
0,583
0,33
0,211
0,095
0,031
753
0,766
0,431
0,271
0,109
0,006
773
0,99
0,551
0,336
0,101
-0,083
793
1,261
0,684
0,389
0,024
813
1,579
0,815
0,392
-0,228
833
1,94
0,902
0,256
853
2,322
0,851
-0,213
873
2,676
0,469
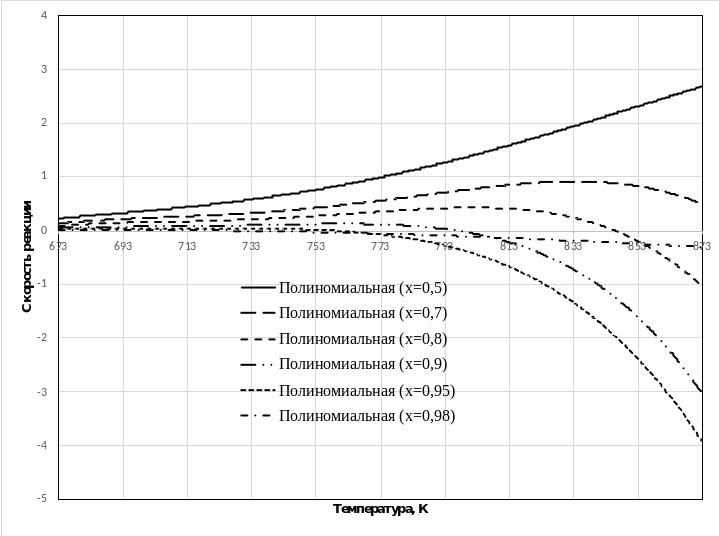
Линия оптимальных температур
СSO2 = 0,095 об., CO2 = 0,115 об., P = 1 атм., X. Равн = 0,5 – 0,98, катализатор – Classik
-
x
0,5
0,52
0,54
0,56
0,58
0,6
0,62
0,64
0,66
0,68
0,7
T, K
898,2
892,2
886,3
880,3
874,4
868,5
862,6
856,7
850,7
844,6
838,4
x
0,72
0,74
0,76
0,78
0,8
0,82
0,84
0,86
0,88
0,9
0,92
T, K
832,1
825,6
818,8
811,9
804,6
796,9
788,6
779,8
770
759,1
746,5
x
0,94
0,96
0,98
T, K
731,3
711,3
680,5
Задача:
Исходная смесь содержит 10 об. % SO2 и получена: а) при сжигании серы в воздухе; б) при обжиге колчедана в воздухе. Полагая, что на выходе из реактора температура прореагировавшей смеси 430°С и достигается равновесие, определите насколько изменится выброс диоксида серы (остаточное содержание SO2) при увеличении давления процесса с 1 атм до 10 атм. Рассчитайте для обоих случаев суточное количество серной кислоты, эквивалентное выбрасываемому в атмосферу SO2, при мощности производства 360 тыс. тонн в год. Объясните полученный результат.
Так как производительность в год составляет 360 тыс тонн, то производительность в сутки составляет: 360000/365=986,3 (тонн/сутки)
Для сжигания S при 1 атм:
Xp=0.9829
mso2=(1-0.9829)* 986,3=16.87 (тонн)
mH2SO4=16.87*98/64=25.83 (тонн)
Для 10 атм:
Xp=0.9945
mso2=(1-0.9945)*986,3=5.42 (тонн)
mH2SO4=5.42*98/64=8.31 (тонн)
Для обжига FeSO4 при 1 атм
Xp=0.9779
mso2=(1-0.9779)* 986,3=21.8 (тонн)
mH2SO4=21.8*98/64=33.38 (тонн)
При 10 атм:
Xp=0.9928
mso2=(1-0.9928)* 986,3=7.1 (тонн)
mH2SO4=7.1*98/64=10.87 (тонн)
Выводы
В ходе выполнения лабораторной работы был рассчитан состав газовой смеси: а) при сжигании S в воздухе; б) при обжиге FeS2; в) при смешении SO2 c воздухом. Было исследовано влияние концентрации, температуры и давления на данные процессы. Было определено, что при уменьшении температуры, увеличении давления и при увеличении соотношения кислорода к сернистому газу равновесная степень превращения растет. Константа равновесия реакции окисления SO2 с ростом температуры падает, что соответствует экзотермической реакции.
