
диссертации / 63
.pdfStorz (Германия) под эндотрахеальным наркозом с созданием карбоксипери-
тонеума 12-15 мм.рт.ст. При необходимости в брюшную полость устанавли-
вались дополнительные троакары и с помощью эндоскопических инструмен-
тов проводилась ревизия петель кишечника или исследование микроцирку-
ляции кишечника с помощью зонда лазерного флоуметра.
2.2.6. Компьютерная томография органов брюшной полости, КТ-
ангиография абдоминальной аорты и ее ветвей.
Компьютерную томографию органов брюшной полости провели у 44
пациентов (27,0%) на мультиспиральном компьютерном томографе Brillians
СТ фирмы Phillips (Нидерланды) с диапазоном сканирования от диафрагмы до уровня лобкового сочленения, коллимацией рентгеновского излучения
0,625, питч 1,172 и толщиной реконструкции 2 мм. Протокол включал полу-
чение топограммы в аксиальной проекции и исследование с болюсным кон-
трастным усилением.
КТ–ангиография (7 больных или 4,3%) выполнялась после внутривен-
ного болюсного введения неионного контрастного вещества Омнипак 350-
100 мл автоматическим инжектором, присоединенного к кубитальному или центральному катетеру, со скоростью введения контрастного препарата 4
мл/секунду, в объеме 80-100 мл. Задержка начала сканирования устанавлива-
лась автоматически по программе Bolus tracking, с установкой триггера на нисходящей аорте на уровне купола диафрагмы. Сканирование начиналось на 5 секунде от достижения порогового значения плотности крови в аорте с задержкой дыхания 5 секунд. Анализ изображения проходил на рабочей станции EBW фирмы Philips в аксиальной, коронарной и саггитальной про-
екциях с шириной окна 360/60, с использованием центра ротации, построе-
нием многоплоскостных реформаций и объемной 3D реконструкцией.
2.2.7. Микробиологическое исследование.
Посевы крови брались из периферической вены до операции, интрао-
61
перационно из брыжеечной вены, а также в послеоперационном периоде ежедневно в течение 7 послеоперационных суток. Всего выполнено 34 мик-
робиологических исследований с применением сред “Bact/ALERT” ® FA
(Франция) для аэробной и анаэробной флор.
2.2.8. D-димеры.
Концентрацию D-димеров определяли у 46 (28,2%) пациентов с ОНМзК и у 25 больных при подозрении на острое нарушение брыжеечного кровообращения при помощи количественного иммунотурбидиметрического метода на анализаторе “Sysmex CA 1500”, реагентами фирмы “Siemens”
(Германия). Метод основан на способности частиц латекса, покрытых моно-
клональными антителами DD5 к продуктам дегидратации фибрина (D-
димеры), агглютинировать при смешивании с плазмой крови, содержащей D-
димеры даже в минимальной концентрации.
2.2.9. Оценка нутритивного статуса пациента.
Нутритивный статус пациентов, перенесших ОРК, оценивали с помо-
щью прогностического индекса гипотрофии (ПИГ) [31], рассчитываемого по формуле:
ПИГ (%) = 140 – 1,5 (А) – 1 (ОП) – 0,5 (КЖСТ) – 20 (Л), где А – альбумин сыворотки крови (г/л), ОП – окружность плеча (см),
КЖСТ – кожно-жировая складка под трицепсом (мм), Л – абсолютное число лимфоциты крови (тысяча в 1 мкл).
Показатели ПИГ от 0 до 20% характеризовали нормальный статус пи-
тания, от 21 до 30% гипотрофию I (легкой) степени, от 31 до 40% гипотро-
фию II (средней тяжести) и более 40% как гипотрофию III (тяжелая) степени.
Нутритивный статус пациентов оценивался перед переводом из реанимаци-
онного отделения, перед выпиской из стационара, а также в отдаленном пе-
риоде в свете оценки отдаленных результатов лечения данной группы боль-
ных.
62
2.2.10. Морфологическое исследование кишечника
Морфологическому исследованию подвергался кишечник, резециро-
ванный у 103 (63,2%) пациентов, особое внимание уделялось краям резекции кишки с целью морфологического подтверждения их жизнеспособности или нежизнеспособности. Окраску материала осуществляли гематоксилин-
эозином и покрофуксином по Ван-Гизону, увеличение 200. Материалы ис-
следовали при помощи светооптических микроскопов Leica DMLS и Leica DM 1000, а также с помощью полляризационного микроскопа Leica DM 2000.
2.2.11. Экстракорпоральные методы детоксикации.
Экстракорпоральная детоксикация (сеансы высокообъемной вено-
венозной гемофильтрации и гемодиафильтрации) проводилась в непрерыв-
ном режиме на аппарате “Prismaflex” (Gambro-Hospal) в режиме постдилю-
ции с использованием бикарбонатных растворов Prismasol 4 (Gambro-Hospal).
Фильтр HF 1400. Под непрерывным режимом понимали продолжительность процедуры более 12 часов в сутки (в большинстве случаев – круглосуточно).
Всем пациентам (n=7 или 4,3%) за расчетную дозу принималась так называе-
вая “септическая”, которая составляла в среднем 45 мл/кг/час.
2.3. Методы статистической обработки
Статистический анализ проведен при помощи пакета программ Microsoft Office Excel с выявлением достоверности различий при помощи кри-
терия Стьюдента или критерия согласия χ2. Однофакторный и многофактор-
ный дисперсионный анализ данных с целью выявления независимых предик-
торов летальности у пациентов с ОНМзК выполнен с использованием про-
граммы IBM SPSS 18 for Windows (SPSS Inc., USA).
63
Решая поставленные задачи, в процессе выполнения данной работы мы разделили всех 163 оперированных больных на две группы: контрольную и основную. Принципом разделения больных на группы стало начало приме-
нения разработанного лечебно-диагностического алгоритма у больных с ост-
рой интестинальной ишемией.
Контрольная группа (n=61, с 2007 по 2009 гг.) и основная группа
(n=102, с 2010 по 2013 гг.) по возрасту, полу, количеству сопутствующих за-
болеваний, причине острой окклюзии ВБА, объему и характеру выполненно-
го оперативного пособия были сопоставимы между собой (табл. 2).
Таблица 2. Сравнительные характеристики контрольной и основной групп пациентов.
|
Контрольная |
Основная |
p |
|
группа (n=61) |
группа (n=102) |
|
|
|
|
|
Возраст |
73,6±10,3 |
71,0±12,3 |
0,86 |
|
(медиана 76) |
(медиана 73) |
|
|
|
|
|
Пол (мужчины/женщины) |
34,4% / 65,6% |
33,3% / 66,7% |
0,89/0,92 |
|
|
|
|
Эмболия/тромбоз ВБА |
29,5% / 63,9% |
40,2% / 52,9% |
0,19/0,31 |
|
|
|
|
Тромбоз НБА |
6,6% |
5,9% |
0,4 |
|
|
|
|
Сопутствующие заболевания |
4,1±1,7 |
3,9±1,5 |
0,94 |
|
|
|
|
Оперативные вмешательства: |
|
|
|
|
|
|
|
Комбинированные операции |
36,1% |
36,3% |
0,98 |
|
|
|
|
Изолированные резекции |
27,9% |
26,5% |
0,85 |
|
|
|
|
Изолированные |
3,3% |
5,9% |
0,39 |
эмбол/тромбэктомии |
|
|
|
|
|
|
|
Эксплоративные лапаротомии |
31,1% |
31,4% |
0,97 |
|
|
|
|
64
Глава 3.
Диагностика, хирургическая тактика и результаты лечения
острого нарушения мезентериального кровообращения в
контрольной группе пациентов.
Контрольную группу составили 63 пациента, проходивших лечение в
2007 – 2009 годах.
3.1. Диагностика и лечение острого нарушения мезентериального
кровообращения в контрольной группе.
В этой группе лечебно-диагностический алгоритм при ОНМзК был стандартен. При поступлении выполняли полноценный лабораторный ана-
лиз: общий анализ крови, биохимия крови, коагулограмма, группа крови и резус-фактор. Пациентам с не ясным диагнозом и отсутствием типичной клинической картины выполняли стандартную инструментальную диагно-
стику: УЗИ органов брюшной полости и забрюшинного пространства, обзор-
ная рентгенография органов брюшной и грудной полости, ЭКГ), в обязатель-
ном порядке больной консультировался необходимыми специалистами (те-
рапевт, невролог) по поводу сопутствующей патологии.
В случае возникновения клинического подозрения на тромбоз или тромбоэмболию брыжеечных артерий, пациентам в обязательном порядке выполняли ангиографию брюшного отдела аорты и ее непарных висцераль-
ных ветвей. Когда диагноз оставался не ясен, и подозрение на ОНМзК не возникало, т.е. исключалось другое ургентное хирургическое заболевание ор-
ганов брюшной полости, выполняли видеолапароскопию.
Видеолапароскопическое исследование в контрольной группе осущест-
влено у 34 (55,7%) пациентов. Диагноз ОНМзК установлен был в 28 (82,4%)
случаях, исключен у 6 (17,6%) из 34 больных. Частота встречаемости различ-
ных эндоскопических признаков острого нарушения брыжеечного кровооб-
65

ращения представлена на рисунке 6.
Рисунок 6. Частота встречаемости эндоскопических признаков острого нарушения брыжеечного кровообращения
Наиболее часто встречался серозно-геморрагический выпот (32,4% или
11 из 34 больных), выявленный у трети пациентов (рис. 7), реже серозный
(11,8% или 4 пациента), бурый (8,8% или 3 больных) и гнойный (2,9% или 1
больных). В остальных 2 случаях описание характера выпота отсутствовало.
Рисунок 7.
Некротизированная петля под-
вздошной кишки с серозно-
геморрагическим выпотом в латеральном канале
Фибрин обнаружен у 7 (20,6%) пациентов (рис. 8), а изменение цвета тонкой и/или толстой кишки выявлено в 26 (76,5%) случаях.
66
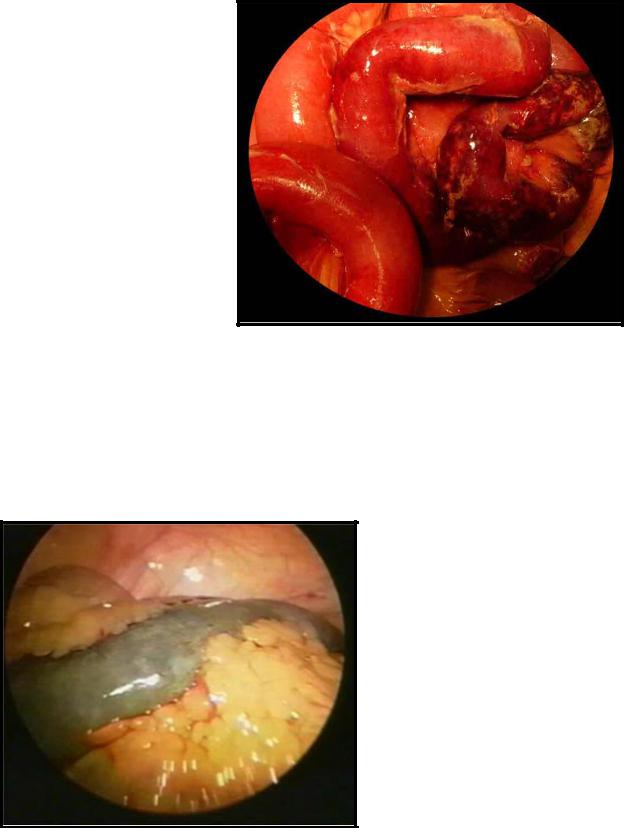
Рисунок 8.
Налет фибрина на некротизированных и ишемизированных петлях тонкой кишки
Некротизированный кишечник черного цвета с пятнами грязно-
зеленого цвета (рис. 9) на стенке кишки диагностирован на видеолапароско-
пии у 12 пациентов (35,3%), у чуть меньшего количества больных (29,4% или
10 пациентов) цвет кишки был синюшно-багровый, а в 1 случае (2,9%) тон-
кая кишка имела бледно-серую окраску.
Рисунок 9.
Некротизированная сигмовидная кишка
Ослабление перистальтики кишечника обнаружено у 12 (35,3%) паци-
ентов, отсутствие перистальтики диагностировано в 3 (8,8%) случаях, у ос-
тальных 19 больных перистальтическая активность кишечника была нор-
мальной.
67
Сочетание 2 или 3 признаков ишемии и/или некроза кишечника имело место в большинстве случаев: изменения цвета кишечника с патологическим выпотом в брюшной полости встретилось у 24 больных (70,6%).
В группе пациентов (n=6), где при первичном видеолапароскопическом исследовании диагноз ОНМзК был исключен, далее, в ходе динамического наблюдения отмечена отрицательная динамика и эти пациенты оперированы уже в стадии некроза кишечника.
Анализируя причины диагностических ошибок при видеолапароско-
пии, мы выделили следующие:
1. Визуальное отсутствие внешних признаков ишемии и некроза кишечника: двое пациентов без внешних признаков деструктивного пораже-
ния кишечника и с отсутствием перистальтики тонкой кишки, оказались в стадии ишемии кишечника и оперированы в дальнейшем на фоне обширного некроза кишечника. Видеолапароскопия проводилась предположительно в стадии ишемии кишечника. Это явилось причиной задержки операции, кото-
рая в итоге была выполнена на фоне обширного некроза кишечника.
2.Неверная трактовка данных, полученных во время видеолапаро-
скопии: у пациентов с отягощенным алкогольным анамнезом и выраженны-
ми нарушениями в диете накануне поступления в больницу имелся бурый выпот в брюшной полости с пневматозом петель тонкой кишки, что было расценено как проявления острого деструктивного панкреатита (геморраги-
ческий панкреонекроз).
Таким образом, чувствительность видеолапароскопии, выполненной при подозрении на ОНМзК, по нашим данным составила 82,4%: диагноз при эндохирургическом исследовании установлен был правильно в 28 из 34 слу-
чаев.
68
Объем и характер оперативного пособия зависел от уровня поражения ВБА и объема поражения кишечника. В случае острой окклюзии устья и про-
ксимальных отделов ВБА, осложненной распространенным некрозом кишеч-
ника, первым этапом выполняли обструктивную резекцию некротизирован-
ного кишечника с последующим восстановлением магистрального кровотока в бассейне ВБА – прямая или непрямая эмболили тромбэктомия из ВБА.
Границы жизнеспособности пораженного кишечника интраоперацион-
но определяли только на основании клинических данных: цвет кишечника,
наличие перистальтики кишечника и пульсация артерий брыжейки.
Программированная релапаротомия выполнялась у пациентов через 12-
48 часов после первичного вмешательства для оценки жизнеспособности ос-
тавшегося кишечника, а также ревизии зоны реконструкции ВБА. В случае жизнеспособности кишечника и проходимости ВБА формировали одноряд-
ный или двухрядный межкишечный анастомоз по типу “бок в бок”. Прогрес-
сирование гангрены кишечника в случае неадекватной субъективной оценки жизнеспособности кишечника на первой операции, но на фоне сохраненного магистрального кровотока по ВБА, диктовало необходимость в ререзекции некротизированного кишечника и формирования межкишечного анастомоза.
В случае продолженного некроза тонкой и/или толстой кишки на фоне рет-
ромбоза зоны реконструкции ВБА, пациенту также выполняли ререзекцию кишки, повторную тромбэктомию из ВБА и планировали программирован-
ную релапаротомию через 12 – 24 часа.
При острой тромботической/тромбоэмболической окклюзии дисталь-
ных сегментов ВБА или тромбоза ее интестинальных ветвей, осложненных сегментарным, необширным некрозом кишечника, выполняли изолирован-
ную резекцию кишечника, а вопрос о наложении первичного межкишечного анастомоза решали в индивидуальном порядке.
Отдельно были проанализирована частота выполнения обширных
(длина оставшейся тонкой кишки менее 200 см) и необширных резекций ки-
шечника. Среди 39 пациентов, перенесших кишечную резекцию, доля об-
69
ширных вмешательств составила 69,2% (27 пациента), соответственно сег-
ментарные или необширные резекции кишки выполнены в 30,8% (12 боль-
ных) случае (p=0,0001).
Доля изолированных тонкокишечных резекций в контрольной группе составила 31,7 % (13 пациентов), толстокишечных резекций – 9,8% (4 боль-
ных), а частота дополнения резекции тонкой кишки правосторонней гемико-
лэктомией – 58,5 % (24 больных). Двадцать пациентов с тотальным некрозом кишечника в вышеуказанный расчет не принимались, как пациенты, которым не выполнялась какая-либо резекция.
Итогом данной тактики лечения пациентов с острым нарушением бры-
жеечного кровообращения стали следующие результаты. В первую очередь в контрольной группе нас интересовала частота развития прогрессирования некроза кишечника в раннем послеоперационном периоде в связи с неадек-
ватностью субъективной оценки его жизнеспособности. В соответствии с этой целью нами были проанализированы 41 пациент контрольной группы:
22 больных после комбинированных вмешательств, 17 пациентов после изо-
лированной резекции кишечника и 2 больных, которым была выполнена изо-
лированная тромбэктомия (n=1) и эмболэктомия (n=1) из ВБА.
Соответственно 20 пациентов с тотальным некротическим поражением кишечника, которым выполнялась только эксплоративная лапаротомия и ре-
визия органов брюшной полости, в анализ включены не были.
Частота выполнения программированных релапаротомий в контроль-
ной группе (n=41) в зависимости от вида оперативного вмешательства пред-
ставлена на рисунке 10.
70
