
- •Опыт Резерфорда по рассеянию альфа-частиц.
- •Атомная модель Бора. Постулаты Бора.
- •Атомная модель Бора. Строение энергетических уровней атома. Основное состояние. Энергия ионизации.
- •Атомная модель Бора. Квантование момента импульса, радиуса орбиты и энергии электрона.
- •Опыт Франка и Герца, подтверждающий существование дискретных энергетических уровней атома.
- •Линейчатые спектры излучения и поглощения разреженных газов. Серия Бальмера. Серия Пашена. Серия Лаймана. Обобщенная формула Бальмера.
- •Рентгеновское излучение. Устройство рентгеновской трубки. Спектр рентгеновского излучения. Закон Мозли.
- •Рентгеновское излучение и его получение в рентгеновской трубке. Тормозное рентгеновское излучение, его коротковолновая граница.
- •Поглощение, спонтанное и вынужденное испускание излучения. Вынужденные переходы. Инверсная заселенность уровней и способы ее создания.
- •Строение атомного ядра. Заряд, размер и масса атомного ядра. Капельная и оболочечная модели атомного ядра.
- •1936 Год — Нильс Бор
- •Нуклоны. Понятие о свойствах и природе ядерных сил.
- •Радиоактивный распад. Виды радиоактивных распадов. Закон радиоактивного превращения. Активность. Период полураспада, постоянная распада.
- •Ядерные реакции. Виды и механизмы ядерных реакций. Законы сохранения. Эффективное сечение реакции.
- •Реакции деления. Цепная реакция. Ядерная энергетика.
- •Ионизирующее излучение. Дозиметрия ионизирующих излучений.
- •Физические основы квантовой механики. Принцип соответствия. Принцип причинности. Принцип дополнительности.
- •Принцип неопределенности Гейзенберга. Неопределенность координат и времени. Неопределенность энергии и импульса.
- •Уравнение Шредингера. Волновая функция и ее статистический смысл.
- •Потенциальный порог (потенциальная ступень). Прохождение частицей потенциального барьера конечной высоты. Туннельный эффект.
- •Квантовые числа атома. Моменты импульса атома: орбитальный, спиновый, результирующий.
- •Квантовые числа атома. Принцип запрета Паули. Заполнение оболочек и подоболочек в атоме.
- •Квантово-механическая модель строения атома.
- •Магнитные свойства атома. Орбитальный и спиновый магнитные моменты. Полный магнитный момент. Эффект Зеемана.
- •Энергия молекулы. Колебательные и вращательные уровни. Молекулярные спектры. Комбинационное рассеяние света.
- •Фундаментальные взаимодействия. Элементарные частицы и античастицы.
- •Виды взаимодействий и их объединение в рамках единой теории. Классификация элементарных частиц. Кварки.
Опыт Резерфорда по рассеянию альфа-частиц.
В свинцовом сосуде с небольшим отверстием (К) находился радиоактивный препарат, испускавший поток альфа-частиц. Они попадали на золотую фольгу (Ф) и, проходя через неё, ударялись о люминесцирующий экран (Э). В местах удара частиц на экране возникали вспышки света, которые наблюдались с помощью микроскопа (М). Вся эта установка помещалась в сосуд, в котором создавался вакуум.


Результаты: большинство альфа-частиц проходило через фольгу почти беспрепятственно, отклоняясь на углы, не превышающие 1-2 градуса; небольшая часть альфа-частиц рассеивалась на углы больше 2 градусов; примерно одна из каждых 20000 альфа-частиц отклонялась на углы в 90 и более градусов (т.е. назад).
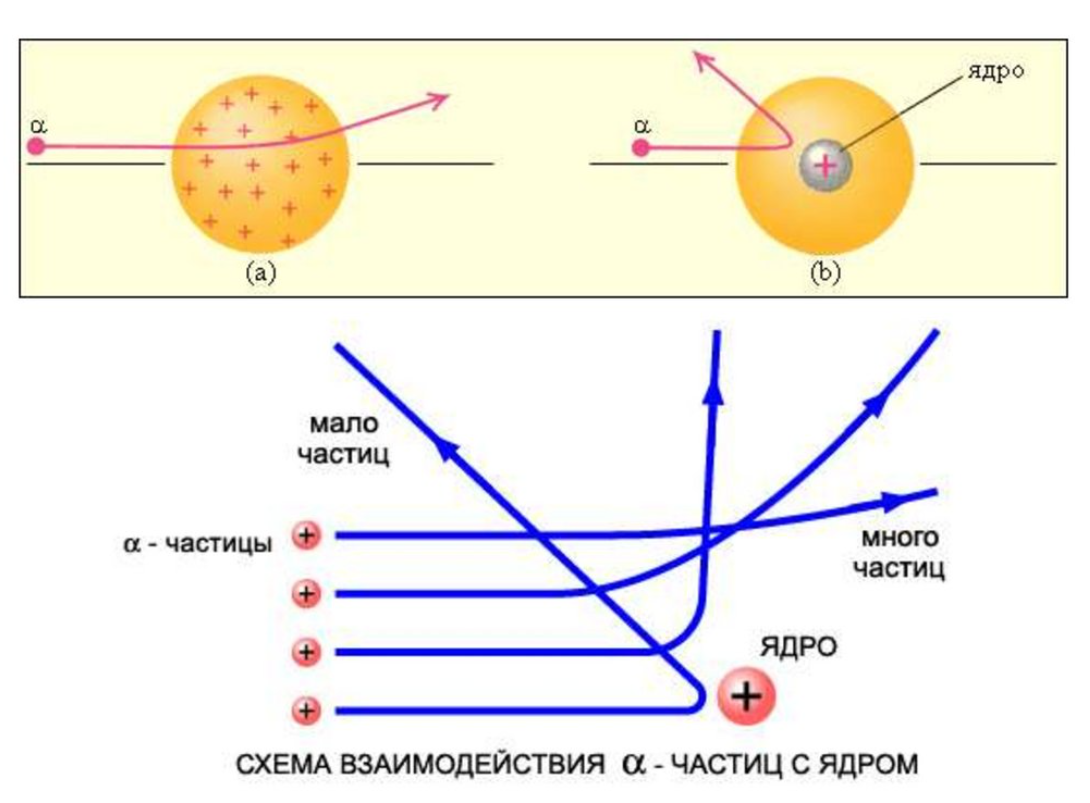
Опыты Резерфорда показали, что α-частицы, прошедшие чрез фольгу, то есть через электронную оболочку атомов фольги, встречая на своем пути электроны, практически на них не рассеиваются, так как масса электронов значительно меньше массы альфа-частицы. Рассеиваются только те α-частицы, которые вблизи ядра испытывают резкие отклонения.
Резерфорд показал, что модель Томсона находится в противоречии с его результатами. Резерфорд предложил ядерную (планетарную) модель строения атома. В центре атома находится положительное ядро, вокруг которого вращаются по определенным орбитам электроны. Основная масса атома сосредоточена в ядре. Атом электрически нейтрален - абсолютное значение суммарного заряда электронов ровно положительному заряду ядра.
Атомная модель Бора. Постулаты Бора.
Постулаты Бора:
1. Из бесконечного множества электронных орбит, которые возможны с точки зрения классической механики, реализуются в действительности только некоторые устойчивые стационарные орбиты, подчиняющиеся определённым условия отбора (квантования). Электрон, двигаясь по стационарной орбите, не излучает ЭМВ, хотя и движется с ускорение.
2. ЭМВ испускаются и поглощаются в виде кванта ЭМИ только при переходе электрона с одной стационарной орбиты на другую. Величина кванта излучения равна разности энергий, которые электрон имеет, двигаясь по орбитам.

3. Отбор стационарных орбит – правило квантования Бора: момент импульса электрона, движущегося по стационарной орбите, может принимать только дискретные значения, кратные постоянной Планка. Для круговых орбит правило квантования Бора имеет вид:
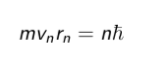

Боровская теория водородоподобного атома
П олуклассическая
модель атома, предложенная Нильсом
Бором в 1913 г. За основу он взял планетарную
модель атома, выдвинутую Эрнестом
Резерфордом. Однако, с точки зрения
классической электродинамики, электрон
в модели Резерфорда, двигаясь вокруг
ядра, должен был бы излучать энергию
непрерывно и очень быстро и, потеряв
её, упасть на ядро. Чтобы преодолеть эту
проблему, Бор ввёл допущение, суть
которого заключается в том, что электроны
в атоме могут двигаться только по
определённым (стационарным) орбитам,
находясь на которых они не излучают
энергию, а излучение или поглощение
происходит только в момент перехода с
одной орбиты на другую. Причём,
стационарными являются лишь те орбиты,
при движении по которым момент импульса
движения электрона равен целому числу
постоянных Планка (правило квантования).
олуклассическая
модель атома, предложенная Нильсом
Бором в 1913 г. За основу он взял планетарную
модель атома, выдвинутую Эрнестом
Резерфордом. Однако, с точки зрения
классической электродинамики, электрон
в модели Резерфорда, двигаясь вокруг
ядра, должен был бы излучать энергию
непрерывно и очень быстро и, потеряв
её, упасть на ядро. Чтобы преодолеть эту
проблему, Бор ввёл допущение, суть
которого заключается в том, что электроны
в атоме могут двигаться только по
определённым (стационарным) орбитам,
находясь на которых они не излучают
энергию, а излучение или поглощение
происходит только в момент перехода с
одной орбиты на другую. Причём,
стационарными являются лишь те орбиты,
при движении по которым момент импульса
движения электрона равен целому числу
постоянных Планка (правило квантования).
Точечный электрон −e и точечное ядро +Ze;
Адиабатическое приближение — ядро неподвижно.
