
- •Организация дыхательной цепи митохондрий, синтез АТФ. Внемитохондриальное окисление. Микросомальное окисление. Свободно-радикальное окисление, токсические
- •Основные вопросы лекции:
- •Современные представления о биологическом окислении.
- •Митохондриальное окисление. Дыхательная цепь митохондрий,
- •Существует строгая последовательность работы каждого звена в ЦПЭ, которая определяется величиной
- •Компоненты дыхательной цепи имеют редокс - потенциалы, занимающие промежуточное
- •Структурная организация дыхательной цепи ( ЦПЭ )
- •Комплекс I: НАДН-дегидрогеназа.
- •КоQ – убихинон (греч. «вездесущий») -
- •Комплекс III: КоQ - Н2-дегидрогеназа
- •Цитохром С играет исключительную роль в процессах тканевого дыхания.
- •Комплекс IV: Цитохром с–оксидаза (цитохром а-а3)
- •Комплекс ΙΙ: Сукцинат-убихинон-оксидоредуктаза (сукцинатдегидрогеназа)
- •Ингибиторы дыхательной цепи (ЦПЭ).
- •Итоги тканевого дыхания:
- •При функционировании ЦПЭ создается электрохимический градиент концентрации протонов
- •Тканевое дыхание выполняет:
- •Механизм синтеза АТФ.
- •Механизм синтеза АТФ.
- •Для оценки эффективности работы ЦПЭ предложен коэффициент фосфорилирования (Р/О)
- •Метаболизм в клетке регулируется соотношением АТФ / АДФ
- •Трансформация энергии в клетке проходит следующие этапы:
- •Гипоэнергетические состояния – это разнообразные по этиологии состояния, при которых
- •Гипоксия — пониженное содержание кислорода в организме или органах и тканях. Вследствие гипоксии
- •Разобщение дыхания и фосфорилирования.
- •Примеры действия разобщителей тканевого дыхания и фосфорилирования.
- •Примеры действия разобщителей тканевого дыхания и фосфорилирования
- •Клетки бурого жира содержат большое количество митохондрий, которые и придают ткани буро-красный цвет.
- •Нефосфорилирующее окисление в дыхательной цепи как механизм образования теплоты.
- •Виды биологического окисления.
- •Особенности оксидазного типа окисления
- •Бактерицидное действие фагоцитирующих лейкоцитов.
- •Окисление оксигеназного типа.
- •Оксигеназы работают в составе мультиферментного комплекса, состоящего из 3-х компонентов:
- •Цитохром Р450-зависимые монооксигеназы катализируют превращение веществ разного типа.
- •Кислород является самым распространенным элементом на Земле.
- •Токсичность кислорода. Активные формы кислорода (АФК) и реакции
- •АФК образуются в ЦПЭ в результате последовательного одноэлектронного присоединения к молекуле О2.
- •АФК реагируют с практически любой молекулой, извлекая из нее электроны.
- •Перекисное окисление мембранных липидов (ПОЛ) является причиной повреждения клеток.
- •ПОЛ - цепные реакции, обеспечивающие расширенное воспроизводство свободных радикалов
- •Обрыв цепи ПОЛ.
- •Принципы взаимодействия живых систем с агрессивной для них кислородной средой.
- •Ферменты АОЗ
- •Ферменты АОЗ
- •Ферменты АОЗ
- •Витамины - антиоксиданты
- •Кофермент Q10 в отличие от других антиоксидантов регенерируется организмом. КоQ10 восстанавливает антиоксидантную активность
- •Витамин Р
- •Благодарю за внимание!
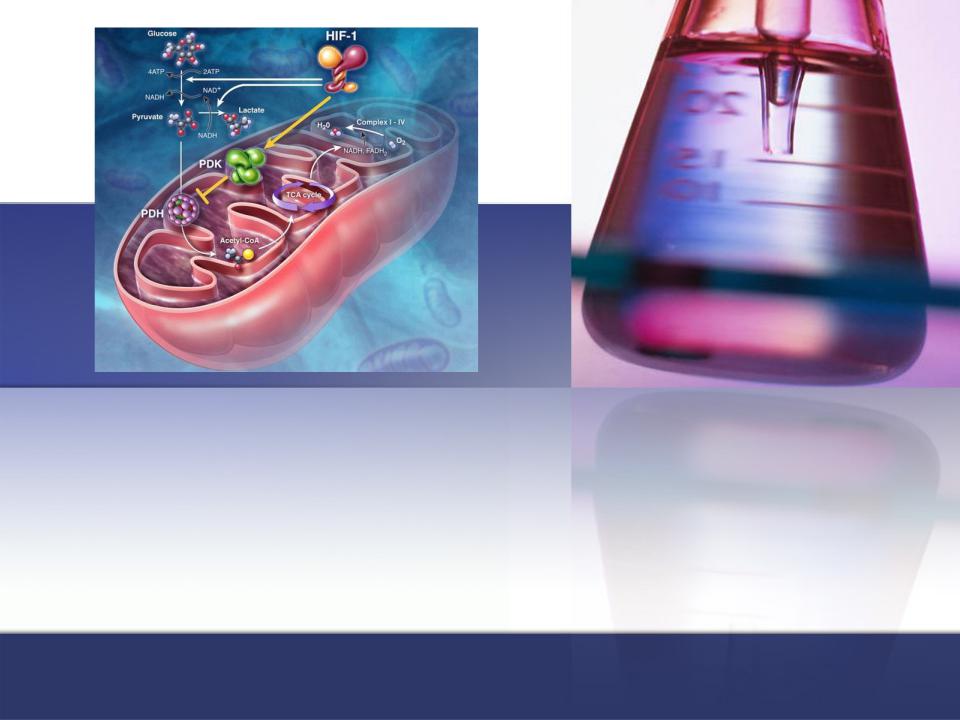
Организация дыхательной цепи митохондрий, синтез АТФ. Внемитохондриальное окисление. Микросомальное окисление. Свободно-радикальное окисление, токсические формы кислорода. Антиоксидантная защита.
Лекция для специальности 31.05.01 Лечебное дело подготовлена доцентом кафедры общей и биологической химии ТГМУ О.А. Артюковой
2017–2018 учебный год

Основные вопросы лекции:
Организация дыхательной цепи митохондрий: мультиферментные комплексы, переносчики электронов.
Хемиосмотическая теория синтеза АТФ. Образование и использование электрохимического потенциала ( Н+).
Протонная АТФ-аза и транспортные системы митохондрий.
Окислительное фосфорилирование, коэффициент Р/О. Дыхательный контроль.
Ингибиторы дыхательной цепи и разобщители с окислительным фосфорилированием. Энергетический обмен и теплопродукция.
Внемитохондриальные виды окисления. Микросомальное окисление, особенности, физиологическое значение. Бактерицидное действие фагоцитирующих лейкоцитов.
Активные формы кислорода: образование, токсическое действие. Перекисное окисление мембранных липидов.
Механизмы защиты от токсического действия кислорода. Прооксиданты и антиоксиданты.

Современные представления о биологическом окислении.
Биологическое окисление – |
|
|
|
|
|
это совокупность окислительных |
|
Биологическое |
|||
процессов в живой клетке. |
|
|
|||
|
|
|
окисление |
||
Окисление одного вещества |
|
|
в клетке |
||
невозможно без восстановления |
|
|
|
|
|
другого вещества. |
|
|
|
|
|
|
|
|
|
|
|
В клетке окисление происходит |
|
|
|
|
|
|
|
|
|
|
|
как в аэробных, так и в |
|
|
|
|
|
анаэробных условиях. |
|
|
|
|
|
Митохондриальное |
Вне- |
||||
|
митхондриальное |
||||
В аэробных организмах |
|
окисление |
|||
|
окисление |
||||
существует несколько |
|
осуществляется |
|||
|
осуществляется |
||||
путей использования |
|
путем отнятия Н2 |
|||
|
путем |
||||
кислорода в процессах |
|
от окисляемого S |
присоединения О2 |
||
|
и переноса его |
||||
биологического окисления: |
|
к окисляемому S |
|||
|
на O2 |
||||
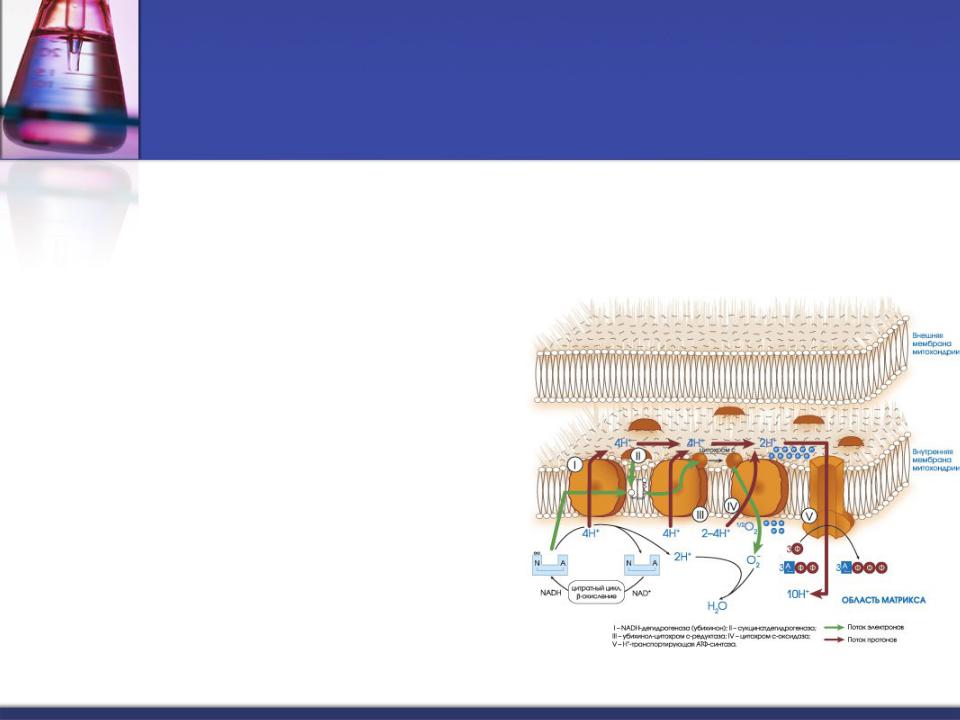
Митохондриальное окисление. Дыхательная цепь митохондрий,
тканевое дыхание, цепь переноса электронов (ЦПЭ)
Мультиферментная система, встроена в кристы митохондрий
(участвует около 40 различных белков и ферментов).
Комплекс ферментов отнимает водород от субстратов и через систему переносчиков последовательно передает на кислород
собразованием воды:
SH2 + ½ O2  S + H2O
S + H2O
Окисление и фосфорилирование (синтез АТФ) между собой сопряжены. В митохондриях потребляется
80 - 90% всего О2.
Окислительное фосфорилирование в ЦПЭ – основной источник образования АТФ в клетках.

Существует строгая последовательность работы каждого звена в ЦПЭ, которая определяется величиной
редокс-потенциала (окислительно - восстановительного потенциала)
Редокс - потенциал – это химическая характеристика способности вещества принимать и
удерживать электроны (e). Величины выражаются в вольтах (V).
В каждой окислительно-восстановительной системе участвует окисленная и
восстановленная формы одного соединения, |
которые образуют сопряженную |
редокс - пару. |
|
Разные редокс-пары обладают различным сродством к e.
Вещества с положительным редокс-потенциалом окисляют водород (отнимают у него e).
Вещества с отрицательным редокс-потенциалом сами окисляются водородом.
|
Самое низкое сродство к e у водорода (- 0,42 V) . |
|
Самое высокое сродство к e у кислорода (+ 0,82 V). |
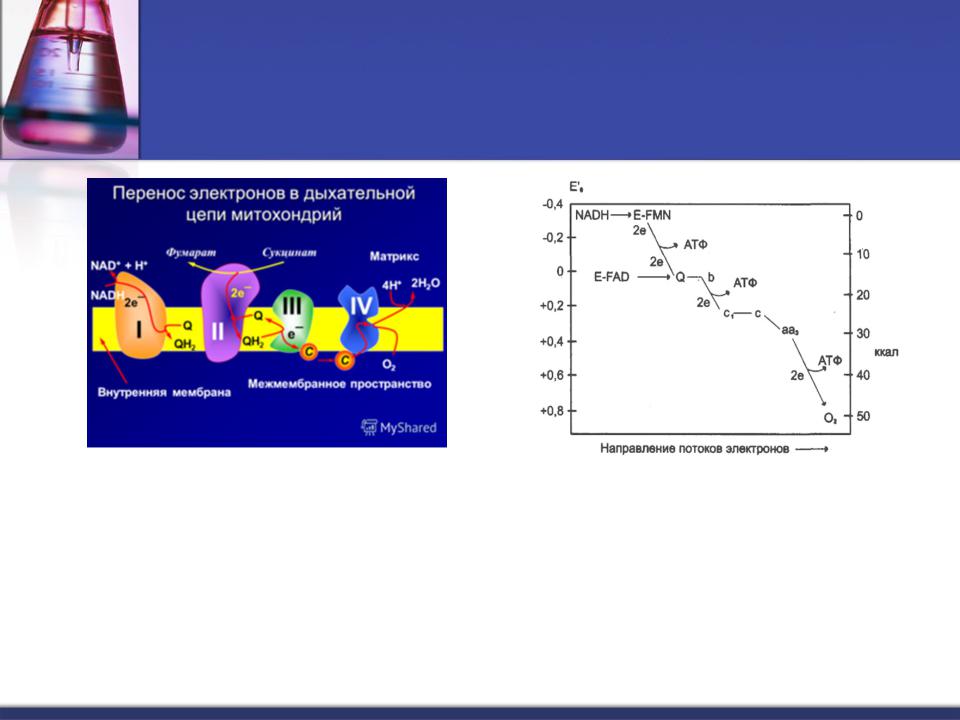
Компоненты дыхательной цепи имеют редокс - потенциалы, занимающие промежуточное
положение между - 0,42 V и + 0,82 V.
|
В ЦПЭ вещества, переносящие e, располагаются в порядке увеличения их |
|
|
редокс –потенциала. e перемещается по ЦПЭ от веществ с низким сродством к |
|
|
e к веществам с более высоким сродством к e , |
при этом |
|
происходит высвобождение свободной энергии, |
часть |
|
которой фиксируется в виде макроэргических связей. |
|
|
Электроны в ЦПЭ поставляют субстраты тканевого дыхания |
|
|
(реакции цикла Кребса и др.) |
|

Структурная организация дыхательной цепи ( ЦПЭ )
Выделяется 4 комплекса переносчиков электронов (комплексы I, II, III, IV).
Комплексы расположены по своему окислительно-восстановительному потенциалу.
Транспорт электронов в цепи протекает самопроизвольно.

Комплекс I: НАДН-дегидрогеназа.
Состоит из 26 полипептидных цепей. Содержит ФМН (вит. В2), 5 FeS – белков (кластеров)
Функции:
-Принимает водород от НАДН-Н
-Разделяет поток протонов и e
Используя энергию транспорта e, работает как протонный генератор - перебрасывает из матрикса 4 Н+ в межмембранное пространство. Восстанавливает промежуточный переносчик –
кофермент Q (убихинон) до QН2 (убихинол).

КоQ – убихинон (греч. «вездесущий») -
промежуточный переносчик протонов и электронов.
.
Q10 восстанавливается на внутренней стороны мембраны и окисляется на другой, при этом
происходит перенос Н+ через мембрану.
Q10 - липид, радикал которого у млекопитающих образован 10 изопреноидными единицами. Витаминоподобное вещество.
Клеточный энергетик.
Синтез в организме снижается с возрастом.
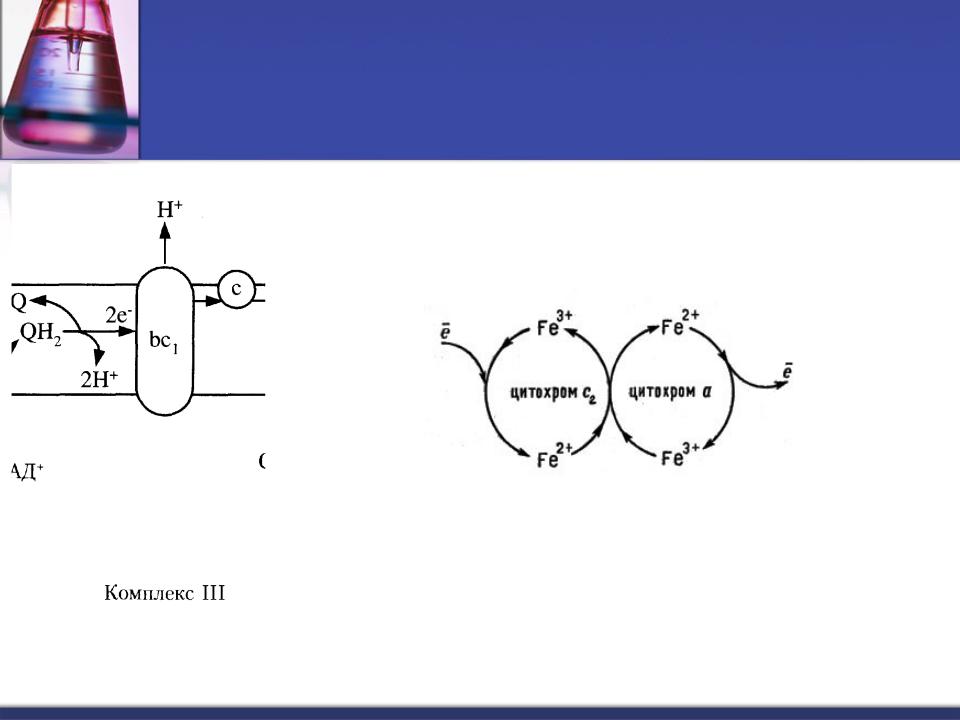
Комплекс III: КоQ - Н2-дегидрогеназа
Содержит цитохромы ( b, c1, c)
Цитохромы - сложные белки, содержащие ГЕМ. Принцип действия цитохромов:
Fe изменяет свою степень окисления, передавая e
QH2 + 2 цитохром С (окисл.) + 2H+ (матрикс) → Q + 2 цитохром С (восст.) + 4H+
Комплекс транспортирует 2е-, работает как протонный генератор - осуществляет выброс еще 4Н+ из матрикса в межмембранное пространство.
