
Большой практикум / Культивирование / Влияние концентрации азота на характеристики культуры
.pdfФедеральное государственное автономное образовательное учреждение
высшего образования «СИБИРСКИЙ ФЕДЕРАЛЬНЫЙ УНИВЕРСИТЕТ»
Институт фундаментальной биологии и биотехнологии
Базовая кафедра биотехнологии
ОТЧЕТ ПО ЛАБОРАТОРНОЙ РАБОТЕ
Изучение влияния концентрации азота в среде на ростовые характеристики культуры Cupriavidus eutrophus B-10646
Преподаватель |
|
|
|
Н. О. Жила |
||
|
|
|
подпись, дата |
|
инициалы, фамилия |
|
Студент |
|
|
|
|
|
|
|
номер группы, номер зачетной книжки |
подпись, дата |
|
инициалы, фамилия |
||
Красноярск 2020
Цель работы: продемонстрировать потенциальные возможности параметрически управляемого культивирования микроорганизмов для получения целевых продуктов.
Ход работы:
1.Студентам разделиться на 4 группы по числу заданных значений концентрации хлористого аммония в среде (1,0; 0,6; 0,4 и 0,2 г/л).
2.Каждой группе приготовить вариант питательной среды Шлегеля для бактерий с заданным значением азота в двух повторностях:
•в микробиологическом боксе в колбу на 0,5 л с 200 мл фосфатного буфера
(Na2HPO4∙H2O – 9,1 г/л; KH2PO4 – 1,5 г/л) добавить 16 мл раствора фруктозы, 2 мл раствора сульфата магния (MgSO4 – 12 г/л), 1 мл лимоннокислого железа (Fe3C6H5O7∙7H2O – 50 г/л), 0,6 мл раствора микроэлементов (H3BO3 – 0,228 г/л; CoCe2∙6H2O – 0,030 г/л; СuSO4∙5H2O – 0,008 г/л; MnCe2∙4H2O – 0,008 г/л; ZnSO4∙7H2O – 0,176 г/л; NaMoO4∙2H2O – 0,050 г/л; NiCe2 – 0,008 г/л), NH4Cl исходя из заданной концентрации (2 мл для получения концентрации 1 г/л);
•в полученную среду добавить 10 мл инокулята культуры;
•колбы плотно закрыть резиновыми пробками, подписать;
•на ФЭК измерить оптическую плотность (без разведения) каждого инокулята в кювете 0,1 см на длине волны λ = 440 нм против воды;
3. Определить концентрацию фруктозы:
•2 мл культуральной жидкости отцентрифугировать при 6000 g в течение 2
минут;
•0,5 мл супернатанта развести в 24,5 мл воды (разведение в 50 раз);
•1 мл полученного раствора поместить в пробирку, куда добавить 3 мл раствора HCl (5:1) и 1 мл спиртового раствора резорцима;
•приготовить контроль, используя воду вместо надосадочной жидкости;
•поместить пробирки на водяную баню на 20 минут;
2

•на ФЭК измерить оптическую плотность каждого раствора в кювете 0,5 см на длине волны λ = 540 нм против контрольной пробы;
•построить калибровочный график, используя растворы фруктозы с известной концентрацией (2, 5, 10 и 20 г/л);
•найти концентрацию фруктозы в исследуемых растворах с помощью калибровочного графика (у = 0,0194 х + 0,1092);
4. Определить концентрацию азота:
•2 мл культуральной жидкости отцентрифугировать при 6000 g в течение 2
минут;
•0,5 мл супернатанта развести в 49,5 мл воды (разведение в 100 раз);
•добавить каплю щелочи (33% KOH) и 0,5 мл реактива Несслера;
•сразу измерить оптическую плотность каждого раствора в кювете 1 см на длине волны λ = 400 нм против воды;
•найти концентрацию азота в исследуемых растворах с помощью калибровочного графика (y = 1,6919 x – 0,1472);
5.Внести полученные данные в таблицу:
Таблица 1 – Начальные значения
0 ч
C NH4Cl, г/л |
OD (б/р) |
Биомасса, г |
C фруктоза, |
C NH4Cl, г/л |
|
г/л |
|||||
|
|
|
|
||
|
|
|
|
|
|
1,0 |
0,117 |
0,1 |
16 |
1,0 |
|
|
|
|
|
|
|
0,6 |
0,111 |
0,1 |
24 |
0,6 |
|
|
|
|
|
|
|
0,4 |
0,12 |
0,1 |
16 |
0,4 |
|
|
|
|
|
|
|
0,2 |
0,1 |
0,1 |
16 |
0,2 |
|
|
|
|
|
|
6.Через 16 часов повторить измерения оптической плотности культуральной жидкости с разведением (1 мл культуры и 5 мл воды) и без; определить концентрацию фруктозы и азота;
7.Измерить биомассу:
3

•20 мл культуральной жидкости отцентрифуриговать при 6000 g в течение
10 минут;
•промыть дистиллированной водой 3 раза, центрифугируя при тех же условиях;
•полученную биомассу перенести в заранее взвешенные бюксы и поставить сушиться при температуре 90 ;
•биомассу определять, как разницу между весом наполненного и пустого бюкса:
15,490 – 15,457 = 0,033 г
13,901 – 13,878 = 0,023 г x̅= 0,028 г
•по данным хроматографии масса полимера составила 44% от общей массы сухого остатка
Масса полимера (1 г/л) = 0,028 ∙ 50 = 1,4 г/л ∙ 44% = 0,61 г/л.
• внести полученные данные в таблицу:
Таблица 2 – Конечные значения
16 ч
C |
OD |
OD |
Биомасса, |
Содержание |
Содержание |
C |
C |
|
NH4Cl, |
полимера, |
полимера, |
фруктоза, |
NH4Cl, |
||||
(б/р) |
(с/р) |
г |
||||||
г/л |
% |
г/л |
г/л |
г/л |
||||
|
|
|
||||||
|
|
|
|
|
|
|
|
|
1,0 |
1,086 |
0,287 |
1,4 |
44 |
0,6 |
11,4 |
0,377 |
|
|
|
|
|
|
|
|
|
|
0,6 |
1,024 |
0,215 |
1,5 |
53 |
0,8 |
19,0 |
0,27 |
|
|
|
|
|
|
|
|
|
|
0,4 |
1,061 |
0,208 |
1,3 |
58 |
0,81 |
11,7 |
0,16 |
|
|
|
|
|
|
|
|
|
|
0,2 |
1,054 |
0,2 |
1,1 |
71 |
0,66 |
12,7 |
0,119 |
|
|
|
|
|
|
|
|
|
4
|
Биомасса, г |
|
|
|
|
|
|
|
1,6 |
|
|
|
|
|
|
|
|
1,5 |
|
|
|
|
|
|
|
|
1,4 |
|
|
|
|
|
|
|
|
1,3 |
|
|
|
|
|
|
|
|
1,2 |
|
|
|
|
|
|
|
|
1,1 |
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
C NH4Cl, г/л |
|
|
|
|
|
|
|
|
|
|
|
0 |
0,2 |
0,4 |
0,6 |
0,8 |
1 |
1,2 |
|
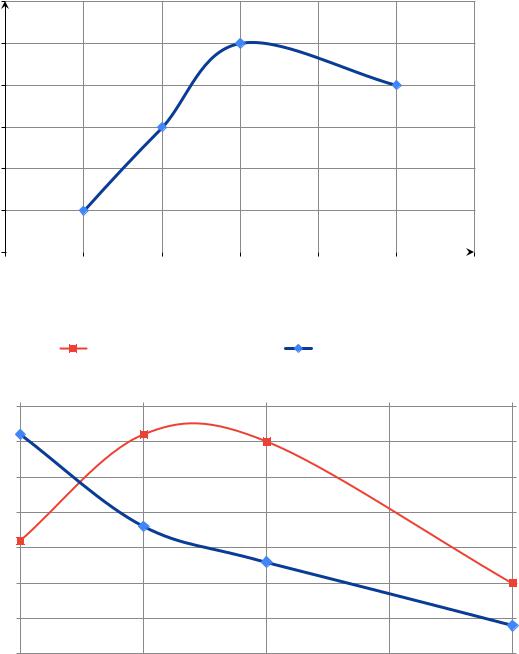
Рисунок 1 – График зависимости биомассы от концентрации NH4Cl |
|
|||||||
|
|
Содержание полимера, г/л |
Содержание полимера, % |
|
||||
|
|
|
|
Концентрация NH4Cl, г/л |
|
|
|
|
|
0,2 |
|
0,4 |
0,6 |
|
0,8 |
1 |
|
|
75 |
|
|
|
|
|
0,85 |
|
% |
70 |
|
|
|
|
|
0,8 |
г/л |
|
|
|
|
|
|
|
||
полимера, |
65 |
|
|
|
|
|
0,75 |
полимера, |
60 |
|
|
|
|
|
0,7 |
||
|
|
|
|
|
|
|
||
Содержание |
55 |
|
|
|
|
|
0,65 |
Содержание |
50 |
|
|
|
|
|
0,6 |
||
45 |
|
|
|
|
|
0,55 |
||
|
|
|
|
|
|
|
||
|
40 |
|
|
|
|
|
0,5 |
|
|
Рисунок 2 – График зависимости содержания полимера (г/л, %) от |
|
||||||
|
|
|
|
концентрации NH4Cl |
|
|
|
|
8. Рассчитать удельную скорость роста: |
|
|
|||||
|
= |
ln − ln 0 |
|
|
|||
|
|
|
|
|
|
||
|
|
|
|
||||
|
|
|
|
|
|
||
(1,0) = |
ln(1,4) − ln(0,1) |
= |
0,34 + 2,3 |
= 0,16 ч−1 |
= 16% в час |
||
|
16 |
|
|||||
16 |
|
|
|
|
|
||
|
|
5 |
|
|
|
||

9.Рассчитать экономический коэффициент
a)по биомассе:
биомасса
б = фрукт.нач. − фрукт.кон.
1,4 1,4б(1,0) = 16 − 11,4 = 4,6 = 0,3
b) по полимеру:
масса полимера
п = фрукт.нач. − фрукт.кон.
0,61 0,61п(1,0) = 16 − 11,4 = 4,6 = 0,13
10.Заполнить таблицу:
Таблица 3 – Влияние концентрации NH4Cl в среде на характеристики культуры
C NH4Cl, г/л |
μ, ч-1 |
Yбиомасса |
Yполимер |
|
|
|
|
1,0 |
0,16 |
0,3 |
0,13 |
|
|
|
|
0,6 |
0,17 |
0,3 |
0,16 |
|
|
|
|
0,4 |
0,16 |
0,3 |
0,19 |
|
|
|
|
0,2 |
0,14 |
0,3 |
0,2 |
|
|
|
|
Значение экономического |
коэффициента |
0,33
0,3
0,27
0,24
0,21
0,18
0,15
0,12
0,09
0,06
0,03
0
1 |
0,6 |
0,4 |
0,2 |
Концентрация NH4Cl, г/л
 Yб
Yб  Yп
Yп
Рисунок 3 – График зависимости экономических коэффициентов по
биомассе и полимеру в зависимости от концентрации NH4Cl
6
μ, ч-1
0,175
0,17
0,165
0,16
0,155
0,15
0,145
0,14
0,135
S NH4Cl, г/л
0,13
0 |
0,1 |
0,2 |
0,3 |
0,4 |
0,5 |
0,6 |
0,7 |
0,8 |
0,9 |
1 |
1,1 |
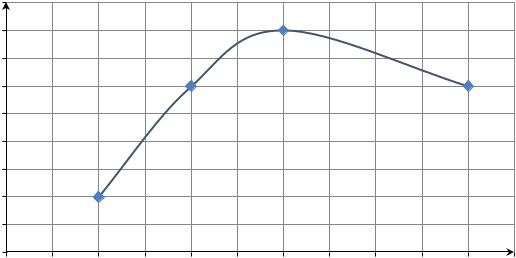
Рисунок 4 – График зависимости удельной скорости роста бактерий от концентрации NH4Cl в среде
11. Рассчитать константу насыщения KS и лимитирования KI. Для этого данные обработать по методу обратных величин Лайнуевера-Берка,
построить график и графически найти величину:
Таблица 4 – Линеаризация методом Лайнувера-Берка
C NH4Cl, г/л |
1,0 |
|
|
|
0,6 |
0,4 |
0,2 |
|
|
|
|
|
|
|
|
|
|
S NH4Cl, г/л |
- |
|
|
|
0,6 |
0,4 |
0,2 |
|
|
|
|
|
|
|
|
|
|
I NH4Cl, г/л |
1,0 |
|
|
|
0,6 |
- |
- |
|
|
|
|
|
|
|
|
|
|
μ, ч-1 |
0,16 |
0,25 |
|
0,17 |
0,16 |
0,14 |
||
|
|
|
|
|
|
|
|
|
1/S NH4Cl, л/г |
- |
|
|
|
1,66 |
2,5 |
5,0 |
|
|
|
|
|
|
|
|
|
|
1/I NH4Cl, л/г |
1,0 |
|
|
|
1,66 |
- |
- |
|
|
|
|
|
|
|
|
||
1/μ, ч |
6,25 |
4 |
|
|
5,88 |
6,25 |
7,14 |
|
|
|
|
|
|
|
|
|
|
7
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1/μ, ч |
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
8 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
7 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
6 |
|
|
|
|
|
|
|
|
|
y = 0,3733x + 5,2844 |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
1/S NH4Cl, л/г |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
|
|
|
|
|
|
|
|
|
|
|
|
-16 |
-14 |
-12 |
-10 |
-8 |
-6 |
-4 |
-2 |
0 |
2 |
4 |
6 |
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
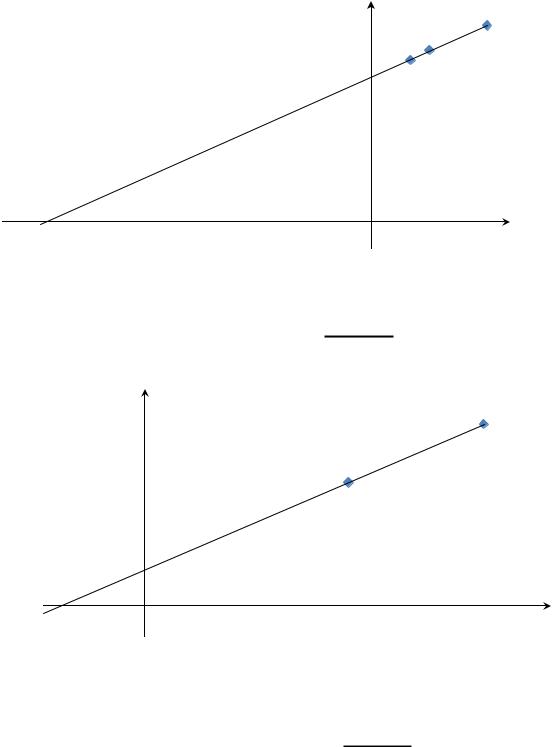
Рисунок 5 – График линеаризации методом Лайнувера-Берка для KS
По полученному графику, 1/ KS = – 14,2; KS = – 0,07.
|
|
|
|
1/μ, ч |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
7 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
6 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
y = 2,8235x + 1,1765 |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1/I NH4Cl, л/г |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-0,5 -0,3 -0,1 |
0,1 |
0,3 |
0,5 |
0,7 |
0,9 |
1,1 |
1,3 |
1,5 |
1,7 |
1,9 |
|||||||||||||||||||||||||||
-1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
Рисунок 6 – График линеаризации методом Лайнувера-Берка для KI
По полученному графику, 1/ KI = – 0,41; KI = – 2,4. По причине того, что значение удельной скорости роста для концентрации NH4Cl было найдено некорректно, константа лимитирования искалась исходя из значения μ (1,0) = 0,25.
8
Выводы:
1.Наибольшая биомасса должна была быть выделена при концентрации азота
1,0 г/л, однако при раскручивании произошла ошибка эксперимента, и не весь осадок был перенесен в бюксы, из-за чего значения биомассы не совпадают с ожидаемыми.
2.В результате нашего эксперимента было выявлено, что наиболее оптимальными концентрациями азота для синтеза полимера являются 0,4
г/л и 0,6 г/л, т. к. содержание в них полимера максимально (0,8 г/л и 0,81 г/л
соответственно). При концентрации азота 0,6 г/л наблюдается меньшее процентное содержание полимера, но большая биомасса (53%, 1,5 г), а при концентрации азота 0,4 г/л противоположное (58%, 1,3 г).
3.Бактерии запасают полимер, когда в среде имеется дефицит азота. При концентрации 1,0 г/л азота много, и происходит рост культуры без синтеза полимера (содержание полимера минимальное, биомасса максимальная).
При концентрации 0,2 г/л азота мало, и клетки запасают полимер, чтобы выжить, однако рост не такой активный (содержание полимера максимальное, биомасса минимальная).
4.Таким образом, наиболее подходящими для культивирования клеток и получения целевого продукта (полимера) являются концентрации азота в среде 0,4 г/л и 0,6 г/л.
9
