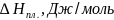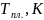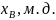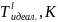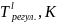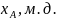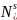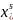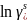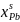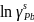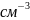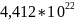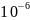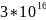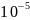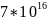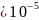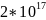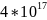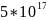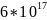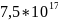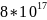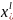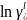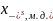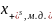лабы / Fkhot_laba2_Kryukova
.docxМИНОБРНАУКИ РОССИИ
Санкт-Петербургский государственный
электротехнический университет
«ЛЭТИ» им. В.И. Ульянова (Ленина)
Кафедра микро- и наноэлектроники
Лабораторная РАБОТА №2
по дисциплине «ФХОТ изделий электроники и наноэлектроники»
Тема: МОДЕЛИРОВАНИЕ ДИАГРАММ СОСТОЯНИЯ СОГРАНИЧЕННОЙ РАСТВОРИМОСТЬЮ КОМПОНЕНТОВ В (ПОЛУПРОВОДНИК – ПРИМЕСЬ)
Студентка гр. 8206 |
|
Крюкова И.А. |
Преподаватель |
|
Налимова С.С. |
Санкт-Петербург
2020
Цель работы: изучение фазовых равновесий в бинарной системе полупроводник (Si, Ge) – примесь методом компьютерного моделирования; расчет параметров межатомного взаимодействия; выбор моделей растворов, адекватно описывающих экспериментальную Т-х-проекцию диаграммы состояния; расчет спинодалей и определение областей устойчивого и метастабильного состояния твердых растворов в заданной системе.
Исходные данные
T-x-проекции фазовой диаграммы состояния, в том числе в крупномасштабном виде:
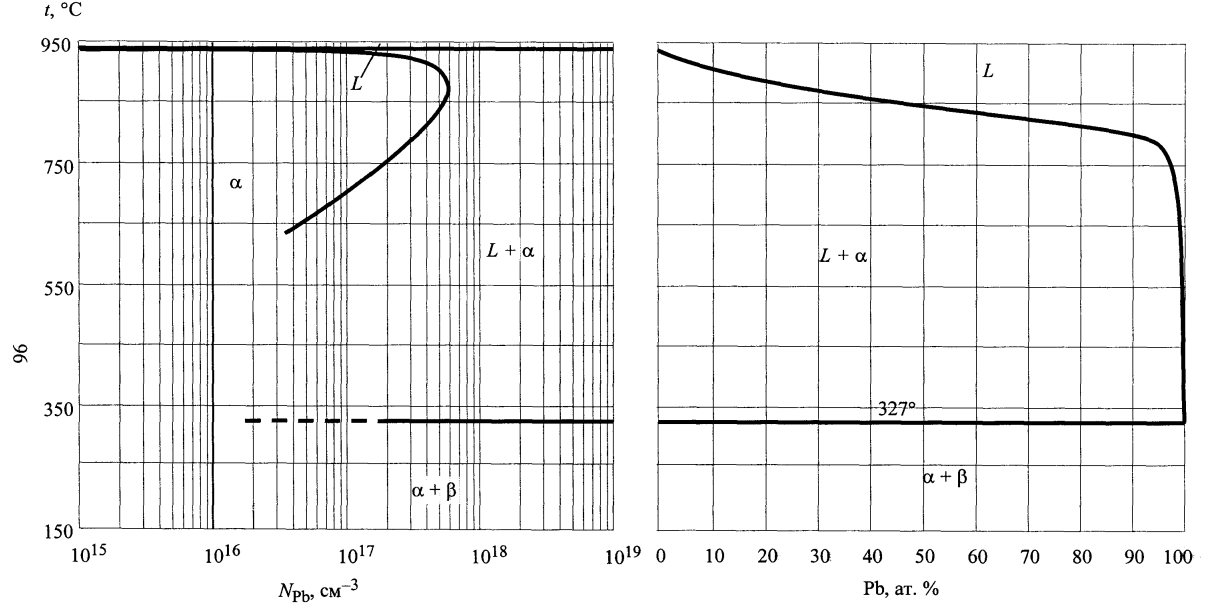
Рис.1 Характер фазового равновесия в системе Ge - Pb
температуры и энтальпии плавления исходных компонентов A и B, температура и состав точки эвтектики, а также значения периода решетки полупроводниковой фазы:
Таблица 1
Фаза |
|
|
Период решетки, нм |
Ge |
36945 |
1210,4 |
0,5657 |
Pb |
4799 |
600,6 |
- |
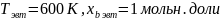
справочные данные о значениях параметров межатомного взаимодействия компонентов в жидком растворе в рамках моделей регулярных и квазирегулярных растворов:
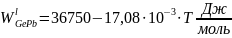
программа «Эвтектика», написанная в среде программирования LabView.
ОБРАБОТКА РЕЗУЛЬТАТОВ
Привести T-x проекции диаграмм состояния (в обычном и полулогарифмическом масштабах) исследованной диаграммы состояния и подобранные оптимальные параметры межатомного взаимодействия
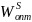 и
и
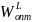 в жидком и твердом растворах соответственно.
в жидком и твердом растворах соответственно.
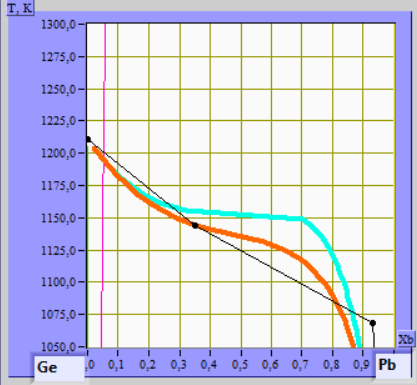
Рис. 2. Диаграмма состояния системы (линейный масштаб по оси составов)

Рис. 3. Диаграмма состояния системы (логарифмический масштаб по оси составов)
Полученные значения параметров взаимодействия:
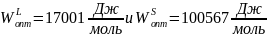 .
.
Рассчитать и построить линии ликвидуса в рамках модели идеального и регулярного жидких растворов. Сравнить линии ликвидуса, построенные в рамках моделей идеальных, регулярных и квазирегулярных растворов, с экспериментальной, приведенной на T-xпроекции. Выбрать модель, наиболее адекватно описывающую экспериментальные данные.
Таблица 2: Составная зависимость температуры для идеального и регулярного моделей растворов
|
|
|
|
0,00 |
1210,4 |
1210,4 |
1,00 |
0,10 |
1176,64806 |
1230,794 |
0,90 |
0,20 |
1141,07757 |
1246,096 |
0,80 |
0,30 |
1103,266049 |
1255,573 |
0,70 |
0,40 |
1062,617232 |
1258,211 |
0,60 |
0,50 |
1018,244879 |
1252,528 |
0,50 |
0,60 |
968,7355363 |
1236,206 |
0,40 |
0,70 |
911,5923993 |
1205,234 |
0,30 |
0,80 |
841,6216634 |
1151,453 |
0,20 |
0,90 |
743,9971282 |
1052,126 |
0,10 |
1,00 |
427,54 |
624,2813 |
0,00 |
Пример
расчета проведем для
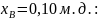
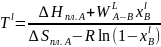 ,
где
,
где
 (для идеального р-ра)
(для идеального р-ра)
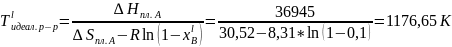
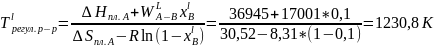
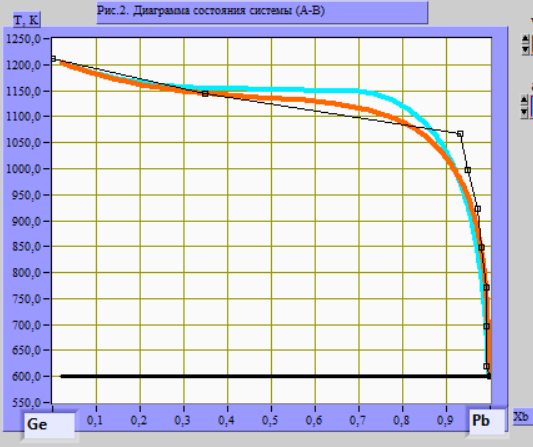
Рис. 4. Диаграмма состояния системы А-В
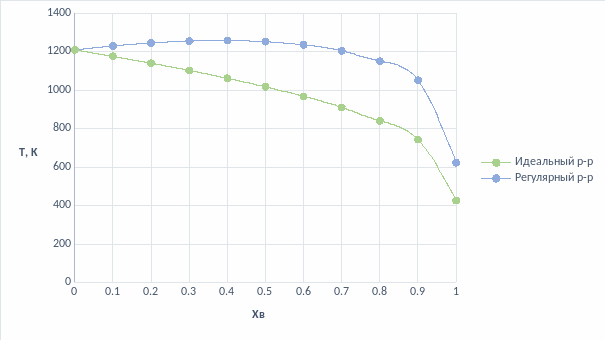
Рис. 5. Расчетная диаграмма состояния для моделей идеального и регулярного растворов
Из вышеприведенных рисунков для описания раствора видно, что для моделирования процессов раствора подходит модель регулярного раствора.
3. Рассчитать и построить концентрационные зависимости коэффициентов активности компонентов в твердом растворе при Т=const в пределах области растворимости, а также жидком растворе во всем диапазоне составов от x = 0 до 1. На тех же графиках построить зависимости, соответствующие модели идеального раствора.
Возьмем T=(Tэвт+ТплА)/2=905,2 К при максимальной растворимости.

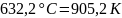
Рис. 6. Исходная диаграмма системы (логарифмический масштаб по оси состава)
Таблица 3: Концентрационные зависимости коэффициентов активности компонентов в твердом растворе
|
|
|
|
|
|
|
|
|
|
|
|
|
0,9999993 |
5,36778* |
|
0,0000007 |
13,36931998 |
0,9999984 |
2,75755* |
|
0,00000159 |
13,36929592 |
|
0,9999977 |
5,62766 |
|
0,00000227 |
13,3692772 |
|
0,9999954 |
3,80546* |
|
0,00000453 |
13,3692157 |
|
0,9999909 |
0,000225106 |
|
0,00000907 |
13,36909538 |
|
0,9999886 |
0,000900426 |
|
0,00001133 |
13,36903388 |
|
0,9999864 |
0,001406916 |
|
0,00001360 |
13,36897506 |
|
0,9999841 |
0,002025958 |
|
0,00001587 |
13,36891356 |
|
0,9999841 |
0,002757554 |
|
0,00001700 |
13,36891356 |
|
0,9999841 |
0,00316556 |
|
0,00001813 |
13,36891356 |
Пример
расчет для
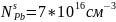 :
:
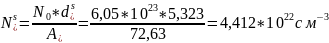
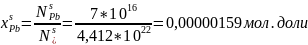
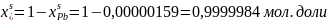
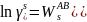
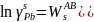
идеальный
р-р
Рис. 7. Концентрационная зависимость коэффициента активности для Ge в твердой фазе
Рис. 8. Концентрационная зависимость коэффициента активности для Pb в твердой фазе
Таблица 4: Концентрационные зависимости коэффициентов активности компонентов для жидкой фазы
|
|
|
|
|
|
|
|
1 |
0 |
0 |
1,690225 |
0,9 |
0,016902 |
0,1 |
1,369082 |
0,8 |
0,067609 |
0,2 |
1,081744 |
0,7 |
0,152120 |
0,3 |
0,828210 |
0,6 |
0,270436 |
0,4 |
0,608481 |
0,5 |
0,422556 |
0,5 |
0,422556 |
0,4 |
0,608481 |
0,6 |
0,270436 |
0,3 |
0,828210 |
0,7 |
0,152120 |
0,2 |
1,081744 |
0,8 |
0,067609 |
0,1 |
1,369082 |
0,9 |
0,016902 |
0 |
1,690225 |
1 |
0 |

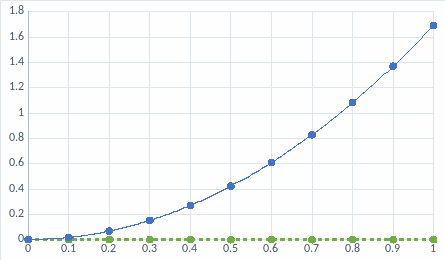
Рис. 9. Концентрационная зависимость коэффициента активности для Ge в жидкой фазе

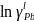
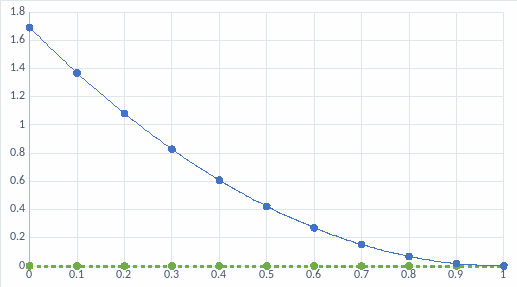
Рис. 10. Концентрационная зависимость коэффициента активности для Pb в жидкой фазе
4. Используя T-x-проекцию диаграммы состояния рассчитать равновесный коэффициент распределения компонента B (примесь) при
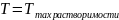 .
.
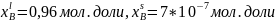
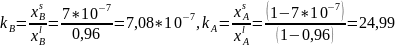
Теоретический расчет:
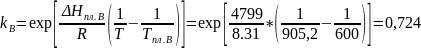
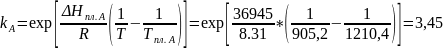
5.
Рассчитать и построить спинодали при
температурах от
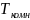 до
до
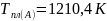 .
Показать на крупномасштабной T-xдиаграмме
заданной системы области стабильных
(равновесных), метастабильных, лабильных
твердых растворов.
.
Показать на крупномасштабной T-xдиаграмме
заданной системы области стабильных
(равновесных), метастабильных, лабильных
твердых растворов.
Таблица 5: Температурная зависимость состава линий спинодали для твердых растворов
T, К |
|
|
298 |
0,01246753 |
0,98753247 |
400 |
0,016808833 |
0,983191167 |
500 |
0,021103216 |
0,978896784 |
600 |
0,025436457 |
0,974563543 |
700 |
0,029809632 |
0,970190368 |
800 |
0,034223865 |
0,965776135 |
900 |
0,038680334 |
0,961319666 |
1000 |
0,043180276 |
0,956819724 |
1100 |
0,047724988 |
0,952275012 |
1210,4 |
0,052795988 |
0,947204012 |
Пример
расчета для
 :
:
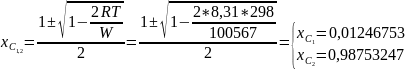
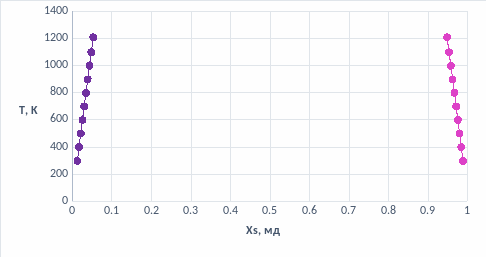
Рис. 11. Температурная зависимость состава линий спинодали
lg(XS)
Т, К

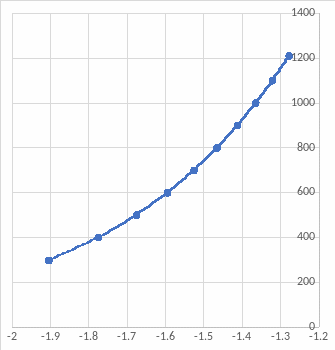
Рис. 12. Температурная зависимость состава линии спинодали (логарифмический масштаб по оси составов)
А Б В
Рис. 13. Диаграмма состояния системы (логарифмический масштаб по оси составов), где А – стабильная область, Б – метастабильная область, В – лабильная область
Вывод
В ходе выполнения лабораторной работы посредством компьютерного моделирования были исследованы фазовые равновесия типа полупроводник (Ge) – примесь (Pb).
Были определены следующие параметры и зависимости: концентрационные зависимости коэффициентов активностей компонентов в жидком и твердых растворах, равновесный коэффициент распределения компонента B(Pb), температурные зависимости состава линий спинодали в интервале температур от Tкомн до Тпл(Ge) .
В качестве модели, наиболее близко описывающей исследуемую систему, была выбрана модель регулярного раствора, т.к. её графики точнее всего совпадают с экспериментальными данными.
Кроме этого, были найдены области лабильного, метастабильного и стабильного состояния растворов в заданной системе (рис. 13).