
Содержание
Содержание 2
Введение 4
Понятие энтропии 5
Измерение энтропии 8
Понятия и примеры возрастания энтропии 9
Заключение 13
Список литературы 14
Введение
Естествознание – это раздел науки основанный на воспроизводимой эмпирической проверке гипотез и создании теорий или эмпирических обобщений, описывающих природные явления.
Предмет естествознания - факты и явления, воспринимаемые нашими органами чувств. Задача ученого обобщить эти факты и создать теоретическую модель изучаемого явления природы включающую законы управляющие им. Явления, например, закон всемирного тяготения, даются нам в опыте; один из законов науки - закон всемирного тяготения, представляет собой варианты объяснения этих явлений. Факты, будучи установлены, сохраняют свою актуальность всегда, законы могут быть пересмотрены или скорректированы в соответствии с новыми данными или новой концепцией их объясняющей. Факты действительности являются необходимой составляющей научного исследования.
Основной принцип естествознания гласит1: знания о природе должны допускать эмпирическую проверку. Это не означает, что научная теория должна немедленно подтверждаться, но каждое ее положение должно быть таким, чтобы такая проверка была возможна в принципе.
От технических наук естествознание отличает то, что оно преимущественно направлено не на преобразование мира, а на его познание. От математики естествознание отличает то, что оно исследует природные, а не знаковые системы. Попробовать связать естествознание, технические и математическую науки попробуем с помощью понятия – «энтропия».
Таким образом, целью данной работы является рассмотрение и решение следующих задач:
Понятие энтропии;
Измерение энтропии;
Понятия и примеры возрастания энтропии.
Понятие энтропии
Понятие энтропии было введено Р. Клаузиусом2, сформулировавшим второе начало термодинамики, согласно которому переход теплоты от более холодного тела к более теплому не может происходить без затраты внешней работы.
Он определил изменение энтропии термодинамической системы при обратимом процессе как отношение изменения общего количества тепла ΔQ к величине абсолютной температуры T:
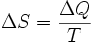
Рудольф Клаузиус дал величине S имя «энтропия», происходящее от греческого слова τρoπή, «изменение» (изменение, превращение, преобразование).
Эта формула применима только для изотермического процесса (происходящего при постоянной температуре). Её обобщение на случай произвольного квазистатического процесса выглядит так:
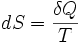 ,
,
где dS - приращение (дифференциал) энтропии, а δQ - бесконечно малое приращение количества теплоты.
Заметим, что энтропия является функцией состояния, поэтому в левой части равенства стоит её полный дифференциал. Напротив, количество теплоты являетсяфункцией процесса, в котором эта теплота была передана, поэтому δQ ни в коем случае нельзя считать полным дифференциалом.
Энтропия, таким образом, определена вплоть до произвольной аддитивной постоянной. Третье начало термодинамикипозволяет определить её точно: при этом энтропию равновесной системы при абсолютном нуле температуры считают равной нулю.
Энтропия – это количественная мера той теплоты, которая не переходит в работу.
S2
-S1
=ΔS=
![]()
![]()
Или, другими словами, энтропия – мера рассеивания свободной энергии. А ведь нам уже известно, что любая открытая термодинамическая система в стационарном состоянии стремится к минимальному рассеиванию свободной энергии. Поэтому если в силу причин система отклонилась от стационарного состояния, то вследствие стремления системы к минимальной энтропии, в ней возникают внутренние изменения, возвращающие ее в стационарное состояние.
Как видно из выше написанного, энтропия характеризует определенную направленность процесса в замкнутой системе. В соответствии со вторым началом термодинамики3 возрастанию энтропии соответствует направление теплового потока от более горячего тела к менее горячему. Непрерывное возрастание энтропии в замкнутой системе происходит до тех пор, пока температура не выровняется по всему объему системы. Наступает, как говорят, термодинамическое равновесие системы, при котором исчезают направленные тепловые потоки и система становится однородной.
Абсолютное значение энтропии зависит от целого ряда физических параметров. При фиксированном объеме энтропия увеличивается с увеличением температуры системы, а при фиксированной температуре увеличивается с увеличением объема и уменьшением давления. Нагревание системы сопровождается фазовыми превращениями и снижением степени упорядоченности системы, поскольку твердое тело переходит в жидкость, а жидкость превращается в газ. При охлаждении вещества происходит обратный процесс, упорядоченность системы возрастает. Эта упорядоченность проявляется в том, что молекулы вещества занимают все более определенное положение относительно друг друга. В твердом теле их положение фиксировано структурой кристаллической решетки.
Другими словами - энтропия выступает мерой хаоса4 (споры определения которого ведутся уже давно).
Все процессы в природе протекают в направлении увеличения энтропии. Термодинамическому равновесию системы соответствует состояние с максимумом энтропии. Равновесие, которому соответствует максимум энтропии, называется абсолютно устойчивым. Таким образом, увеличение энтропии системы означает переход в состояние, имеющее большую вероятность. То есть энтропия характеризует вероятность, с которой устанавливается то или иное состояние, и является мерой хаотичности или необратимости. Это мера хаоса в расположении атомов, фотонов, электронов и других частиц. Чем больше порядка, тем меньше энтропия. Чем больше информации поступает в систему, тем система более организована, и тем меньше её энтропия:
![]()
(По теории Шеннона5)
