
8988
.pdf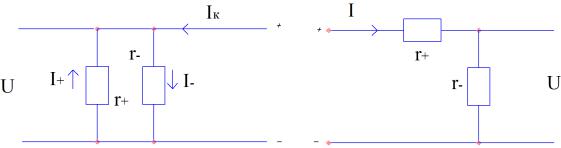
ал трубопровода по причине выноса потенциала будет оставаться практически равным φс, т. е. φс ≈ φс’, в отличие от потенциала грунта φг’ в той же точке φс’.
Таким образом, Uизм = φс – φс’(– φг + φмэс) для точки С (в точке дренажа).
Для отдаленной точки С’ при φс ≈ φс’ и φг’ ≈ 0, а φмэс = const , получим измеряе-
мое напряжение в точке дренажа всегда Uизм > U’изм, хотя потенциал φс’ на большом расстоянии S практически, как выше отмечено, остается равным φс ≈ φс’.
Таким образом, измеряемый потенциал по длине трубопровода не позво-
ляет в полной мере судить о полноте катодной защиты.
Трубопровод защищен при условии iА = iК = 0 или iС = iА = i0' , а не при усло-
вии |φс| = | – φг|.
8.4. Использование опытных данных для определения электрических параметров в электродных системах
Для расчета электрических цепей широко используются схемы замещения источника электромагнитной энергии. Существуют две схемы замещения ис-
точника постоянного тока: параллельная схема замещения и последовательная
(рис. 26 а, б).
а |
б |
Рис. 26. Схемы замещения источника постоянного тока:
а – параллельная схема замещения; б – последовательная схема замещения
130
Анализ этих схем показывает, что относительно внешней цепи они дают одинаковые значения U, I, P только при условии, когда Iк = E/r. В схемах с ре-
альными устройствами, конденсаторами, индуктивностями и резисторами, па-
раметры которых практически не изменяются, последовательная схема считает-
ся основной.
Однако в проводниках второго рода ток в токоприемнике (например, в
электролитах) движется одновременно и встречно с различными скоростями,
зависящими от величины ЭДС.
При этом условии Iк = E/r практически всегда нарушается, и тогда последо-
вательная схема не выполняет своей расчетной функции. В проводниках второ-
го рода при регулировании ЭДС источника ток анионов может равняться току катионов, тогда возникает ситуация, при которой ЭДС становится равной на-
пряжению.
В этом случае реальному процессу соответствует параллельная схема за-
мещения. Неопределенность данной ситуации затрудняет применение как од-
ной схемы замещения, так и другой.
В данной работе приводится расчет электрических параметров производ-
ственного процесса кадмирования по экспериментальным данным прямых из-
мерений [11, 16].
Исходные |
данные |
производственного |
процесса |
кадмирования: |
t,◦C = 18–30, δ = 1–2 A/ дм², толщина покрытия 6–9 |
мкр – продолжительность |
|||
≈50 мин, толщина покрытия 12–15 мкр – ≈80–90 мин. Состав: 1. Кадмий серно-
кислый 50–80 г/л., 2. Кислота серная 50–100 г/л., 3. Эмульгатор ОП-10 5–10 г/л.
Таблица 11
Экспериментальные данные одновременной фиксации электрических параметров при производственном кадмировании
Мощность Рw, Вт |
170 |
70 |
68 |
65 |
|
|
|
|
|
Ток I+, А |
22,1 |
9,5 |
9,5 |
8,6 |
|
|
|
|
|
Падение напряжения U, В |
1,5 |
0,75 |
0,5 |
1 |
|
|
|
|
|
131
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Таблица 12 |
||
|
|
|
|
Расчеты по данным прямых измерений |
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||
|
Напряженность |
Напряженность поля |
|
Ток, образованный |
|
|
Кажущееся |
|||||||||
|
стороннего поля |
EAK = U − EAKстор , B |
|
|
|
катионами |
|
|
сопротивление |
|||||||
|
стор |
= P / I , B |
|
|
|
I− = ЕAK / z, A |
|
|
r+ = z =U / I,Ом |
|||||||
|
E AK |
|
|
|
|
|
|
|
|
|||||||
|
170/22,1 = 7,6923 |
1,5–7,6923 = –6,192 |
|
–6,192/0,0679 = –91,192 |
|
1,5/22, 1 = 0,0679 |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
70/9,5 = 7,3684 |
0,75–7,3684 = –6,6184 |
–6,6184/0,078 |
9 = –83,8834 |
|
0,0789 |
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
68/9,5 = 7,1579 |
0,5–7,1579 = –6,6579 |
|
–6,6579/0,0526 |
= –126,576 |
|
0,0526 |
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
65/8,6 = 7,5581 |
1–7,5581 = –6,5581 |
|
–6,5581/0,1162 = |
–56,438 |
|
0,1162 |
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Таблица 13 |
||
|
|
|
|
Расчетные дополнительные данные |
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
Р+ = I+·U, Вт |
|
|
|
33,15 |
|
7,125 |
|
|
4,75 |
|
8,6 |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
P– = Pw – P+, |
Вт |
|
|
|
136,85 |
62,875 |
|
|
63,325 |
|
56,4 |
||
|
|
|
|
|
|
|
|
|
|
|||||||
|
Проводимость анионов |
g+ = P+/U²,Ом–1 |
|
1,47333 |
1,26666 |
|
19 |
|
8,6 |
|||||||
|
Проводимость катионов g– = P–/U², |
Ом–1 |
|
60,822 |
111,7777 |
|
253,3 |
|
56,4 |
|||||||
|
Сопротивление катионам r– = U/I–, |
Ом–1 |
|
0,0164 |
0,0789 |
|
|
0,0526 |
|
0,1162 |
||||||
|
|
|
Падение напряжения на активном |
|
7,691 |
|
7,3682 |
|
|
7,1573 |
|
7,5508 |
||||
|
|
|
сопротивлении анионов U+ = I+R |
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|||||||
|
Падение напряжения катионов U_ = I_·z |
|
6,1919 |
6,6184 |
|
|
6,6579 |
|
6,558 |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
Измеряемое напряжение U = U+ – U_ |
|
1,5 |
|
0,7498 |
|
|
0,499 |
|
0,993 |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Выводы
1. Анализ таблиц производственных измерений показывает, что известные схемы замещения не могут быть использованы для расчета электрических па-
раметров с целью определения ситуации, при которой ток в среде становится равным нулю, т. е. критерия прекращения процесса.
2. Из табл. 12 видно, что в процессе кадмирования постоянно изменяются:
напряженность стороннего поля, поля источника и величины токов анионов и катионов.
3. Измеряемое напряжение U (табл. 13) есть падение напряжения, а не на-
пряжение источника, поскольку U = U+ – U – , т. е. U равно разности падений на-
пряжений анионов и катионов.
132
4. Для расчета электрических параметров в цепях с проводниками второго рода необходимо применять теорию, учитывающую резкое изменение парамет-
ров среды εµ [15, 19].
Только в этом случае можно отказаться от многочисленных методических указаний, инструкций для различных сред.
8.5. Экспериментальные исследования производственной системы
катодной защиты
В настоящее время используется контроль полноты катодной защиты по косвенным измерениям потенциального состояния защищаемого сооружения.
Такие измерения часто приводят к ошибочным выводам, снижению надежности и безопасности эксплуатации газопроводов, нефтепроводов и других строи-
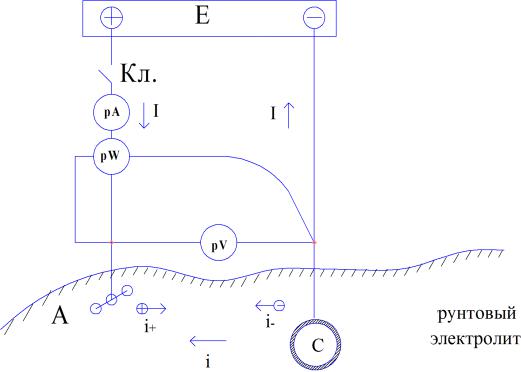
тельных конструкций. На рис. 27 представлена принципиальная схема системы катодной защиты.
Г
Рис. 27. Принципиальная схема катодной защиты
133
Описание эксперимента
Если ключ Кл отключен, мы имеем два источника. Один источник вы-
прямленного напряжения с ЭДС, Е – источник катодной защиты и другой ис-
точник тока, образованный гальваническими токами i+, i– защищаемого соору-
жения С и анодного заземления А. Одновременно заметим, что локализовать гальванический источник с показателями его электрических параметров с вы-
сокой для практики точностью не удаётся. Хорошо известно, что в любой элек-
тродной системе, в том числе и в системе катодной защиты, ток обусловлен од-
новременным и противополярным движением анионов и катионов. Другого то-
ка в электролитах не образуется.
Если Кл включен, амперметр рА зафиксирует ток I в цепи системы катод-
ной защиты, но не ток i в электролите; вольтметр зафиксирует падение напря-
жения под воздействием суммарного значения токов i– и i+, но не напряжение
источника; ваттметр зафиксирует Р – полную активную мощность, поскольку
Р = Р+ + Р– , где Р+ – затраченная электромагнитная энергия, P = IE на превра-
щение химической энергии в гальваническом элементе и Р– – на преобразова-
ние в теплоту.
Таким образом, прямыми измерениями можно получить основные и доста-
точные данные для анализа и контроля полноты катодной защиты.
С этой целью, регулируя источником Е напряжение, получим величину
зафиксированных амперметром токов от Imin до Imax, вольтметром – |
падение на- |
||||||
пряжений и ваттметром – |
мощностей. Данные сведем в табл. 14. |
|
|
||||
|
|
|
|
|
|
|
Таблица 14 |
|
|
Данные прямых измерений |
|
|
|
||
|
|
|
|
|
|
|
|
Ток I, A |
|
3 |
5 |
8 |
10 |
|
12 |
|
|
|
|
|
|
|
|
Напряжение U, B |
|
5 |
10 |
15 |
18 |
|
25 |
|
|
|
|
|
|
|
|
Мощность Р, Вт |
|
43,75 |
118,75 |
250 |
325 |
|
550 |
|
|
|
|
|
|
|
|
134
По данным прямых измерений проведем расчеты для каждого фиксиро-
ванного шага и сведем их в табл. 15.
|
|
|
|
|
Таблица 15 |
|
|
Расчетные данные |
|
|
|
|
|
|
|
|
|
g = P/U2, Ом– 1 |
1,75 |
1,187 |
1,11 |
1,0 |
0,88 |
|
|
|
|
|
|
r+ = U/I, Ом– 1 |
1,66 |
2 |
1,875 |
1,8 |
2,1 |
|
|
|
|
|
|
g+ = 1/ r+, Ом– 1 |
0,6 |
0,5 |
0,53 |
0,55 |
0,48 |
|
|
|
|
|
|
g– = g – g +, Ом– 1 |
1,15 |
0,67 |
0,58 |
0,44 |
0,4 |
|
|
|
|
|
|
Достаточным и единственным условием резонанса токов в электролите яв-
ляется равенство проводимостей положительно и отрицательно заряженных ионов. Только в этом случае не будет тока в проводнике и наступит электроли-
тическое равновесие, а Е = −Естор .
По данным |
g+ и g– для каждого фиксированного напряжения построим за- |
||||||||||||||||||||||||||||
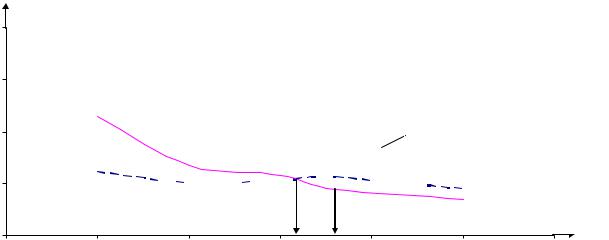
висимости g+, g– |
= f(U) (рис. 28). |
||||||||||||||||||||||||||||
g+, g– , Ом– 1 |
|||||||||||||||||||||||||||||
2,0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1,5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
1,0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
g+ |
|
|
0,5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
U, B |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,0
0 |
5 |
10 |
15 |
18 |
20 |
25 |
30 |
Рис. 28. Зависимости проводимостей положительно и отрицательно
заряженных частиц от уровня приложенного напряжения
135
Как видим, точка пересечения кривых определяет эффективную полноту катодной защиты и величину напряжения, при которой она возможна (реализу-
ется). В этом случае ток анионов i+ равен току i– катионов (наблюдается свое-
образный резонанс).
При этом заметим, что измеряемое напряжение на клеммах электродов в электролитах представляет собой сумму падений напряжений, произведения ионного тока I– , направленного от катода к аноду, на соответствующее ему со-
противление r– и произведения ионного тока I+, направленного к катоду от ано-
да на соответствующее сопротивление r+, при этом полная сила тока является определяющей мерой переноса суммарного заряда положительно и отрица-
тельно заряженных ионов, а не напряжение на клеммах.
136

Глава 9
РАЗВИТИЕ ТЕОРИИ И ЭКСПЕРИМЕНТАЛЬНОГО ИССЛЕДОВАНИЯ ЭЛЕКТРОЛИТОВ ПО ПРОВОДИМОСТИ
Легко измерять, труднее знать, что измеряешь!
Творцы ньютоновской механики
Для получения данных электропроводности необходимо измерять сопро-
тивление между двумя электродами. Однако известные способы измерения со-
противлений электролитов требуют точного поддержания заданной температу-
ры, устранения поляризации электродов, высокой точности электрических из-
мерительных систем. В эксплуатационных условиях в большинстве случаев ни одно из упомянутых требований не может быть выполнено. Поэтому до на-
стоящего времени на практике используется весьма сомнительный, научно не обоснованный способ определения электролитического равновесия по потен-
циалу относительно медносульфатного электрода сравнения или другого.
9.1. Взаимодействие диссоциирующей силы и диэлектрической
проницаемости под влиянием электромагнитной энергии
В. Нернст и Дж. Томсон отмечали, что диссоциирующая сила различных жидкостей практически пропорциональна их диэлектрической проницаемости:
диэлектрическая проницаемость бензола ε = 2,5; эфира ε = 4,1; алкоголя ε = 25;
муравьиной кислоты ε = 62; воды ε = 81. В таком же порядке идут и диссоции-
рующие силы, способные образовывать электролитические растворы. Этот па-
раллелизм диссоциирующей силы и диэлектрической проницаемости до неко-
торой степени можно пояснить взаимодействиями между ионами, т. к. электри-
ческие силы обратно пропорциональны диэлектрической проницаемости. При этом установлено, что в растворителях с высоким значением ε электролиты ве-
137

дут себя как сильные, а в растворителях со средним и низким значениями ε – как слабые. При увеличении ε растворители становятся, как правило, более по-
лярными. Растворители с низкой диэлектрической проницаемостью – неполяр-
ные жидкости. По величине диэлектрической проницаемости ε известна и их классификация: ε > 50 – сильные электролиты, ε < 12–50 – слабые. В растворе мерой движения являются положительно и отрицательно заряженные анионы и катионы, движущиеся одновременно и встречно друг к другу. Памятуя, что под энергией понимается единая мера различных форм движения, а энергия преоб-
разуется только в форме работы и теплоты, можно заключить, что в электриче-
ской цепи, где токоприемником является электролитическая «ванна», можно составить математическую модель и молекулярно-кинетическую схему движе-
ния микрочастиц [6].
Рис. 29. Молекулярно-кинетическая модель измерения электрических параметров в проводниках первого рода: ∫ ES ds = 0.
Как видим, в «ванне» (рис. 29) частицы движутся навстречу противопо-
лярно соответственно их массам. Следовательно, задача сводится к нахожде-
нию общего тока, образованного в электролитической «ванне» анионами с со-
ответствующим им сопротивлением и катионами с другим соответствующим им сопротивлением под воздействием постоянной электромагнитной энергии (а
не напряжения и тока, измеряемых в металлическом проводнике первого рода).
138
Таким образом, ток в электролитической ванне обусловлен величиной положи-
тельного заряда в соответствии с законом Фарадея, (выделенного вещества),
величиной диэлектрической проницаемости εа, потоком Гаусса, связанного с величиной потока напряженности электромагнитной энергии, поскольку каж-
дая точка поля характеризуется энергией, а потенциалы каждой точки φА и φК –
скалярные величины: F = EA·g = Q·g/ 4·π·r2·εаt , где Q – электрический заряд,
создающий поле; g – пробный положительный заряд; r – расстояние между за-
рядами; εаt – диэлектрическая проницаемость среды при соответствующей тем-
пературе [7]. Поэтому разность потенциалов двух точек характеризует напря-
жение, а напряжение характеризуется энергией, затраченной на перемещение единицы пробного положительного заряда g на расстояние l между этими точ-
ками, т. е. UАК = WАК/g = φA – φК = F·l/g = E·l, тогда φ = W/g = Дж/Кл = В. По-
скольку энергия, необходимая для вырывания или переноса электрона от одно-
го атома к другому, приблизительно равна 1В, умноженному на элементарный заряд, очевидно, поэтому за единицу измерения в исследованиях химических реакций следует принять электрон-вольт: 1В = 1,6·10–19 Дж/элем. заряд, тогда
1А = 6,25·10+18 элем. зарядов.
Учитывая вышеизложенное, мы предлагаем электродинамический подход к рассмотрению процессов в электродных системах. В этом случае электромаг-
нитная энергия воздействует на токоприемник, в свою очередь токоприемник воздействует на источник и результатом этого взаимодействия является ток между электродами. Электрический ток в «ванне» принимается равным сумме токов, образованных одновременным действием противополярных ионов, и на-
правлен от катода к аноду вопреки отталкиванию этих частиц от зажимов ис-
точника энергии. В этом процессе используется химическая энергия для на-
сильственного перемещения заряженных частиц к зажимам источника.
В электрической цепи Ома постоянный или выпрямленный ток является замкнутой субстанцией и определяется направленным потоком заряженных
139
